Шарипов И.З. Физика металлов
Подождите немного. Документ загружается.

Министерство общего и профессионального образования
Российской Федерации
УФИМСКИЙ ГОСУДАРСТВЕННЫЙ АВИАЦИОННЫЙ ТЕХНИЧЕСКИЙ
УНИВЕРСИТЕТ
Шарипов И.З.
Физика металлов
Учебное пособие
Уфа 2004
Физика металлов. Учебное пособие.
Уфа: УГАТУ, 2004.
В учебном пособии изложены основы строения и физики явлений,
происходящих в металлических материалах. Рассмотрено влияние структуры,
химического состава на их свойства. Пособие рассчитано на студентов обучающихся
по заочной и вечерней форме по направлениям «Физика металлов» и
«Материаловедение».
Рецензенты:
Проф. кафедры «Общей технологии и металловедения» УГАТУ Астанин В.В.
Д. физ.-мат. наук, с.н.с. ИПСМ РАН Пшеничнюк А.И.
© Уфимский государственный авиационный технический университет, 2004.
2
ВВЕДЕНИЕ...............................................................................................................................5
I. СТРОЕНИЕ ВЕЩЕСТВ.........................................................................................................7
1. Межатомное взаимодействие...................................................................................................7
2. Типы химических связей........................................................................................................10
3. Кристаллическая структура твердых тел...........................................................................15
4. Дефекты кристаллических решеток....................................................................................17
4.1 Точечные дефекты решетки...............................................................................................18
4.2 Линейные дефекты кристаллической решетки................................................................21
4.3 Поверхностные дефекты кристаллической решетки.......................................................24
4.4 Объёмные дефекты кристаллической решетки................................................................29
4.5 Энергетические дефекты кристаллической решетки......................................................30
5. Основы теории сплавов..........................................................................................................31
6. Диаграммы состояния сплавов и закономерности Курнакова......................................33
7. Строение электронных зон. Проводники, диэлектрики и полупроводники.
...37
II. КРИСТАЛЛИЗАЦИЯ МЕТАЛЛОВ....................................................................................39
1. Самопроизвольная кристаллизация....................................................................................39
2. Несамопроизвольная кристаллизация................................................................................43
3. Получение монокристаллов...................................................................................................43
4. Аморфное состояние металлов..............................................................................................45
5. Полиморфизм............................................................................................................................46
III. ПРОВОДНИКОВЫЕ МАТЕРИАЛЫ.................................................................................47
1 Материалы высокой электропроводности..........................................................................48
3
2 Материалы высокого удельного сопротивления...............................................................50
2.1 Сплавы на основе меди.......................................................................................................50
2.2 Никель-хромовые сплавы...................................................................................................51
2.3 Железохромалюминиевые сплавы.....................................................................................51
2.4 Сплавы на основе благородных металлов........................................................................52
3 Материалы электрических контактов.................................................................................52
3.1 Зажимные контакты............................................................................................................52
3.2 Цельнометаллические контакты........................................................................................52
3.3 Материалы разрывных контактов.....................................................................................54
3.4 Материалы скользящих контактов....................................................................................55
IV. МАГНИТНЫЕ МАТЕРИАЛЫ...........................................................................................56
1. Природа ферромагнетизма.....................................................................................................56
1.1. Доменная структура ферромагнетиков............................................................................57
1.2. Кривая намагничивания....................................................................................................58
2. Основные классы магнитных материалов.........................................................................61
2.1. Промышленные магнитомягкие материалы....................................................................61
2.2 Магнитомягкие материалы для работы в слабых полях.................................................63
2.3 Магнитомягкие материалы, для работы в высокочастотных полях..............................64
3. Магнитотвердые материалы.................................................................................................66
3.1 Промышленные магнитотвердые материалы...................................................................66
3.2. Дисперсионно твердеющие сплавы..................................................................................68
3.3 Деформируемые магнитотвердые материалы..................................................................68
3.4 Магнитотвердые ферриты..................................................................................................69
3.5 Высококоэрцитивные магниты..........................................................................................70
4
ВВЕДЕНИЕ
Умение получать необходимые материалы из имеющихся в окружающем
мире ресурсов является необходимой предпосылкой развития цивилизации. В
древние времен для создания орудия и инструмента человек применял только
те материалы, которые ему предлагала природа - дерево, камень, так или иначе
отвечающие требованиям твердости, прочности.
Около 6-7 тыс лет назад человек начал использовать самородные
металлы: золото, серебро, медь, добыча которых не требовала больших знаний
и техники. В 4-3 тысячелетии до н. э. научились выплавлять металл из руды:
медь, олово, свинец. Благодаря добавлению относительно легко получаемого
олова к меди получили новый материал сплав бронзу. В сплаве удалось снизить
точку плавления по сравнению с медью (медь Т
пл
- 1083
о
С, бронза Т
пл
ниже
415
о
С), что значительно облегчило обработку этого сплава. Началась бронзовая
эра. Применение железа началось во II тысячелетии в Египте и Малой Азии,
затем распространилось в Европу. Железо тверже , прочнее меди и бронзы,
поэтому народы овладевшие новой технологией становились лидерами в
развитии цивилизации. Это открыло железный век - эпоху железного меча, а
также железного плуга и топора. К XVII - XVIII вв. железо стало наиболее
употребляемым металлом.
Рассмотрим любопытную таблицу:
Таблица 1.
Металл Au
1+
Ag
1+
Cu
2+
Sn
2+
Fe
2+
Zn
2+
Al
3+
Mg
3+
Электро-
химич.
потенциал,
е
о
+1,5 +0,81 +0,34 0,14 0,44 0,76 1,67 2,34
Начало
освоения
4 тыс.
лет
до н.э.
4 тыс.
лет
до н.э.
3
тыс .ле
т
до н.э.
2 тыс.
лет
до н.э.
1 тыс.
лет
до н.э.
15 век
н.э
1850
н.э
1850
н.э
Мы видим, что положение металла в электрохимическом ряду
напряжений определяет время его освоения, что, в свою очередь, оказало
значительно большее влияния на развитие человечества, чем события и
личности, которые историки выдвигают на передний план. Человек начинал
активно использовать тот или иной металл лишь после накопления
определенной суммы знаний, овладев достаточным мастерством. Так, железо
или цинк требовали более высокоразвитой технологии по сравнению с
благородными металлами, а металлы как алюминий и магний освоены совсем
5
недавно. Титан, как элемент, был открыт в 1791 году, а получить первые тонны
промышленного металла смогли лишь в 1948 году.
Уже в ранние исторические времена были развиты технические приемы
по регулированию свойств материалов. Применением различных
технологических приемов можно задавать материалу различные свойства как
прочность, жаростойкость, коррозионная стойкость, получать комбинации или
соединения материалов, которые обычными способами достигнуть нельзя. С
развитием технологии стало возможно массовое производство микро
легированных сталей, материалов с направленной кристаллизацией,
монокристаллов, аморфных сплавов, композиционных материалов, металлов с
памятью формы и др.
Обратившись к истории техники мы можем увидеть тесную связь между
техническим прогрессом и наличием подходящих материалов. Например, в
1820 году в Англии была запатентована прокатка сортового металла, что дало
толчок строительству железных дорог, так как стало возможным изготавливать
рельсы в большом количестве и с высокой точностью. Новые технологии и
специальные сплавы позволяют сегодня создавать компьютеры, мощные
самолеты, космическую и ядерную технику. Поэтому современному
специалисту крайне важно знание многообразия применяемых металлических
материалов и умение сделать выбор наиболее эффективного материала для
конкретной цели.
В учебном пособии даются представления об основные процессах и
явлениях происходящих в металлических материалах при различных
технологических операциях.
6
I. СТРОЕНИЕ ВЕЩЕСТВ.
1. Межатомное взаимодействие.
Любой материал представляет собой продукт взаимодействия огромного
количества атомов одного или нескольких химических элементов. Его свойства
прежде всего зависят от типа и энергии химической связи составляющих
атомов. При любом характере взаимодействия частицы тела стремятся
расположиться в таком порядке и на таких расстояниях, которые
обусловливают относительный минимум энергии всей системы, иными
словами, ее наиболее устойчивое в данных условиях состояние.
Взаимодействие множества атомов в основном определяются
взаимодействием соседних атомов, поэтому вначале для простоты рассмотрим
взаимодействие двух атомов
При очень больших взаимных расстояниях атомы практически не
взаимодействуют друг с другом, так что энергию их можно считать постоянной
и равной нулю. При уменьшении расстояния между атомами проявляются силы
притяжения и потенциальная энергия понижается. При некотором равновесном
расстоянии R энергия W принимает минимальное значение, а результирующая
сила взаимодействия F = dW/dR становится равной нулю. Это равновесное
расстояние между частицами обозначим R
0
. При дальнейшем сближении
частиц возникнут силы отталкивания, так как внешние слои атомов,
заряженные отрицательно, придут в тесное соприкосновение.
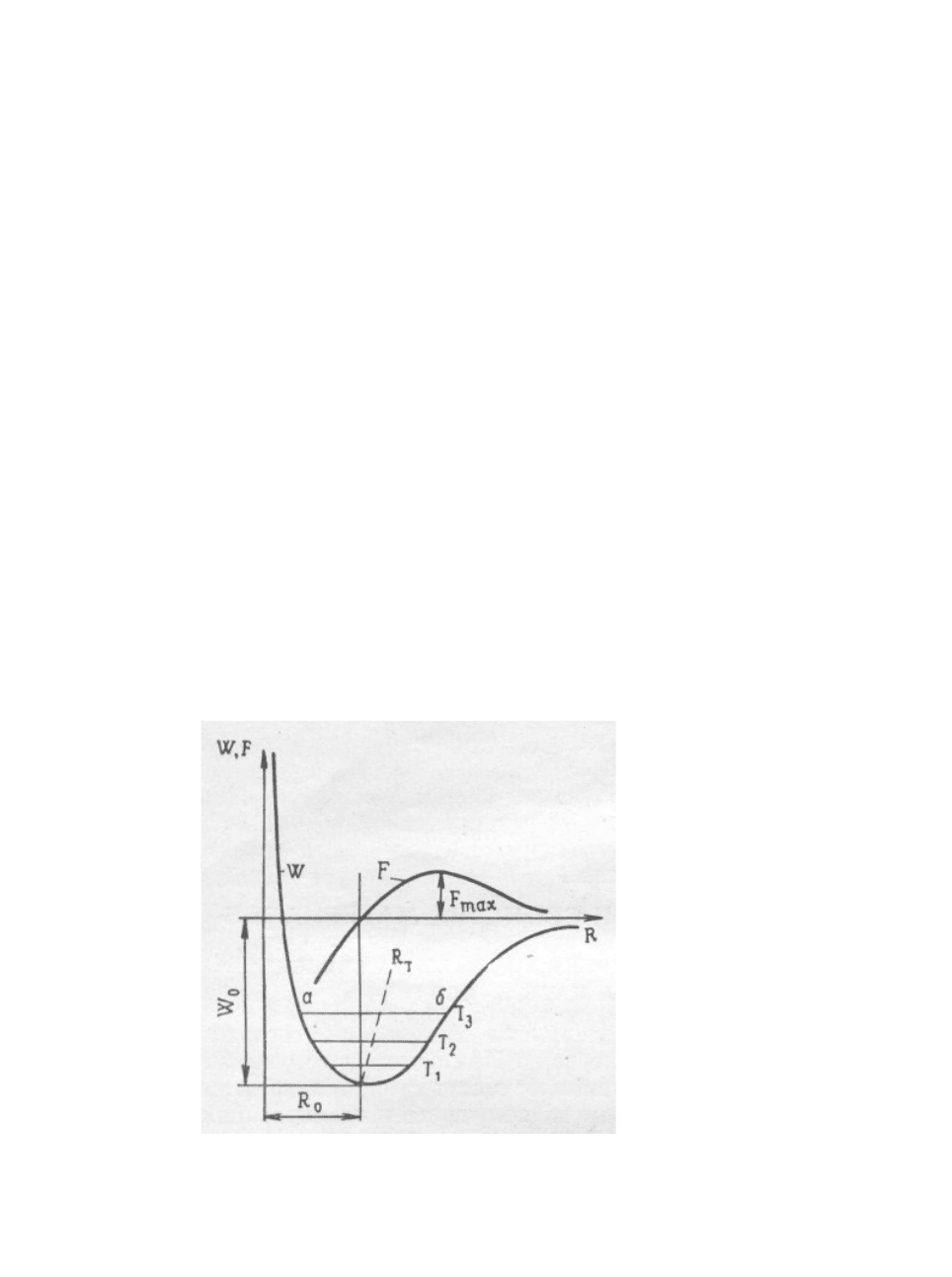
Общая зависимость изменения энергии W и сил взаимодействия F пары
частиц в молекулах отражается графиком, приведенным на рисунке 1.
Рис. 1 Потенциальная энергия W и сила F взаимодействия двух атомов.
В условиях равновесия частицы располагаются в минимумах
потенциальной кривой — в «потенциальных ямах».
7
Величина W
o
характеризует энергию связи частиц, т. е. ту энергию,
которую нужно затратить, чтобы разобщить частицы тела. Максимум величины
F представляет собой теоретическое усилие, которое может выдержать тело при
упругом растяжении.
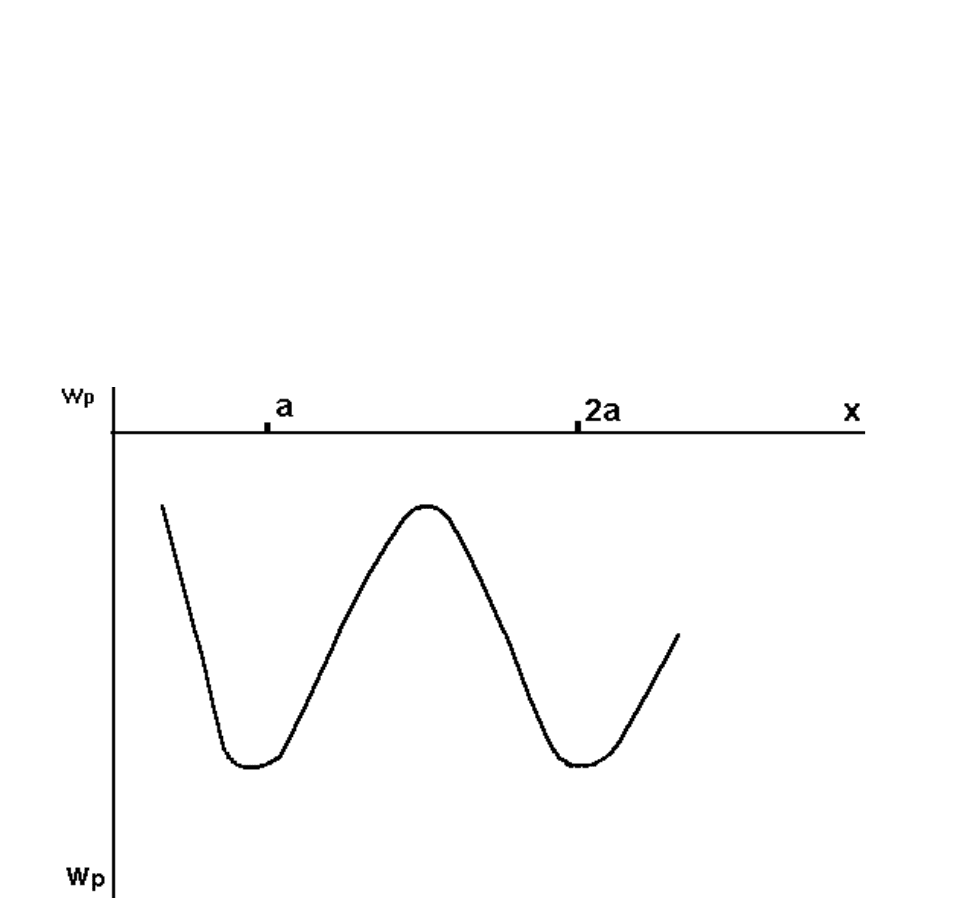
В том случае, когда взаимодействует множество атомов, смещение
любого из них приводит к росту энергии системы, Поэтому потенциальную
кривую можно представить в виде периодической функции (рис. 2). При
минимуме энергии системы расстояния между атомами одинаковы и равны R
0
.
Вдоль любого направления расстояния будут равны R
0
, хотя эти расстояния по
разным направлениям будут разными. Расстояние между атомами вдоль
какого-либо направления называют периодом кристаллической решетки и
обозначают буквами: а, b, c и т.д..
Для перехода атома из одного равновесного положения в другое
необходимо преодолеть потенциальный барьер ΔW . Величина ΔW — энергия
перехода частиц из одного относительно устойчивого состояния в другое. В
том случае, когда энергия системы мала, атомы не могут перемещаться из
одного положения в другое, и мы имеем дело с твердым телом. При повышении
энергии системы атомы активно колеблются, обмениваются энергией - и в
результате некоторые частицы могут перескакивать из одного положения в
другое. В этом случае мы имеем дело с жидким телом. Температура
превращения в жидкость или температура плавления – важнейшая
характеристика материала. Дальнейший рост тепловой энергии системы
приводит к выходу атомов из потенциальной ямы, они начинают двигаться
беспорядочно, могут занимать различные положения – и мы имеем дело с
газом. Переход в газообразное состояние определяет температуру испарения
вещества.
Рис. 2. Зависимость энергии потенциального взаимодействия (Wp) от
расстояния между атомами (x) для случая взаимодействия множества атомов.
8
Знание кривых взаимодействия позволяет судить о ряде общих свойств тел
и особенностях их поведения. Чем ниже расположена точка W
o
, тем выше
энергия связи частиц тела, выше его температура плавления и испарения. Чем
больше глубина потенциальной ямы, тем круче ее стенки , тем большая сила
возникает при смещении атома из положения равновесия, эначит тем больше
модуль упругости материала.
Другой интересной особенностью влияния формы кривой взаимодействия
на свойства материалов является термическое расширение. Увеличение энергии
системы двух атомов за счет роста температуры ведет к взаимному смещению
атомов относительно друг друга в пределах, определяемых стенками
потенциальной ямы. С ростом энергии системы амплитуда колебаний
возрастает (см. на рис. 1, отрезки, соответствующие Т
3
>T
2
>T
1
). Как видно из
рисунка, кривая потенциальная кривая асимметрична, поэтому при росте
температуры середина отрезков постепенно смещается вправо. Это означает,
что среднее расстояние между атомами увеличивается, а значит и линейные
размеры тела увеличиваются. Изменение линейных размеров тела при нагреве
описывается коэффициентом теплового расширения: a
Т
= (1/L)(L/T). Чем
более асимметрична кривая взаимодействия, тем больше коэффициент
теплового расширения a
Т
.
При увеличении глубины потенциальной ямы W
o
форма стенок становится
более симметричной, а значит коэффициент теплового расширения a
Т
уменьшается.
Таким образом, свойства материалов оказываются взаимосвязаны.
Поэтому зная одни свойства вещества можно предсказать другие. Например,
как было рассмотрено, увеличение глубины потенциальной ямы ведет к росту
температуры плавления и температуры испарения вещества. Вместе с тем,
увеличение глубины потенциальной ямы ведет к уменьшению коэффициента
теплового расширения a
Т
. Значит, вещества с большей температурой
плавления, как правило, имеют меньший коэффициент термического
расширения.
Эту взаимосвязь иллюстрирует таблица 2., где приведены теплота
Таблица 2.
Металл K Zn Cu Fe W Mg
Q , ккал/моль 21,5 31,2 81 99,5 200 36
Т
плав
, К 336 792 1357 1809 3650 650
Е , ГПа 0,001 80 125 216 415 45
a, 10
-6
1/К 16 12 4,4 26
, г/см
3
8,9 7,8 19,3 1,7
9

испарения Q, температура плавления Т
плав
, модуль упругости Е , .коэффициент
теплового расширения a , плотность некоторых металлов.
При воздействии на тело силовых полей (электрического, механического,
магнитного) частицы тела смещаются из равновесных положений. При этом
могут реализовываться три случая.
1. Под действие поля частицы не переходят через потенциальные
барьеры. При исчезновении поля частицы возвращаются в исходные
положения. В этом случае мы имеем дело с упругими процессами: упругой
деформацией, упругой поляризацией и так далее. Чем "круче" стенки
потенциальной ямы, тем труднее осуществляется упругий процесс.
2. Под действием поля некоторые слабо связанные частицы
перебрасываются из одного положения в другое. После снятия внешнего
воздействия под влиянием теплового движения или внутренних напряжений
устанавливается состояние, статистически эквивалентное исходному. Этот
случай реализуется при близости величины некоторых потенциальных
барьеров со средней энергией частиц. Такие процессы называются
гистерезисными (типичный пример - "неупругость" пружин, гистерезис
намагничивания) и характеризуются замкнутыми кривыми, называемыми
циклами гистерезиса.
3. Если внешнее поле перемещает частицы через потенциальные барьеры,
достаточно высокие по сравнению с тепловой энергией материала, то при
снятии внешнего воздействия частицы в исходные положения не
возвращаются, появляется остаточный эффект (пластическая деформация
металлов, получение постоянных магнитов, электретов и т.д.).
Хотя точный вид кривой взаимодействия зависит от конкретных свойств
взаимодействующих частиц и от направления, в котором она исследуется,
однако в общих чертах ее вид определяется типом и энергией химической
связи.
2. Типы химических связей.
Основными типами химической связи являются: ковалентная, ионная,
металлическая и поляризационная связь (или связь Ван-дер-Ваальса).
Ковалентная связь. Ковалентная связь образуется между атомами
одного или нескольких химических элементов с близкими ионизационными
потенциалами. В чистом виде ковалентная связь реализуется при
взаимодействии элементов с наполовину заполненными электронными
оболочками. Из квантовой химии следует, что система из положительно
заряженного ядра и отрицательно заряженных электронных оболочек имеет
минимальную энергию в том случае, когда электронные оболочки заполнены
полностью. Для этого внешняя оболочка атома должна содержать восемь
электронов. Поэтому атомы с почти заполненной оболочкой стремятся
присоединить недостающие электроны, а атомы имеющие один - два электрона
на внешней оболочке – отдать лишние электроны. Атомы имеющие наполовину
заполненные электронные оболочки обмениваются электронами. При этом
10
