Маркин А.Н., Низамов Р.Э., Суховерхов С.В. Нефтепромысловая химия: практическое руководство
Подождите немного. Документ загружается.


глава 2
_______________________________________________________________________________________
70
внутреннего диаметра НКт в результате отложения солей и, как следствие, сниже-
ние количества жидкости, добываемого скважинами; выход из строя глубинных на-
сосов при механизированном способе добычи; выход из строя измерительного обо-
рудования; снижение эффективности работы сепараторов-подогревателей (heater-
treater); интенсивная коррозия внутренней поверхности НКт, трубопроводов ссН
и систем ППд в местах локального отслаивания отложений и под отложениями.
На рис. 2.4, 2.5 показаны примеры солеотложений из нефтепромысловых систем.
так же как АсПо никогда не состоят на 100 % из парафинов, солеотложения
никогда не являются 100 %-ной соответствующей солью. Постоянными компо-
нентами минеральных отложений являются соединения железа (оксиды, карбо-
наты) и не растворимые в концентрированных кислотах вещества (механические
примеси) – песок или глина. в табл. 2.3 приведены составы солеотложений не-
которых месторождений. часто соль, являющаяся основой осадка (в том смысле,
что если бы вода не выделяла эту соль, то минеральные отложения не образова-
лись бы в данном месте нефтепромысловой системы), не является его наиболь-
шей массовой составляющей.
таблица 2.3. Составы солеотложений некоторых нефтяных месторождений
месторождение
состав отложений, % масс.
CaCO
3
CaSO
4
BaSO
4
соединения
железа
механические
примеси
другое
самотлорское, добывающая скважина 78,1 – – 4,5 16,3 1,1
самотлорское, добывающая скважина 48,5 – – 47,3 4,2 –
мишовдаг, трубопровод (рис. 2.5) 35,6 – – 41,3 9,8 13,3
Когалымское, добывающая скважина 25,7 4,8 43,7 12,2 6,1 7,5
Когалымское, добывающая скважина 2,3 – 88,5 1,1 8,1 –
Присутствие в составе солеотложений механических примесей (в том числе
оксидов железа) объясняется тем, что они являются центрами кристаллизации:
кристаллы соли начинают расти на них, и при образовании минеральных отложе-
ний макроразмеров механические примеси оказываются включенными в состав
осадков.
Знание химического состава минеральных отложений важно как для понима-
ния механизма их образования, так и для правильного выбора методов предотвра-
щения солеотложения.
такие методы анализа, как рентгено-флуоресцентный и рентгеновская дифрак-
ция, позволяют быстро определить элементный состав солеотложений и полуко-
личественный фазовый состав. тем не менее основным методом определения со-
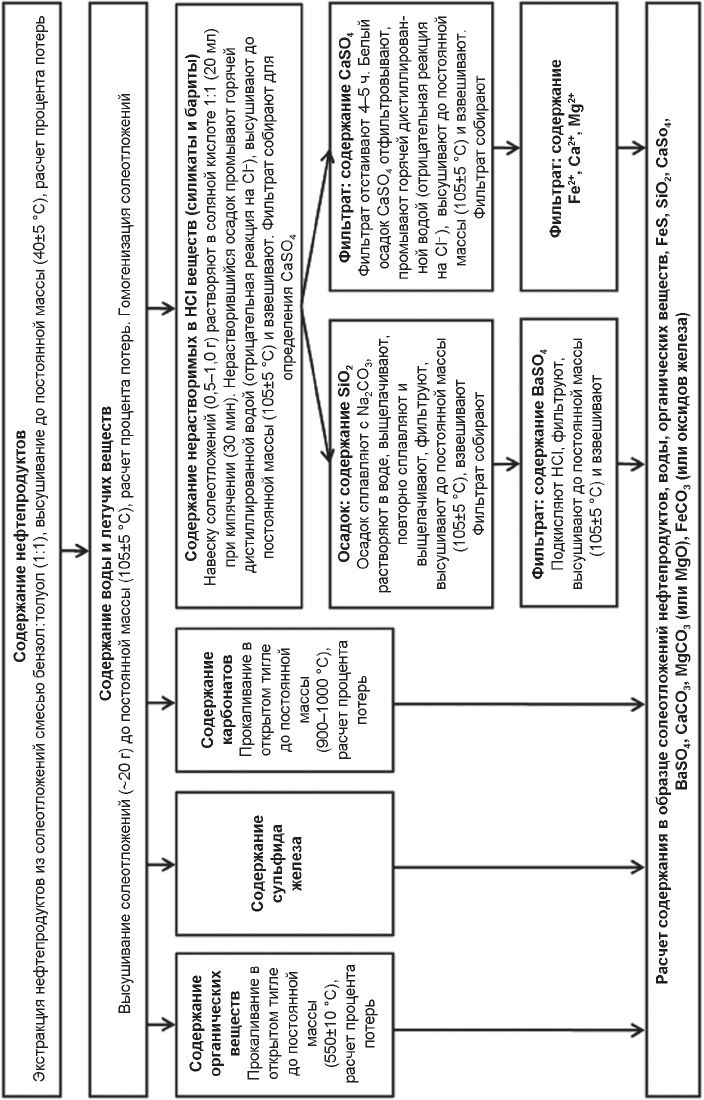
става солеотложений является химический метод [10, 11]. На рис. 2.6 приведена
схема систематического количественного анализа солеотложений
16
. схема анализа
16
см. также гост 26449.4–85 «Установки дистилляционные опреснительные стационарные. методы хи-
мического анализа накипи и шламов».

71
__________________________________________________________________________________________
соли
рис. 2.4. минеральные отложения в трубопроводе ∅ 159 × 8 мм подтоварной воды от сепаратора-
подогревателя. одно из месторождений Кумкольской группы, Казахстан, 2002 г.
рис. 2.5. внутренняя поверхность трубопровода ∅ 254 × 10 мм системы ППд полностью покрыта
минеральными отложениями. интенсивная локальная коррозия под отложениями. месторождение
мишовдаг, Азербайджан, 2006 г.
глава 2
_______________________________________________________________________________________
72
рис. 2.6. схема систематического количественного анализа солеотложений
73
__________________________________________________________________________________________
соли
составлена на основе предположения о том, что основными компонентами соле-
отложений являются CaCO
3
, FeCO
3
, CaSO
4
, BaSO
4
, FeS и механические примеси,
представленные окисью кремния (песок). После проведения анализов по схеме
рис. 2.6 можно с достаточной для практических целей точностью рассчитать со-
держание указанных веществ в образце солеотложений. Коротко остановимся на
тех анализах, которые недостаточно описаны на рис. 2.6.
определение сульфида железа. в мерную колбу на 100 мл переносят ~0,1 г
солеотложений, добавляют 30 мл 0,05 н раствора йода и выдерживают 20 мин. За-
тем добавляют 10 мл Нсl (1 : 1), доводят до метки дистиллированной водой и по-
мещают на 30 мин в темное место. титруют 0,1 н раствором тиосульфата натрия,
добавляя в конце титрования несколько капель раствора крахмала.
определение окиси кремния (песка). Нерастворимый в HCl остаток смеши-
вают с пятикратным количеством Na
2
CO
3
, заворачивают в папиросную бумагу,
помещают в фарфоровый тигель, на дно которого положена вчетверо сложенная
фильтровальная бумага, смоченная водой (для предупреждения действия соды на
тигель), сплавляют 15–20 мин при 450–500 °с и охлаждают. Полученный спек
переводят в стакан, добавляют 1 г Nа
2
со
3
, разбавляют раствор до 100 мл дис-
тиллированной водой и кипятят 10 мин. отфильтровывают углекислые соли че-
рез бумажный фильтр, промывают 1 %-ным раствором Na
2
CO
3
. Фильтр с осадком
высушивают, озоляют в том же тигле, слабо прокаливают, смешивают с содой,
повторно сплавляют и выщелачевают водой. отфильтровывают углекислые соли
через бумажный фильтр, предварительно высушенный до постоянной массы, про-
мывают 1 %-ным раствором Nа
2
сO
3
. осадок с фильтром высушивают при 105 °с
до постоянной массы и после охлаждения в эксикаторе взвешивают.
определение Fe
2+
, Ca
2+
и Mg
2+
из раствора. Подходят любые широко рас-
пространенные методы, в том числе наборы для экспресс-анализов (HACH,
CHEMetric и др.): Fe
2+
– метод с сульфосалициловой кислотой [10] или с 1,10-фе-
нантролином, Ca
2+
и Mg
2+
– трилонометрический метод с мурексидом и эриохро-
мом черным т [10] или с калмагитом.
в заключение следует упомянуть, что солеотложения могут обладать есте-
ственной радиоактивностью. Несмотря на то что существуют природные радио-
активные изотопы кальция, магния, бария и стронция, естественная радиоактив-
ность солеотложений связана, главным образом, с радием (
226
Ra и
228
Ra). изотопы
радия соосаждаются с сульфатами, чаще всего с сульфатом бария. мощность дозы
радиоактивных солеотложений может достигать 15000 мкр/ч (дозиметр располо-
жен вплотную к солеотложениям), средние значения 50–1000 мкр/ч.
2.3. ПРОгНОзИРОВАНИЕ ОбРАзОВАНИЯ СОЛЕОТЛОжЕНИй
для прогнозирования выпадения в осадок малорастворимой соли пользу-
ются величиной пересыщения раствора этой солью. величина пересыщения

глава 2
_______________________________________________________________________________________
74
раствора (П) малорастворимой солью Kt
m
An
n
, диссоциирующей в растворе по
реакции
Kt
m
An
n
↔ mKt + nAn, (2.15)
равна
[ ] [ ]
m n
m n
K An
Kt An
П ,
Пр
t
a a⋅
=
(2.16)
где a
Kt
– активность катиона, a
An
– активность аниона, Пр
Kt
m
An
n
– произведение рас-
творимости соли. если П < 1, то раствор не насыщен рассматриваемой солью, при
П = 1 имеем насыщенный, а при П > 1 – пересыщенный раствор соли. в послед-
нем случае возможно выделение осадка малорастворимой соли. На практике чаще
используют не величину пересыщения раствора П, а еe десятичный логарифм,
который называется индексом насыщения раствора и обозначается SI
17
:
[ ] [ ]
m n
m n
Kt An
Kt An
SI lg .
Пр
a a⋅
=
(2.17)
При SI ≤ 0 раствор не выделяет осадок малорастворимой соли, при SI > 0
осадкообразование возможно.
прогнозирование образования карбоната кальция. Карбонат кальция, CaCO
3
,
образуется в результате реакций:
2
3 3 2 2
Ca 2(HCO ) CaCO CO H O,
+ −
+ → ↓ + ↑ +
(2.18)
2 2
3 3
Ca CO CaCO .
+ −
+ → ↓
(2.19)
известны три формы CaCO
3
– кальцит, арагонит и ватерит. Кальцит наибо-
лее распространен в нефтепромысловых системах, и далее под CaCO
3
мы будем
иметь в виду именно кальцит. в водных фазах нефтепромыслов, где концентрация
карбонат иона близка к 0, образование сасо
3
идет в основном по реакции (2.18).
одним из продуктов этой реакции является углекислота, поэтому осаждение
сасо
3
зависит от р
со
2
: с увеличением парциального давления со
2
реакция (2.18)
смещается влево. Этот эффект в несколько раз повышает растворимость сасо
3
в
пресной и слабоминерализованной воде при изменении р
со
2
от 0 до 1 мПа. Повы-
шение температуры и pH сдвигают реакцию (2.18) вправо, в сторону образования
сасо
3
. в 1936 г. ланжелье [3] предложил эмпирическое уравнение для определе-
ния индекса насыщения воды карбонатом кальция:
3
' ' 2
CaCO S 2 S
SI pH pH pH ( K K [Ca ] [Alk]),p p p p
−
= − = − − + +
(2.20)
где pH – фактическое значение водородного показателя раствора, pH
S
– значение
водородного показателя данного раствора, находящегося в равновесии с твер-
17
Аббревиатура английских слов Saturation Index (индекс насыщения).

75
__________________________________________________________________________________________
соли
дым CaCO
3
при данных концентрациях Ca
2+
, Нсо
3
–
и остальных веществ, pK
2
'
и
pK
S
'
–эмпирические константы, p[Ca
2+
] = –lg[Ca
2+
]
18
, [Alk] – общая щелочность,
выраженная в моль/л CaCO
3
. При SI
CaCO
3
> 0 CaCO
3
может выпасть в осадок, при
SI
CaCO
3
≤ 0 раствор не выделяет CaCO
3
. Значения эмпирических констант формулы
(2.20) для ионной силы раствора 0–0,02 моль/л и температуры 0–90 °с приведены
в [3], а также в большинстве изданий, где рассматривают карбонатное равнове-
сие растворов. в дальнейшем были предложены другие индексы, позволяющие
прогнозировать образование CaCO
3
в различных «специальных» системах: индекс
ризнера
19
[12] для пресной воды; индекс стиффа–дэйвиса [13], расширяющий ин-
декс ланжелье на нефтепромысловые системы; индекс оддо–томсона [14] для
воды под давлением газовой фазы. тем не менее индекс ланжелье – SI
CaCO
3
– ши-
роко и успешно применяют и в настоящее время:
3
CaCO S
SI pH pH ,= −
(2.21)
причем рН
S
может быть найден по формуле [15]:
рН
S
= pK
2
– pПр
CaCO
3
+ pa
Ca
2+
+ pa
HCO
3
–
,
(2.22)
где K
2
– константа диссоциации угольной кислоты по второй ступени, Пр
CaCO
3
–
произведение растворимости CaCO
3
; значения K
2
, Пр
CaCO
3
, а также активности ио-
нов должны отвечать температуре раствора (температурные зависимости констант
химического равновесия, встречающихся в этой книге, приведены в прил. 2).
в качестве примера рассчитаем возможность выпадения карбоната кальция
в фонтанной арматуре (на устье) и в трубопроводе от скважины 401 до группо-
вой замерной установки одного из нефтяных месторож дений Нижневартовского
района.
П р и м е р 3. химический состав водной фазы продукции скважины при-
веден в табл. 2.4.
таблица 2.4. Химический состав водной фазы скважины 401
вещество
Концентрация
мг/л моль/л
Cl
–
19219 0,5419
Na
+
9772 0,4251
Ca
2+
1812 0,0452
Mg
2+
413 0,0170
HCO
3
–
422 0,0069
CO
3
2–
0,17 2,9∙10
–6
SO
4
2–
1,2 1,2∙10
–5
pH (измерена в условиях, исключающих дегазацию пробы) 6,71
температура 30 °с
18
Здесь и далее знак p означает отрицательный десятичный логарифм величины, стоящей под этим зна-
ком.
19
SI
CaCO
3
= 2∙pH
S
– pH.
глава 2
_______________________________________________________________________________________
76
1. По формуле (2.10) рассчитываем ионную силу раствора, пренебрегая вкла-
дом CO
3
2–
, SO
4
2–
и H
+
:
I = ½∙ [0,5419 + 0,4251 + 0,0069 + 4(0,0452 + 0,0170)] = 0,6114 (моль/л).
2. вычисляем коэффициенты активности и активности ионов Ca
2+
, Нсо
3
–
(формула (2.12а), прил. 1), а также
2
Ca
pa
+
и
3
HCO
pa
−
:
2
Ca
f
+
= 0,5522,
2
Ca
a
+
= 0,0250,
3
HCO
f
−
= 0,8620,
3
HCO
a
−
= 0,0060,
2
Ca
pa
+
= 1,6021,
3
HCO
pa
−
= 2,2218.
3. рассчитываем pK
2
и pПр
CaCO
3
при 30 °с по формулам прил. 2:
pK
2
= 10,2855, pПр
CaCO
3
= 8,5249.
4. Находим pH
S
по формуле (2.22) и SI
CaCO
3
по формуле (2.21):
pH
S
= 10,2855 – 8,5249 + 1,6021 + 2,2218 ≈ 5,59,
SI
CaCO
3
= 6,71 – 5,59 = 1,12.
так как индекс ланжелье > 0, то образование карбоната кальция возмож-
но. водная фаза продукции этой скважины действительно интенсивно выделяет
карбонат кальция, который откладывается в трубопроводах и запорной арматуре
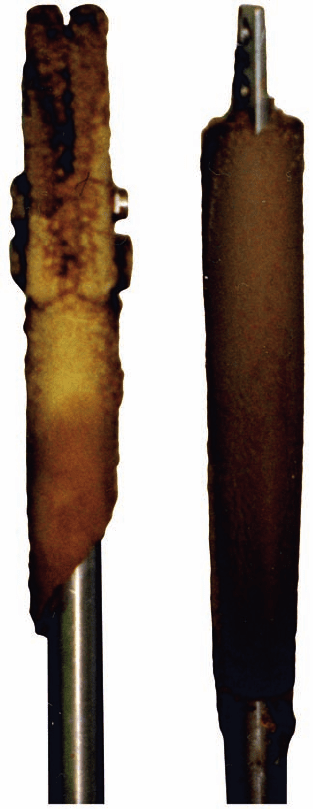
групповой замерной установки, а также в трубопроводах ссН. На рис. 2.7 при-
ведена фотография держателя образцов контроля скорости коррозии весовым ме-
тодом, экспонировавшегося 3 мес. в трубопроводе от скважины 401 до групповой
замерной установки.
Нарушение химического равновесия, приводящее к образованию минераль-
ных отложений, основным компонентом которых является карбонат кальция, про-
исходит в результате изменения р
со
2
, химического состава воды или температуры.
с увеличением температуры произведение растворимости CaCO
3
понижа-
ется (см. прил. 2), следовательно, SI
CaCO
3
увеличивается (формула (2.17)), т.е. по-
вышение температуры способствует образованию CaCO
3
(факт, сегодня, после
рекламы «Калгон», известный каждой домохозяйке). При добыче нефти темпера-
тура жидкости понижается от забоя к устьям скважин и по длине трубопроводов
от скважин к насосным станциям. Поэтому при «обычном» технологическом про-
цессе добычи нефти образования отложений карбоната кальция из-за изменения
температуры не происходит. если же технологический процесс предусматривает
нагрев продукции добывающих скважин, то необходимо оценить возможность
образования CaCO
3
при максимальной температуре и при положительном прогно-
зе либо снизить температуру, либо принять меры для предотвращения образова-
ния солеотложений. Это, в частности, относится к сепараторам-подогревателям.
температура поверхности жаровых труб сепараторов-подогревателей может до-
стигать 300 °с. Поэтому, даже если солеотложения никогда не наблюдались в до-
бывающих скважинах и трубопроводах данного месторождения, следует быть го-
77
__________________________________________________________________________________________
соли
товым к тому, что без принятия мер для пре-
дотвращения солеотложений минеральные
отложения будут интенсивно образовываться
на жаровых трубах и в трубопроводе под-
товарной воды от сепаратора-подогревателя
(см. рис. 2.4). иногда повышение темпера-
туры, приводящее к образованию солеотло-
жений, происходит вследствие нарушения
технологического процесса. характерный
пример – неправильный выбор типоразмера
УЭЦН при механизированной добыче нефти.
скважина была оборудована УЭЦН с номи-
нальным дебитом 80 м
3
/сут, фактический де-
бит скважины составлял от 90 до 100 м
3
/сут,
т.е. превышал номинальный дебит УЭЦН.
При оптимизации добычи нефти посчитали,
что, вероятно, данная скважина может давать
больше жидкости (и нефти), и в скважину
спустили УЭЦН с номинальным дебитом
140 м
3
/сут. добыча жидкости возросла до
120 м
3
/сут, но через 28 сут произошел отказ
УЭЦН. После извлечения УЭЦН установили
причину отказа – перегрев двигателя в резуль-
тате отложения карбоната кальция в насосе и
на корпусе двигателя. до данного случая за
предыдущие 8 лет эксплуатации солеотложе-
ний в этой скважине не наблюдали, а хими-
ческий состав водной фазы практически не
изменился. объяснение очевидно. Как извест-
но, УЭЦН охлаждается потоком жидкости.
Притока жидкости из пласта не хватало для
охлаждения УЭЦН с номинальным дебитом
140 м
3
/сут, и температура двигателя и установ-
ки повысилась до значений, при которых ста-
ло возможно образование карбоната кальция.
изменение химического состава воды
также может приводить к образованию
CaCO
3
. существенное изменение химическо-
го состава происходит при смешивании вод разных месторождений. Классический
случай: в воде одного месторождения высокая концентрация Ca
2+
, а в воде другого
высокая концентрация HCO
3
–
. При смешивании этих вод происходит интенсивное
выделение CaCO
3
. смешивание разных вод, одни из которых содержали 1000–
рис. 2.7. осадок карбоната кальция,
образовавшийся на держателе и
образцах контроля скорости коррозии
весовым методом, экспонировавшихся
в трубопроводе от скважины 401
до групповой замерной установки
(г. Нижневартовск, 1995 г.)

глава 2
_______________________________________________________________________________________
78
4000 мг/л Ca
2+
, а другие –500–1800 мг/л HCO
3
–
, привело к тому, что внутренняя по-
верхность трубопровода системы ППд месторождения мишовдаг полностью по-
крылась минеральными отложениями, основным солеобразующим компонентом
которых являлся карбонат кальция (рис. 2.5). Классическая ситуация встречается
редко, обычно смешиваемые воды близки по химическому составу. тем не менее
оценивать возможность образования CaCO
3
необходимо каждый раз, когда пред-
стоит смешивание вод, так как даже если воду, имеющую отрицательный индекс
ланжелье, но содержащую ионы Ca
2+
и HCO
3
–
, смешивают с водой, не содержа-
щей этих ионов, то полученный раствор может иметь SI
CaCO
3
> 0, если вторая вода
является высокоминерализованной (проявляется влияние ионной силы раствора).
На рис. 2.8 показано изменение индекса ланжелье при разбавлении (1 : 1) подто-
варной воды (Ca
2+
= 205 мг/л; HCO
3
–
= 606 мг/л; Cl
–
= 13930 мг/л; р
со
2
= 7,09 кПа)
раствором NaCl (м = 142 г/л), не содержащим ионов кальция и HCO
3
–
. Как видно
из данных рис. 2.8, при температуре 10 °с исходная вода имеет отрицательный
индекс ланжелье, а разбавленная – положительный. частный случай изменения
химического состава воды – повышение рН за счет уменьшения р
со
2
. общее дав-
ление, а следовательно, и р
со
2
понижаются от забоя к устьям скважин и по длине
трубопроводов от скважин к насосным станциям, поэтому вероятность образо-
вания отложений карбоната кальция из-за уменьшения р
со
2
возрастает от забоя к
устьям скважин и по длине трубопроводов. одновременное уменьшение t и р
со
2
противоположно влияют на образование сасо
3
: расчет SI
CaCO
3
следует проводить
рис. 2.8. изменение индекса ланжелье при разбавлении (1 : 1) подтоварной воды (Ca
2+
= 205 мг/л;
HCO
3
–
= 606 мг/л; Cl
–
= 13930 мг/л; р
со
2
= 7,09 кПа) раствором NaCl (м = 142 г/л)
79
__________________________________________________________________________________________
соли
для каждой точки промысловой системы, где происходит существенное измене-
ние t или р
со
2
.
прогнозирование образования карбоната железа. Карбонат железа (FeCO
3
–
сидерит) является вторым часто встречающимся компонентом минеральных от-
ложений в нефтепромысловых системах с углекислым газом [8, 16–18]. он об-
разуется в результате реакций:
2
3 3 2 2
Fe 2(HCO ) FeCO CO H O,
+ −
+ → ↓ + ↑ +
(2.23)
2 2
3 3
Fe CO FeCO .
+ −
+ → ↓
(2.24)
Фоновые концентрации ионов железа в водных фазах нефтепромыслов, как
правило, менее 1 мг/л. Превышение этого уровня до значений 5–15 мг/л и бо-
лее (70–80 мг/л) происходит в результате коррозии промыслового оборудования.
в нефтепромысловых системах из-за незначительных концентраций CO
3
2–
образо-
вание FeCO
3
в объеме раствора идет по реакции (2.23), при условии что pH близко
к 8. чаще, однако, pH в объеме раствора значительно ниже 8, и реакция (2.23)
протекает в тонком водном слое у поверхности металла (приэлектродный слой),
обогащенном в результате коррозии ионами железа и подщелоченном из-за ги-
дролиза Fe(HCO
3
)
2
. в этом случае на поверхности стали образуется плотный, не-
проницаемый осадок FeCO
3
, обладающий хорошей адгезией и защитными свой-
ствами [17–19]. возможен и иной механизм осадкообразования – по реакциям,
протекающим в адсорбированном состоянии на поверхности стали (pH < 8) [20]:
2
2 2 3 2
Fe nH O CO Fe(HCO ) 2H ,
+ +
+ + → +
(2.35)
2
2 2 3
2Fe nH O CO 2FeO FeCO 4H .
+ +
+ + → ⋅ ↓ +
(2.26)
ионы водорода, высвобождающиеся по реакциям (2.25) и (2.26), расходуются
на деполяризацию коррозионного процесса, гидрокарбонат железа, растворяясь,
попадает в приэлектродный слой, а на поверхности стали образуется труднора-
створимое соединение предполагаемого состава FeO∙FeCO
3
, названное авторами
[19] коррозитом. По [19] коррозит представляет собой легкопроницаемое рых-
лое вещество черного цвета, отличающееся от известных окислов железа. в [16]
было установлено, что в оксидном слое образцов углеродистой стали, коррози-
ровавших в трубопроводах ссН и в синтетической пластовой воде самотлорско-
го и других месторождений Нижневартовского района, присутствуют цементит
(Fe
3
C), сидерит и третья фаза, имеющая кубическую (типа шпинели) структуру,
изоморфную структуре сидерита. Эта фаза, возможно, является суперпозицией
структур вюстита (FeO), магхемита (a-Fe
2
O
3
) и магнетита (FeO∙Fe
2
O
3
), которые
имеют кубическую структуру. Поскольку третья фаза всегда присутствует вместе
с FeCO
3
и не полностью растворившимся Fe
3
C матрицы, но не обнаружена от-
дельно ни в одном из исследованных образцов, представляется более правильным
называть коррозитом не ее, а гетерофазную структуру, состоящую из трех указан-
