Лекции по минералогии
Подождите немного. Документ загружается.

AsS
3
-3
) анионы. В зависимости от характера аниона собственно сульфиды делятся на три
подкласса:
1-й подкласс. Низшие сульфиды (моносульфиды).
2-й подкласс. Высшие сульфиды (персульфиды).
3-й подкласс. Сульфосоли.
Катионы дают с серой:
1) Простые соединения - PbS, галенит; ZnS, сфалерит.
2) Упорядоченные двойные соединения - CuFeS
2
, халькопирит.
3) Более сложные (тройные и более) соединения: Cu
2
FeSnS
4
, станнин.
4) Нестехиометричные (дефектные) соединения: Cu
2-x
S - дигенит, Cu
+1
8
Cu
+2
S
5
(9 катионов,
а не 10 на 5S
-2
); Fe
1-x
S - пирротин.
Особо обратим внимание на положение As
+3
, Sb
+3
, Bi
+3
- в сульфидах они выступают
именно в таком, неполновалентном (полная валентность группы - +5) виде как катионы, и
образуют молекулярные кристаллы - реальгар, аурипигмент, антимонит, висмутин. Для
сравнения отметим, что в классе арсенидов и сульфоарсенидов они проявляют себя как
анионы: входят в полианионные гантельные группы, напр., [AsS]
-3
.
Структурные особенности сульфидов. Для сульфидов характерны все три надотдела
соединений: нормальные, кластерные и молекулярные. Большинство нормальных и
кластерных сульфидов обладают структурой по типу ПУ и относятся к отделу
координационных. Какие тут возможны особенности? В соединениях с Cu, Ag возможно
расположение катионов в плоскости слоев ПУ или между ними - соответственно КЧ таких
катионов понижается до 2, 3. Это характерно для низкотемпературных модификаций.
Соответственно, симметрия таких соединений понижается по сравнению с
координационными, в которые они переходят (или становятся близкими) при повышении
температуры. Из этого следует, что для сульфидов широко будут проявляться полиморфные
превращения.
Можно выделить три типа полиморфных переходов.
1) Тип ПУ анионов не изменяется, а происходит лишь перераспределение
(упорядочивание) катионов по структурным позициям. Такие переходы связаны с
изменением температуры и характерны для сложных (несколько катионов!) сульфидов.
Пример: Халькопирит. При высокой температуре он кубический, со структурой
сфалерита (алмаза), где Cu и Fe заполняют тетраэдрические пустоты неупорядоченно. Это
можно выразить формулой (Cu,Fe)S. При понижении температуры за счет того, что катионы
занимают строго упорядоченное положение (чередование слоев пустот, заполненных Cu, и
слоев с Fe), параметр c удваивается и симметрия снижается до тетрагональной, а формула
халькопирита приобретает более привычный вид: CuFeS
2
.
2) Изменяется тип ПУ анионов из-за перераспределения связей. Например, кубический
сфалерит переходит в гексагональный вюртцит.
3) Катионы с переменной валентностью часто дают структуры дефектные - при
замещении нескольких низковалентных катионов меньшим числом более высоковалентных
- это разбиралось уже, когда речь шла о кластерных соединениях - пирротине, дигените, с
общей схемой замещения 3Ме
+2
- 2Ме
+3
, или 2Ме
+1
- Ме
+2
; так вот, если вакансии при таких
замещениях распределяются неупорядоченно, то симметрия остается равной симметрии
стехиометричного аналога, если же вакансии упорядочены - симметрия понижается: FeS
Fe
1-x
S Fe
7
S
8
(стехиометричный гексагональный троилит переходит в гексапирротин - с
неупорядоченными вакансиями, а затем в клинопирротин - вакансии упорядочены.
До сих пор речь шла о нормальных и кластерных сульфидах; молекулярные сульфиды
характеризуются более сложными структурами, все зависит от мотива, по которому
построены "молекулы" - и потому различают островные (реальгар As
4
S
4
), цепочечные
(киноварь HgS), ленточные (висмутин Bi
2
S
3
), слоистые (молибденит MoS
2
) структуры и
соответственно - отделы в систематике.
31

Морфология. Для сульфидов с координационной структурой характерен изометричный
облик кристаллов, кубическая и гексагональная сингонии. Для молекулярных минералов
особенности структуры определяют и облик кристаллов - удлиненный до игольчатого у
минералов с цепочечным или ленточным строением и уплощенный, таблитчатый - у
минералов со слоистой структурой.
Свойства. Характер структуры напрямую проявляется в таких свойствах, как спайность.
В молекулярных минералах спайность будет проходить по направлениям слабых,
межмолекулярных связей -параллельно слоям, лентам, цепочкам. В нормальных и
кластерных сульфидах спайность определяется и структурой, и химизмом, т.е. зависит от
состава плоских сеток решетки и расстояния между ними. Т.к. эти сульфиды
координационные, и для них характерна высокая симметрия, то обычно спайность в них
проявляется по нескольким направлениям, напр., по {100} у галенита, по {110} у сфалерита.
В минералах с полианионной структурой, где связь распределяется более равномерно,
спайность обычно отсутствует - мы это знаем на примере пирита: гантель [S
2
]
-2
обеспечивает
большую равномерность и большую прочность связей катион-анион.
Плотность - прямо пропорциональна отношению Ме:S, т.к. большинство сульфидов -
структуры координационные, т.е. ПУ или близкие к ним, значит, степень заполнения пустот
в ПУ и будет определять плотность. При этом в однотипных структурах плотность прямо
пропорциональна атомным весам катионов, напр., Sb
2
S
3
- d=4,6, Bi
2
S
3
- d=6,8.
Цвет, блеск и пр. свойства. Цвет и блеск сульфидов определяются характером связи (а
это преимущественно ковалентная связь с металлической компонентой) и составом:
суммарным Z (атомным номером) слагающих частиц, главным образом катионов. Каким
образом проявляется эта зависимость? По характеру связи - это соединения-
полупроводники. Это значит, что зона, в которой отсутствует проводимость, у них невелика,
и в ней есть свободные электроны. А наличие свободных электронов обусловливает
металлический блеск, да если еще есть взаимодействие Ме-Ме (кластерные соединения), то
этот металлический блеск усиливается, кроме того следует помнить, что металличность
катионов нарастает в ряду As-Sb-Bi. Все это и приводит к тому, что у большинства
сульфидов блеск металлический. При этом могут возникать цветные оттенки: розоватый,
желтоватый, до латунно-желтого и медно-красного. Это касалось сульфидов непрозрачных,
но среди сульфидов имеются прозрачные или полупрозрачные - для них характерен блеск
алмазный или полуметаллический. Это разнообразие издавна фиксировалось в минералогии
делением сульфидов на колчеданы - минералы с металлическим блеском, с цветными
оттенками (бронзово-желтый пирротин - магнитный колчедан, латунно-желтый пирит -
железный или серный колчедан), блески - сстально-серые сульфиды с металлическим
блеском (свинцовый блеск, сурьмяный блеск, висмутовый блеск вместо привычных нам
галенита, антимонита, висмутина) и обманки - сульфиды с неметаллическим блеском:
цинковая обманка, кадмиевая обманка. Цвет сульфидов с алмазным блеском определяется
спектром поглощения, а он зависит от химизма - атомного номера слагающих элементов,
точнее, их суммарным атомным номером (Z). Напр., клейофан Z=46 - желтый,
пираргирит Z=96 - темнокрасный). И, конечно, существенную роль в окраске играют
изоморфные примеси, которые вносят свой вклад в энергетическое взаимодействие катионов
и анионов в структуре.
Твердость - свойство, сильно зависящее от степени прочности связей в решетке, т.е. от
структуры. Здесь применимы те же рассуждения, что и относительно спайности: твердость
моноанионных сульфидов ниже, чем у аналогичных по составу полианионных (пирротин -
3,5, пирит - 5,5-6); молекулярные сульфиды - как правило, с низкой твердостью, как и
сульфосоли.
Генезис. Большинство сульфидов - гипогенного образования, и лишь немногие из них
могут образовываться в гипергенных условиях - акантит, борнит, халькозин, гринокит.
Для гипогенных это будут следующие генетические типы:
32
1. Магматический (ликвационно-магматический) - Cu-Ni м-ния типа Норильска, Седбери;
образование связано с основными-ультраосновными интрузиями - пирротин, пентландит,
халькопирит.
2. Гидротермальный генезис характерен для большинства сульфидов.
а) Гидротермальная минерализация в скарнах, (молибденит, полиметаллическая
ассоциация).
б) Гидротермальная жильная (как высокотемпературная - молибденит, висмутин, так и
среднетемпературная - полиметаллические месторождения, и низкотемпературная -
киноварь, антимонит, реальгар, аурипигмент).
3. Колчеданные месторождения. Это полигенный тип - в его образовании принимают
участие разные процессы: сначала - вулканогенно-осадочный, а затем - гидротермальная
метасоматическая проработка. Как показывает название, главые минералы здесь колчеданы -
пирит, марказит, пирротин - и медные сульфиды.
В гипергенном образовании сульфидов можно выделить следующие типы:
1. Зоны окисления, где при разложении и окислении сложных сульфидов образуется ряд
более простых (акантит по серебросодержащим минералам; халькозин, ковеллин по
медьсодержащим), или они заново возникают в подзоне цементации (вторичного
сульфидного обогащения) - те же халькозин, ковеллин.
2. Медистые песчанники - особый тип, по-видимому, также полигенный - сульфиды здесь
могут возникать как сингенетичные осадконакоплению минералы за счет взаимодействия
сероводорода, образующегося при разложении органических остатков, и сносимых в
морской бассейн металлов, так и при последующем просачивании (инфильтрации)
поверхностных или очень низкотемпературных гидротермальных растворов, отлагающих
растворенные в них вещества.
Изменение. На поверхности сульфиды неустойчивы, окисляются и дают начало
сульфатам, карбонатам и большому числу оксидов и гидроксидов.
Систематическое рассмотрение сульфидов мы начнем с низших сульфидов.
Подкласс 2.1а. Низшие сульфиды.
Систематика - табл....
Семейство халькозина (Chsn)
В этом семействе объединяют несколько полиморфных модификаций с общей формулой,
близкой к Cu
2
S.
Химизм. Примесь Ag, твердые растворы с борнитом.
Структура. Среди модификаций семейства выделим главные в структурном отношении:
1. Моноклинный халькозин (клинохалькозин) -Cu
2
S, устойчивый до ~103°С -
низкотемпературный халькозин.
2. Выше по T (103-420°С) устойчив гексахалькозин.
3. Еще выше - высоко-T кубический халькозин (кубохалькозин), который близок к
модификации, называемой -дигенит, Cu
2-x
S. В таком порядке рассмотрим и особенности
структуры.
Моноклинный халькозин имеет структуру типа акантита: S образует ПГУ, 1/2Cu
+1
- в
плоскости слоя ПГУ с КЧ=2+1, вторая половина Cu
+1
- между слоями упаковки, с КЧ=2,
образуя с S зигзагообразные цепочки.
В гексахалькозине симметрия структуры повышается за счет того, что Cu
+1
, находящаяся
в плоскости ПГУ, приобретает КЧ=3, т.е. смещается в центр треугольников, а вторая
половина Cu
+1
, расположенной между слоями упаковки, занимает место в тетраэдрических
пустотах. (Сколько пустот занято? 1/2).
Кубохалькозин » -дигенит. S
-2
образует ПКУ, все октаэдрические позиции которой
свободны, а все тетраэдрические заняты Cu
+1
. При этом тетраэдры имеют общие ребра:
33

каждое ребро принадлежит двум тетраэдрам - получается восьмерик, но восьмерики не
изолированные, а заполняют структуру сплошь! При этом ионы Cu
+1
, находящиеся в
тетраэдрах, оказываются сближенными, и это вызывает взаимодействие Ме-Ме. Это
означает, что образуется кластер. Взаимодействие Ме-Ме усугубляется еще тем, что
происходит замещение 2Cu
+1
- Cu
+2
, т.е. структура оказывается дефектной с дефицитом
меди: Cu
2-x
S против идеальной формулы Cu
2
S. Сколько этих "х"? Обычно на каждые 10
тетраэдров приходится 8Cu
+1
+1Cu
+2
, т.е. Cu
+1
8
Cu
+2
S
5
вместо Cu
10
S
5
на тот же объем. Такую
структуру рассматривают как антифлюоритовую. Почему "анти"? - исходя из соотношения
Cu:S=2:1 и F:Ca=2:1, но с обратным положением катиона и аниона - во флюорите по закону
ПКУ расположен катион, а в халькозине - анион.
Морфология. Очень редко халькозин образует уплощенные кристаллы. Обычно дает
мелкозернистые агрегаты, иногда сплошные, образует псевдоморфозы гексахалькозина по
борниту и халькопириту.
Свойства: Цвет на свежем изломе - свинцово-серый, за что минерал имеет другое
название - медный блеск; старая поверхность черная. Дигенит макроскопически отличается
от халькозина фиолетово-синим оттенком. Н=2-3, d°»5,5; сп. нет, минерал хрупкий при
ударе, но при царапании обнаруживает ковкость - от иглы или ножа остается блестящий
след, и это одно из свойств, по которым халькозин отличается от чрезвычайно похожей на
него блеклой руды. Второе свойство - это черта: у халькозина она черная, без оттенка, у
блеклых руд при растирании черты заметен буроватый оттенок. Кроме того, блеклые руды
имеют твердость 3-3,5 и ,кроме медных вторичных минералов, сопровождаются обычно
гидроксидами железа и скородитом, в то время как с халькозином скорее уместна
самородная медь. Поскольку халькозин - кластерное соединение, он хорошо проводит
электричество; легко растворим в HNO
3
с голубым окрашиванием раствора.
Генезис. I. Гипогенный:
1. Низко-Т гидротермальный - халькозин (чаще дигенит) образуется в богатых медью и
бедных серой сульфидных рудах; ассоц.: ковеллин, борнит, энаргит. Это - Бьютт, Монтана,
США : жилы до 10 км протяженностью; Кенникот (Аляска).
II. Гипергенный генезис.
2. Тип медистых песчаников и сланцев ( с проблематичным источником Cu-содержащих
р-ров, возможно поверхностных или низко-t° гидро-t°; частью оруденение считается
сингенетичным осадочным породам, его вмещающим). Это Джезказган, Казахстан,
Приуралье. Как подтип этого генетического типа - слабо метаморфизованные осадочные
породы с халькозин-борнитовым оруденением - медный пояс Сев. Родезии-Заира.
3. Зона окисления медных сульфидных м-ний - наиболее характерный для Chsn генезис! -
а именно: подзона вторичного сульфидного обогащения (зона цементации).
Изменение. На поверхности в условиях водно-воздушного окисления Chsn Covell+Cu°.
В дальнейшем образуются куприт, карбонаты, сульфаты меди. Взаимоотношения
халькозина с этими минералами хорошо видны на ранее приведенной схеме зоны окисления.
Группа борнита
Борнит Сu
+1,+2
5
Fe
+2
S
4
- пестрая медная руда, пурпурная руда, бурая медная руда,
фиолетовая медная руда, павлинья руда + еще 6 синонимов.
Химизм. В качестве примей - Re, Se, Te. Характерно образование твердых растворов - во-
первых, с халькопиритом, во-вторых - с халькозином и дигенитом (при Т>300°С При
охлаждении эти твердые р-ры распадаются, возникают структуры распада Born+Chsn;
Born+Chpyr.
Структура. Такое "пристрастие" борнита к образованию твердых растворов обусловлено
структурными особенностями - наличием полиморфных модификаций.
А. Высоко-Т кубическая (>230°С). Эта структура похожа на структуру кубического
халькозина (-дигенита) - та же ПКУ S
-2
, все октаэдрические пустоты свободны; но вот в
заселении тетраэдрических позиций есть отличия, а именно:
34
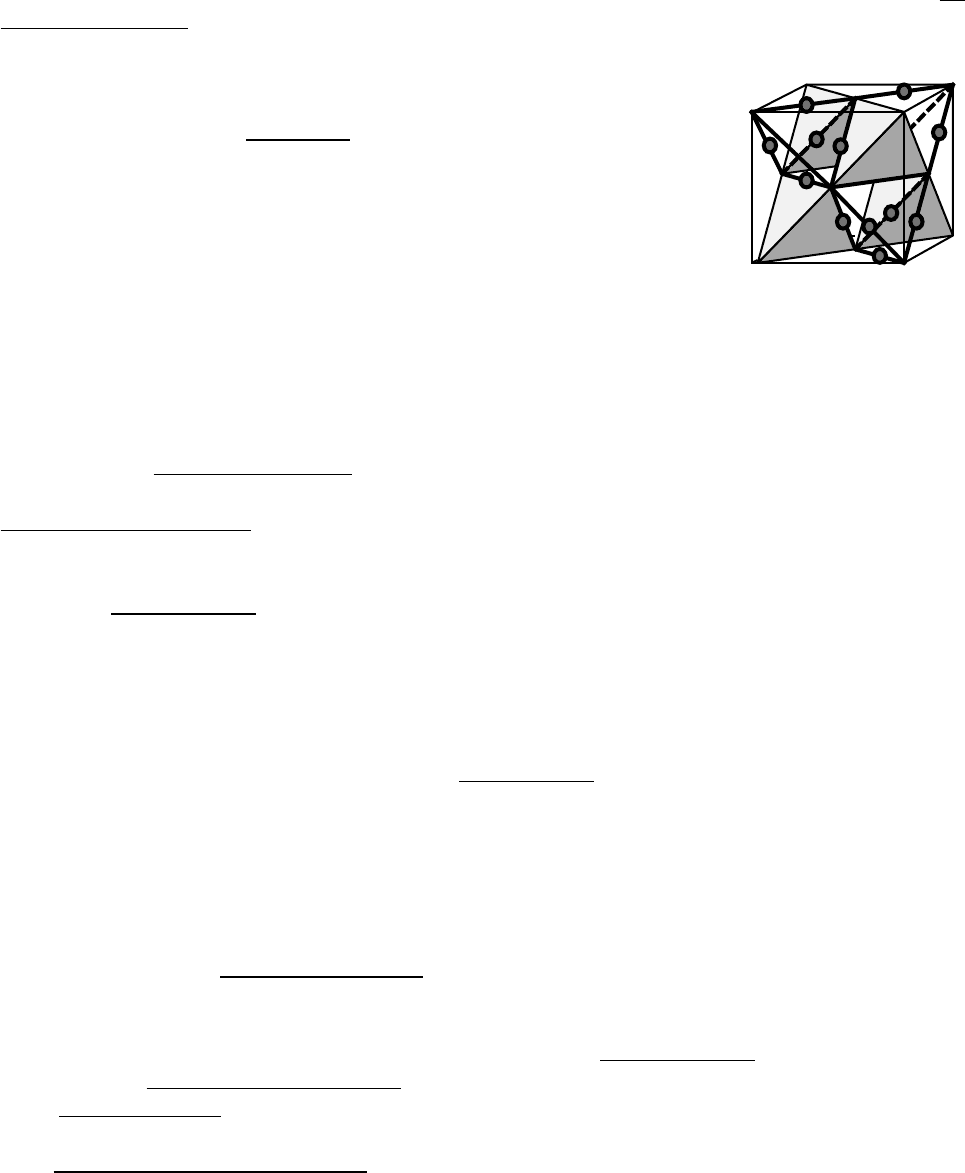
1. Половина тетраэдров заселена Fe
+2
, т.е. КЧ
Fe+2
=4. Эти тетраэдры расположены по
алмазному закону: в вершинах кубической элементарной ячейки, в серединах ее граней и в
четырех из восьми октантов - по тетраэдру (рис...).
2. Логично ожидать, что медь занимает вторую половину
тетраэдров. Так и есть, но только располагаются ионы Cu
+1
не в
средине тетраэдров, а на ребрах этих тетраэдров; при этом каждая
частица Cu+1 находится между двумя вершинами тетраэдров - между
двумя S
-2
. Т.е. КЧ
Cu+1
=2. Ребер 6, значит на каждый тетраэдр должно
приходиться 6 частиц Cu
+1
; но происходит замена - по схеме 2Cu
+1
Cu
+2
: т.е.одно ребро в тетраэдре остается свободным (вакансия) а на
другом вместо Cu
+1
располагается Cu
+2
(рис...).
Такие [Cu
5
S
4
]-тетраэдры располагаются на середине ребер элементарной ячейки и в
четырех оставшихся октантах (рис...). Значит, формула Cu
5
FeS
4
расшифровывается по
структуре так: Cu
+1
4
Cu
+2
Fe
+2
S
4
. Проекция структуры в целом на плоскость (001) дает
положение [FeS
4
]- и [Cu
5
S
4
]-тетраэдров между собой (рис...). Из нее очевидно, что структура
должна быть кубической. Но тут сказывается распределение вакансий.
Если вакансии распределены беспорядочно, то структура будет кубической - высоко-Т
модификация, кубический борнит Fm3m. Если же распределение вакансий упорядочивается,
происходит снижение симметрии, получается вторая структурная модификация -
тетрагональный борнит P42
1
с.
Переход кубической модификации в тетрагональную сопровождается образованием
промежуточных модификаций ( по мере упорядочения расположения вакансий), одна из
которых, тригональная, очень близка к структуре халькопирита (структурный мотив
сфалерита) - отсюда понятно образование твердых растворов Born-Chpyr. Кубическая же
структура борнита близка к структуре халькозина-дигенита - отсюда образование твердых
растворов с халькозином и дигенитом. А это значит, что очень часто все эти минералы будут
встречаться (и образовываться!) совместно. Для структуры Chsn-Dygen мы видели
возможность взаимодействия Ме-Ме, в имеющей аналогию структуре борнита - то же самое,
следовательно, минералы гр. борнита будут кластерными образованиями.
Морфология. Кристаллы с простыми формами {100}, {110}, {111}- очень редки. Обычно
борнит образует вкрапленники, зерна, каемки вокруг Chpyr, сплошные зернистые агрегаты.
Свойства. Ну, не даром у этого минерала столько синонимов, и все цветные! - он очень
быстро покрывается побежалостью и приобретает "цвет засохших чернил", становится
пестрым ("павлинья руда"). В свежем сколе он темномедно-красный, с оранжевым оттенком
(в случае твердых растворов с Chpyr) или с розовым (при распаде твердых растворов с
дигенитом). Блеск полуметаллический. Сп. нет, излом мелкораковистый. Н=3, d»5.
Хрупкий. Растворяется в HNO
3
(S, р-р голубой).
Диагностика: похожие: 1) никелин - не дает побежалости, Н»5, другого цвета
вторичные продукты; 2) Cu° -другой оттенок цвета, блеск металлический, ковкость.
Генезис. I. Гипогенное образование.
1. Магматический, в виде вкрапленников в основных породах (с Chpyr, Ti-Mgt). Это
Волковское м-ние (Екатеринбургская обл.).
2. Гидротермальное образование:
А. Вулканогенные типы:
а) Медно-порфировые руды (вкрапленность, прожилки Chpyr + Born + MoS
2
+ Ferz (блекл.
руда) - в Qu-порфирах или близповерхностных гранитоидных массивах. Это Чукикамата,
Чили.
б) Медно-колчеданные м-ния - Урал.
Б. Плутоногенные типы:
а). Жильные образования - полиметаллические и меднорудные жилы: Успенское
(Казахстан), Бьютт (Монтана, США), Цумеб (Намибия).
б) Сульфидное наложение на скарны - меднорудные скарны Хакассии.
35

II. Гипергенное образование:
3. Медистые песчаники и сланцы - проблематичный тип, возможно частично
сингенетичный осадочным породам, частично - гидротермальный. Это Джезказган,
Казахстан; Мансфельд, ФРГ.
4. Зона окисления медных сульфидных м-ний. Здесь идет целый ряд реакций, в результате
некоторых из них образуется борнит (в том числе в подзоне вторичного сульфидного
обогащения):
CuFeS
2
+4O2 CuSO
4
+FeSO
4
,
2CuFeS
2
+3CuSO
4
+3FeSO
4
Cu
5
FeS
4
+2Fe
2
(SO
4
)
3
,
CuSO
4
, FeSO
4
, Fe
2
(SO
4
)
3
- сильные окислители.
CuFeS
2
+CuSO
4
2CuS+FeSO
4
,
Cu
5
FeS
4
+Cu
+2
2Cu
2
S+2CuS+Fe
+2
,
CuS+2e Cu°+S-2.
Изменение - см. схему изменения халькопирита и выше приведенные реакции.
Применение. Важная часть медных руд.
Cемейство сфалерита-вюртцита
Включает две полиморфные модификации ZnS и соответствено две группы: гр сфалерита
и гр. вюртцита.
Гр. сфалерита
Сфалерит ZnS, цинковая обманка.
Хим. Главная ИП - Fe
+2
, его бывает настолько много, что иногда это отражают в формуле:
(Zn,Fe)S. Высокожелезистые разности имеют свое название - марматит, в отличие от
безжелезистых клейофанов. Обратим внимание, что изоморфизм Zn-Fe имеет направленный
характер: нет непрерывного ряда ZnS-FeS из-за различия структур сфалерита и троилита,
поэтому Fе
+2
может входить вместо Zn
+2
в структуру сфалерита, и в большом количестве, а
вот Zn
+2
в структуру троилита, несмотря на близость ионных радиусов, не входит. Такой
изоморфизм называют полярным. Железистость сфалерита зависит:
1) От давления. Увеличение Р переводит Fe
+2
в более плотную структуру: КЧ
Fe+2
в пирите
и пирротине - 6, а в сфалерите - 4.
2) От концентрации S: увеличение активности S способствует уходу Fe в пирит или
пирротин: 2(Zn,FeS)+S ZnS+FeS
2
.
3) От Т: при прочих равных условиях (постоянстве Р, rS) повышение Т способствует
вхождению Fe в структуру сфалерита (т.е. действие Т обратно действию Р!). На этом
основан геотермометр Куллеруда (Каллеруда), и хотя он очень относителен, но в общем
выдерживается зависимость - более высоко-Т сфалериты - более железистые.
Из других ИП для высоко-Т сфалеритов характерны также Mn, In (в марматитах Sn м-
ний); для клейофанов (средне-Т) - Cd (до 2,5% CdS), Ga, Ge, Co, Hg.
Стр. S
-2
образует ПКУ, Zn занимает 1/2 тетраэдрических пустот, все тетраэдры
ориентированы одинаково. F(-4)3m. (С такой структурой мы встречались у халькопирита,
станнина; геометрическая аналогия со стр-рой алмаза!)
Морф. Кристаллы - тетраэдрического габитуса, часто одновременное присутствие граней
"+" и "-" тетраэдров уподобляет кристалл октаэдру (разная скульптура: "-"гладкие грани, "+"
несут треугольные ступеньки и спиральную штриховку, на "+" идет эпитаксическое
нарастание Chpyr, на "-" - нет). Бывает огранка в форме {110}. Двойники по {111} -
сфалеритовый закон (равноценен шпинелевому закону для оксидов), полисинтетические
двойники, зернистые агрегаты. Порошковатые разности - брункит.
Св. Цвет - от черного (марматит) до желтого (клейофан), промежуточные по
железистости - бурые, коричневые. Cd в маложелезистых сфалеритах дает красный оттенок,
Co-содержащие сфалериты - зеленые. Блеск алмазный. Черта в зависимости от
36
железистости: от светлой, слабо желтоватой, до бурой. Сп. сов. по {110} (рис...). Н=3,5-4,
d=4.
Диагн. Похожи: энаргит - только два напр. спайности; вольфрамит - одно напр. сп.,
выделения вытянутые, тяжелее в два раза; касситерит - Н=6-7, нет сп., высокая плотность;
сидерит - характерная сп. по ромбоэдру.
Ген. 1. Гидротермальный.
а) Наложенная минерализация в скарнах - с Pyrr, Aspyr, (наиболее высоко-Т), с Gal,
иногда сульфосолями - блеклой рудой и буланжеритом (средне-Т). Тетюхе (Приморье),
Савинское (Забайкалье), Лянгар (Узб.); Брокен-Хилл (Австрал.).
б) Полиметаллическое (Pb-Zn) жильное оруденение (средне-T до низко-T)- c Gal, Chpyr,
Born, Ferz - Рудный Алтай, Забайкалье.
в) Колчеданные залежи (вулк.-осад.+низко-T гидро-T проработка) - как правило без
галенита! - с Pyr, Chpyr, Born, Ferz. Урал, Екатеринбургск. обл.
г) Вулканогенное близповерхностное образование - с Aspyr, Wt, SnO
2
и в то же время с
сульфосолями, Chpyr, Born, - все очень тонкодисперсное, т.наз. "черные руды Японии"
(куромоно, око, кейко) - о-в Хонсю.
д) Телетермальные (низко-T) образования - почковидный Sphal, порошковатый брункит,
вюртцит, марказит, Pyr, Pyrr, Chpyr, (Gal - подчинен.). Олькушское м-ние (В. Силезия,
крупнейшее в Европе, разрабатывается уже 600 лет), Джоплин (США).
2. В осадочных породах (в конкрециях сидерита, фосфоритов, тонкая вкрапленность в
мергелях - медистые сланцы Мансфельда (ФРГ), в аргиллитах юго-востока Сибирской
платформы и во многих других случаях. Полигенность образования: частично
сингенетичное за счет сероводородного заражения бассейнов, частично - более позднее, при
взаимодействии глубинных эманаций с нефтью, что позволяет использовать как поисковый
признак на нефть.
Изм. В пов. усл. разрушается в присутствии CO
2
или (СО
3
)
-2
, переходит в смитсонит
ZnCO
3
, в присутствии кремнекислоты - в гемиморфит Zn
4
[Si
2
O
7
](OH)
2
H
2
O и виллемит
Zn
2
[SiO
4
] - образуются т.н. галмейные руды. За счет ИП Fe образуется лимонит.
Знач. Основная руда на Zn и главный источник Cd, In, Ga.
Основная часть Zn используется для изготовления оцинкованной жести, цинковых белил,
в фармацевтическом производстве. Менее известно применение Cd. Сплавы 99% Cd и 1% Ni
- подшипники в авто-, самолето-, и судовых двигателях, работающие при высоких T.
Легирование меди кадмием - более износостойкие провода для электротранспорта, Cd-Ni
аккумуляторы более надежны, чем свинцовые, и используются в управляемых ракетах. Сd -
это также регулирующие и аварийные стержни атомных реакторов, CdSe - окраска
рубинового стекла.
Применение In. Использование в подшипниках авиационных и автодвигателей
пятикратно увеличивает срок службы. Легкоплавкие сплавы In+Ga с T плавления 16°С и
сплавы Bi+Pb+Sn+Cd+In (T плавления 46,5°С) - пожарные предохранители и сигналы.
Полупроводниковая техника - припои с In дают возможность соединять стекло, керамику и
металлы, легирование германиевых диодов индием создает дырочную проводимость -
основа транзисторов. Наконец, антимонид индия (интерметаллид!) - основа инфракрасных
детекторов (ночное видение по тепловому излучению).
Гр. вюртцита.
Вюртцит ZnS
Гринокит CdS
Вюртцит (лучистая цинковая обманка)
Хим. ИП Mn
+2
(до 13%), Fe
+2
(до 6%), Cd до 3,7%.
Стр. В отличие от сфалерита, S
-2
образует ПГУ, 1/2 тетраэдрических пустот занята Zn
+2
, в
соседних слоях тетраэдры повернуты относительно друг друга. P63mc. Политипия.
37

Морф. Лучистые агрегаты, плотные, скрытокристаллические; шестоватые прожилки,
редко пирамидальные кристаллы с гранями призмы и моноэдром.
Св. Цвет, блеск, тв. - как у сфалерита, но сп. сов. по призме {10,-1,0} ( по удлинению!).
От Sphal отличают по х-ру выделений, хотя нередко наблюдаются параморфозы Sphal по
вюртциту.
Ген. Вюртцит образуется из кислых гидро-T р-ров при низкой T и Р. Часто
колломорфные выделения из гелей - Олькушское м-ние (В.Силезия, Польша), где
наблюдается чередование сфалерита и вюртцита в зонально-концентрических агрегатах в
доломитизированных осадках с полостями. Cd-вюртцит известен на м-нии Цумеб (Намибия)
в ассоциации с медной минерализацией и пиритом.
Гринокит CdS (кадмиевая обманка).
Хим. ИП Zn до 58%.
Стр. вюртцита P63mc.
Морф. Порошковатые и землистые агрегаты.
Св. Цвет "канареечно-желтый", до оранжевого, черта оранж., до кирпичной, блеск алм.,
сп. сов. по {10,-1,0} - но все это, кроме цвета, неопределимо из-за тонкодисперсности
агрегатов.
Ген. Зона окисления сульфидных м-ний - по Cd-содержащему сфалериту. Редок, известен
лишь в виде мин. находок - Пршибрам (Чехия), колчеданное Сибаевское (Ю.Урал), Алтын-
Топкан (Тадж.), Кан (Кирг.).
Группа халькопирита.
Халькопирит CuFeS
2
. Синоним: медный колчедан.
Химизм. Халькопирит богат примесями - как изоморфными, так и за счет микровростков
других минералов, образующихся при распаде твердых растворов. Отметим содержащиеся в
наибольшем количестве Mn, Ag, Zn, (In, Ga), Bi, Sb, As, Te, Se. Особенностью химизма
является образование твердых растворов халькопирит-пирротин (халькопирротинов) с
ограниченной смесимостью компонентов в пропорции от 1:6 до 1:1, халькопирит-сфалерит
(неограниченная смесимость при T>600°С) и халькопирит-борнит (выше 700°C). Эта
особенность тесно связана со структурой.
Структура. Сера образует ПКУ, в которой 1/2 тетраэдрических пустот занята Cu
+1
и Fe
+3
,
(аналогия со структурой алмаза-сфалерита).
При Т>820°K (~550°C) заполнение пустот Сu
+1
и Fe
+3
неупорядоченное, такая структура
имеет симметрию F4,-3,m, и формула такого кубического халькопирита может быть
выражена (Cu,Fe)S, - структура в точности соответствует структуре сфалерита ZnS, с той
лишь разницей, что в сфалерите лишь один "сорт" катионов - Zn. Поэтому обычно структуру
Chpyr и уподобляют структуре сфалерита - "решетка типа Sphal", и это подобие и вызывает
образование твердых растворов Chpyr-Sphal, которые при понижении T дают структуры
распада.
При T<820°K заполнение тетраэдрических пустот упорядоченное: Cu
+1
и Fe
+3
чередуются по слоям пустот ^L
3
, в связи с этим удваивается параметр решетки по оси c, и
симметрия снижается до тетрагональной - I,-4,2d. Эта модификация наиболее
распространена, так что ее и будем характеризовать, говоря о халькопирите (хотя
существует еще одна, тоже тетрагональная, модификация).
Морфология. Кристаллы в виде тетрагональных тетраэдров, иногда - тетрагональных
трапецоэдров, двойники, сростки; эпитаксическое нарастание на Sphal (близость структуры!)
синтаксическое срастание с пиритом, блеклой рудой; чаще всего - зерна, вкрапленники,
зернистые агрегаты (иногда сливные).
Свойства и диагностика. Латунно-желтый с зеленоватым оттенком цвет, часто желтая,
синяя и разноцветная побежалость, мет. блеск, черта зеленовато-черная. H=3-4, d»4,3, сп.
отсутствует. Похожие минералы: Pyr (выше Н), Au (ниже Н, ковкость), Pentl (цвет и
38

спайность). Очень характерно развитие по Chpyr вторичных медных минералов - зеленых,
синих примазок малахита и азурита.
Генезис. Очень богат генетическими типами:
1. Магматический генезис.
а) Ликвационно-магматический - Cu-Ni сульфидные руды, связанные с основными-
ультраосновными породами: Норильск, Мончетундра, Печенга; Седбери (Канада).
б) Кроме собственно-ликвационных к этому же типу относится связанное с теми же
массивами позднее, по-видимому метасоматическое, оруденение того же состава.
Ассоциация -Pyrr + Pentl+Chpyr+Mgt(Pyr).
2. Очень близко к (1) примыкает тип медно-порфировых руд - вкрапленность и прожилки
сульфидов в кварцевых порфирах и др. близповерхностных интрузиях. Ассоц.:
MoS
2
+Chpyr+Pyr - Коунрад, (Каз.); Алмалык (Узб.), Сорское (Хакасия), Чукикамата (медный
пояс Чили).
3. Гидротермальное образование.
а) Высоко-T сульфидное наложение в скарнах: с Pyrr, Mgt, Pyr; иногда с кобальтином
(Cotn), Spal, Gal. Это меднорудные скарны Хакасии, Турьинское и Гумешевское м-ния в
Екатеринбургской обл.
б) Высоко-T жильные м-ния W-Mo формации - Chpyr, Wt, MoS
2
, Bi
2
S
3
,- Караоба, Вост. и
Сев. Коунрад (все - Каз.), Корнуэлл (Англ.) (с SnO
2
).
в) Средне-T полиметаллические жильные м-ния - Chpyr - обычный минерал в ассоц: Gal,
Sphal, Pyr, блеклые руды (Казахстан и Рудный Алтай - Риддерское, Зыряновское,
Заводинское, Белоусовское м-ния).
г) Иногда в таких жилах Chpyr становится ведущим минералом, а ассоциация других
сульфидов бедна, тогда выделяют кварц-сульфидные жилы не как полиметаллический, а как
медный тип. (Бьютт, Монтана, США; Успенское, Казахстан).
4. Медно-колчеданные (Chpyr+Pyr), полиметаллическо-колчеданные, колчеданные м-ния.
Везде в ассоциации преобладает Pyr, Shpal; менее распространены Gal, блеклые руды.
Нерудные - Qu, Bat, Cat. Это вулканогенно-осадочные образования, позднее переработанные
гидротермальными растворами, метасоматически измененные; часто это пластового типа
залежи большой протяженности и больших запасов. Целая полоса таких колчеданных
залежей - на Урале: несколько м-ний в Екатеринбургской обл., Блявинское в Оренбургской,
Сибай в Башкирии - все на этой полосе. Из зарубежных - Рио-Тинто в Испании,
разрабатывается уже около 3000 лет, содержит больше половины мировых запасов
колчеданных руд. К этому же типу относят крупнейшее в Европе медное м-ние Оутокумпу
(Финляндия), где Chpyr+Pyrr+Sphal в брекчированном кварците образуют залежь.
5. Тип медистых песчаников. Здесь Chpyr - один из главных минералов, тесно связан с
Born, Chksn, Ferz (блеклой рудой). Генезис - неоднозначный: часть рудного материала
сингенетична осадконакоплению, часть возможно связана с более поздним
гидротермальным (?) привносом. Это стратиформные (имеющие форму пласта) м-ния:
Джезказган (Каз.), Удокан (Чит.обл.), медистые сланцы Мансфельда (Герм.), меднорудный
пояс Родезии.
Изменение. В зоне окисления халькопирит неустойчив. Его изменение можно выразить
следующей схемой:
Chpyr
Born Chksn
Covell
гидроксиды Fe + Cu°
тенорит CuO + Cu
2
O куприт
азурит Cu
3
[CO
3
]
2
(OH)
2
+ Cu
2
[CO
3
](OH)
2
малахит.
Значение. Важнейшая руда на медь (о применении речь шла при рассмотрении
самородной меди), источник добычи Se.
39

Род галенита-клаусталита.
Хим. Почему род? - непрерывные твердые р-ры PbS галенит PbSe клаусталит.
Значит, Se является наиболее обычной примесью в галените, кроме того характерны Ag, Sb
(для более низко-T галенита) и Bi ( для более высоко-T).
Стр. Самая известная из структур - "типа NaCl", но надо помнить, что характер связей
совсем иной. КЧ Pb=6, КЧ S=6.
Морф. Зернистые агрегаты: кр.зерн. = свинцовый блеск, тонкозерн. = свинчак, часто
"давленый" - с удлиненными зернами. Кристаллы - при более высоких T - куб, при более
низких - октаэдр.
Cв. и диагн. Цвет свинцово-серый, в к/зерн. агрегатах с голубоватым оттенком. Иногда
синяя или пестрая побежалость. Черта черн. Бл. мет. Хрупкий. Сп сов по {100} (сопоставить
со структурой: - ^L
4
скомпенсированные сетки Pb,S---Pb,S), иногда отдельность по {111}
(эндотаксия висмутина, возникающего при распаде Bi-содержащих твердых растворов).
Излом ступ. Н=2-3, d=7,6. Диагностическими признаками являются форма кристаллов,
спайность, высокая плотность. Сильно исцарапанный образец Gal "пишет" по бумаге - тогда
его путают с MoS
2
, и надо смотреть оттенок растертого порошка- у MoS
2
он будет
заленоватым. Давленный Gal с вытянутыми зернами принимают за антимонит -
внимательно проверить спайность и ассоциацию.
Ген. А. Гидро-T средне- и низко-T.
1. Наложенная сульфидная минерализация в скарнах (Gа-Px) - со Sphal, Pyrr, Aspyr - та
же, что и для Sphal (Тетюхе, Приморье; Савинское, Заб.; Лянгар, Узб.).
2. Гидро-T жильный:
а) полиметаллические м-ния (Рудный Алтай, Забайкалье).
б) сульфидно-касситеритовые (Приморье и др.).
Б. При некоторых процессах осадкообразования - в полостях внутри конкреций
фосфоритов (Подолия) за счет реакций сероводорода с солями свинца либо взаимодействия
органики с PbSO
4
.
Изм. В зоне окисления может замещаться англезитом Pb[SO
4
], церусситом Pb[CO
3
],
вульфенитом Pb[MoO
4
], пироморфитом Pb
5
[PО
4
]
3
Cl, миметезитом Pb
5
[AsO
4
]Cl т.е. входить
в состав галмейных руд с каламином, лимонитом.
Знач. Источник Pb, а также значительной доли Ag, Bi, Se. Из всех цветных металлов
только Al, Cu и Zn производятся в большем количестве, чем Pb.
Использование Pb: 1/3 - на изготовление автомобильных аккумуляторов. Топливная
пром. - этилированный бензин, за счет 1г/л тетраэтила свинца в бензине за год над морями и
океанами северного полушария выпадает около 50 тысяч тонн Pb! Электротехническая
пром. - оболочка кабелей. Типографский сплав Pb+Sb+Sn (шрифты для газет, журналов).
Сурик, свинцовые белила - краски, известные еще 3000 лет назад. Рентгеновская защита,
свинцовые экраны в атомной энергетике.
Семейство киновари- метациннабарита .
Семейство включает две полиморфные модификации HgS и соответственно две группы -
киновари и метациннабарита. Прежде всего вспомним: "хидраргиум"- "серебряная вода",
поскольку ртуть единственный металл, жидкий при комнатной температуре.
Гр. киновари.
Киноварь HgS. Название "киноварь" возводят к персидским источникам и переводят как
"кровь дракона", хотя ничего общего ни с кровью, ни с драконом в персидском языке это не
имеет. Между тем слово это - искаженное "циннабар"с типичной для русского языка
заменой латинского "с" на"к" (центавр-кентавр) и однокоренное с метациннабаритом
("циннабарит" -"тяжелое олово", из-за похожести ртути на расплавленное олово). "Кровью
дракона" киноварь стала называться по парагенезису с антимонитом, который в средние века
алхимики именовали "драконом".
40
