Горохов А.А. Общая химия: Курс лекций
Подождите немного. Документ загружается.


51
Перенося все значения концентраций в правую часть равенства, а
постоянные К
1
и К
2
– в левую и обозначая их отношение через К
с
имеем:
C
2
I
2
H
2
HI
2
1
K
CC
C
K
K
=
⋅
=
Постоянная К
с
называется константой равновесия. Уравнение является
выражением закона действия масс для рассматриваемой реакции. Этот закон
был выведен подобным же путем Гульдбергом и Вааге.
Для гомогенных равновесных систем он формулируется следующим
образом: произведение концентраций образовавшихся веществ, деленное на
произведение концентраций исходных веществ, в равновесной системе при
постоянной температуре есть величина постоянная, называемая константой
равновесия. В уравнении закона действующих масс концентрации всех веществ
записываются в степени, равной их стехиометрическим коэффициентам в
уравнении реакции. Предположим, что
А
ν
моль вещества А взаимодействует с
В
ν моль вещества В с образованием
С
ν
моль вещества С и
Д
ν
моль вещества Д
по реакции:
ДСВА
ДСВА
ν
+
ν
⇔
ν
+
ν
Тогда имеем:
С
В
В
А
А
Д
Д
С
С
Кconst
СС
СС
==
⋅
⋅
νν
ν
ν
, (15)
где С
А
, С
В
, С
С
, С
Д
– равновесные концентрации веществ;
А
ν ,
В
ν ,
С
ν
,
Д
ν – стехиометрические коэффициенты;
К
с
– константа равновесия.
Если во взаимодействии участвуют газообразные вещества, то равновесие
количественно может быть охарактеризовано не через концентрации, а через
равновесные давления:
Р
В
В
А
А
Д
Д
С
С
Кconst
РР
РР
==
⋅
⋅
νν
ν
ν
, (16)
где Р
А
, Р
В
, Р
С
, Р
Д
– равновесные давления участников реакции;

52
К
р
– константа равновесия.
Какую информацию несет величина константы равновесия? Прежде всего
она позволяет судить относительно содержания реагентов и продуктов реакции
в равновесной системе. Например, сравнение двух величин констант при
разных температурах К
р
=100(25
0
С) и К
р
=0,01(300
0
С) показывает, что при
низкой температуре в равновесной смеси больше продуктов реакции С и Д,
тогда как при высокой температуре преобладают реагенты – А и В. Это, в свою
очередь, позволяет управлять процессом и проводить реакции так, как –
диктуют потребности практики.
Различают гомогенные и гетерогенные химические реакции. Гомогенный
– значит однородный. Типичными гомогенными реакциями являются
химические процессы в растворах и газах:
)г(2)г(2)г(
СО2ОСО2
⇔
+
2
О
2
2
СО
2
2
СО
С
СС
С
К
⋅
=
+
−
−
−
−
+
⇔
)рр()рр(3
)рр(
3
НСООСНСООНСН ,
СОО
3
СН
НСОО
3
СН
С
С
СС
К
+−
⋅
=
Химические реакции, в которых реагирующие вещества находятся в
различных фазах, называются гетерогенными. Достижение химического
равновесия в такой системе соответствует существованию равновесных
концентраций или равновесных давлений участников реакции. Однако
индивидуальные химические соединения в твердом и жидком состояниях не
меняют состава фазы при изменении условий равновесия, оставаясь 100%-
ными по составу кристаллическими или жидкими соединениями. В то же время
газы, участвующие в химическом равновесии, меняют концентрацию при
изменении внешних условий (изменение температуры, объема). Поэтому в
гетерогенных химических реакциях в выражение константы равновесия
учитываются только переменные равновесные концентрации (равновесные
давления) участников реакции. Например,

53
)г(2)ж()к(
ОHg2HgO2 +⇔
2
OC
CK
=
;
2
Op
PК =
)г(2)к()к(3
СОСаОСаСО +⇔
2
COC
CK
=
;
2
СОр
РК =
−
−
+
−
+⇔
2
)pp(4
2
)pp()к(4
SОBaBaSO
−+
⋅
=
2
4
SO
2
Ва
C
CCK
Несмотря на то, что константы равновесия гетерогенной реакции
выражается через парциальные давления газообразных реагентов (О
2
и СО
2
)
величина К
р
будет зависеть от свойств всех участников реакции (HgO и Hg;
CaCO
3
и CaO). Так, при термодинамической диссоциации MgCO
3
и CaCO
3
выражение для константы равновесия одно и то же,
2
СОр
РК
=
, но величина ее
различна, так как химические потенциалы MgCO
3
и MgO отличаются от
химических потенциалов СаСО
3
и СаО.
На основании термодинамических расчетов, которые здесь опускаются,
для реакции
dDсСвВаА
+
⇔
+
установлена взаимосвязь между функцией Гиббса и неравновесными
концентрациями реагентов и продуктов реакции (уравнение изотермы)
)Kpln
PP
PP
(lnRTG
b
'
B
a
'
A
d
'
D
c
'
C
−
⋅
⋅
=∆ (17)
)Kcln
CC
CC
(lnRTF
b
'
B
a
'
A
d
'
D
c
'
C
−
⋅
⋅
=∆ (18)
где Р
i
’
и C
i
’
– неравновесные давления и неравновесные концентрации
реагентов и продуктов реакции.
Всякое равновесие лишь относительно и временно. С изменением
внешних условий (Т, Р, С) состояние системы изменяется. Применительно к
химическому равновесию это означает, что равновесие сдвигается в сторону
образования в большем количестве либо продуктов реакции, либо реагентов.
Рассмотрим влияние изменений концентраций участников реакции на
смещение химического равновесия. Для этого воспользуемся (17). Величина и
знак G∆ представляет собой показатель свойства, по которому можно судить о
направлении смещения химического равновесия. При 0G <
∆
неравенство

54
показывает, что в реакционной смеси имеется избыток реагентов (А и В) и
недостаток продуктов (С и D) по сравнению с равновесным состоянием.
0
CC
CC
lnRTKlnRT
b
'
B
a
'
A
d
'
D
c
'
C
c
<
⋅
⋅
+−
b
'
B
a
'
A
d
'
D
c
'
C
C
CC
CC
K
⋅
⋅
>
В этом случае реакция будет идти самопроизвольно в направлении уменьшения
концентрации реагентов и увеличения концентрации продуктов до
равновесного состояния при котором 0G
=
∆
.
При 0G >∆ получаем:
0
CC
CC
lnRTKlnRT
b
'
B
a
'
A
d
'
D
c
'
C
c
>
⋅
⋅
+−
b
'
B
a
'
A
d
'
D
c
'
C
C
CC
CC
K
⋅
⋅
<
Неравенство показывает, что в реакционной смеси имеется избыток
продуктов реакции по сравнению с равновесным состоянием и
самопроизвольное прохождение реакции в прямом направлении невозможно.
Реакция пойдет в обратном направлении до тех пор, пока не будет достигнуто
равновесие, при котором 0G =∆ . В состоянии равновесия:
b
'
B
a
'
A
d
'
D
c
'
C
с
CC
CC
К
⋅
⋅
=
процессы превращения реагентов в продукты реакции и наоборот продуктов
реакции в реагенты не прекращается. Прямая и обратная реакции идут, но с
одинаковыми скоростями.
Для оценки влияния температуры на состояние равновесия системы
используется уравнение изобары химической реакции:
2
RTdT
lnK d
∆
Η
= (19)
−
∆Η
−=
21
2
T
1
T
T
1
T
1
RK
K
ln
(20)
Решение уравнения приводит к выражению (20), где Н∆ - изменение
энтальпии химической реакции;
1
Т
К и
2
Т
К - константы равновесия химической
реакции при температурах Т
1
и Т
2
соответственно.
55
Соотношение позволяет вычислить изменения энтальпии реакции по двум
константам равновесия
1
T
K и
2
T
K или вычислить константу равновесия при
заданной температуре, если известно изменение энтальпии реакции и
константы равновесия при другой температуре.
Неопределенное интегрирование уравнения изобары химической реакции
приводит к зависимости К от Т:
const
T
1
R
Кln +⋅
∆
Η
−= (21)
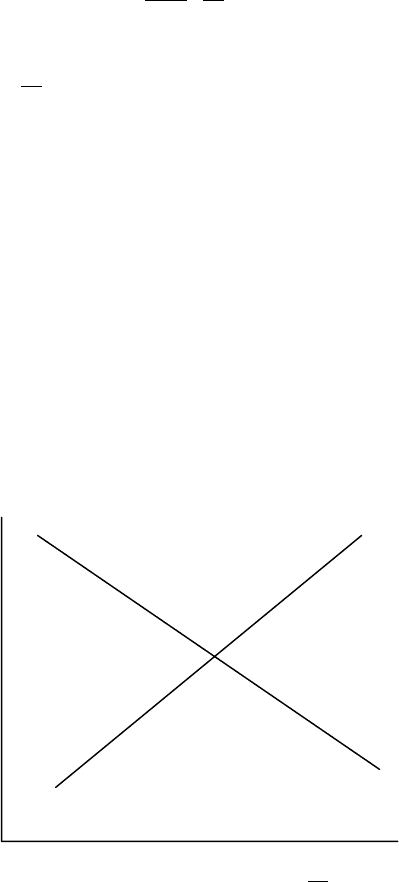
В координатах
T
1
-Кln уравнение представляет собой прямую линию,
наклон которой зависит от знака и величины энтальпии реакции.
Анализ уравнения показывает, что для экзотермической реакции )0Н(
〈
∆
увеличение температуры ведет к уменьшению константы равновесия, т. е. к
уменьшению содержания продуктов реакции и увеличению содержания
реагентов в равновесной смеси. Это означает смещение первоначального
равновесия в сторону обратной реакции, которая является эндотермической
)0Н( 〉∆ .
Рисунок 2 – Зависимость константы равновесия от температуры
lnK
p
1
0Н
〈
∆
0Н〉
∆
2
3
10
Т
1
⋅
1 – экзотермический процесс;
2 – эндотермический процесс
56
Для эндотермической реакции )0Н( 〉
∆
увеличение температуры ведет к
увеличению константы, т. е. к увеличению содержания продуктов реакции в
равновесной смеси, что означает смещение равновесия в сторону прямой
реакции, для которой как было принято, 0Н〉
∆
. Равновесие химической
реакции всегда смещается при увеличении температуры в сторону
эндотермического процесса. Влияние концентрации и температуры на
смещение химического равновесия обобщено в принципе Ле-Шателье-Брауна.
57
8 Кинетика химических реакций
Общие понятия и определения.
Термодинамический и кинетический критерий реакционной способности
химической системы.
Скорость химической реакции.
Факторы, влияющие на скорость химической реакции (концентрация,
температура, катализаторы, среда и др.).
Химическая кинетика – учение о химическом процессе, его механизме и
закономерностях развития во времени.
Все химические процессы, наблюдаемые в природе и осуществляемые
человеком в его практической деятельности, протекают во времени с
определенными скоростями. Часто в химической системе, содержащей
исходные химические вещества, могут протекать химические реакции с
образованием различных конечных продуктов. Например, из смеси углерода и
водорода при определенных условиях (Р, Т, катализатор) могут быть получены
альдегиды, органические кислоты, спирты и различные углеводороды. При
осуществлении химического процесса стремятся проводить его так, чтобы
выход какого-нибудь продукта был максимальным. Для этого надо создать
такие условия, при которых скорость образования необходимого продукта
будет значительно больше скоростей всех других возможных реакций.
Химическая кинетика, как и термодинамика, является теоретической
базой химической технологии. Поэтому состояние и достижения науки в
области кинетики и катализа в значительной степени определяют технический
уровень производства в химической промышленности.
В последние десятилетия в значительной мере расширились возможности
экспериментального исследования кинетики химических процессов в связи с
развитием ряда физических методов (спектроскопических,
радиоспектроскопических), позволяющих непосредственно, без проведения
58
сложных химических анализов, наблюдать и регистрировать ход химического
превращения. Стали доступны количественному исследованию быстро
протекающие химические процессы, заканчивающиеся за малые доли секунды,
вплоть до пикосекундных реакций. Уникальные возможности для исследования
сложных химических превращений в многокомпонентных системах открыли
газо-жидкостная хроматография и жидкостная хроматография под высоким
давлением. Огромное значение для современной химической кинетики имеет
интенсивное развитие вычислительной техники, появление
быстродействующих электронно-вычислительных машин. Благодаря им
ведется статистическая обработка больших массивов экспериментальных
данных по кинетике химических превращений, рассчитывается протекание
процессов, описываемых системами большого числа дифференциальных и
алгебраических уравнений, появилась возможность математического
моделирования реакторов. На базе законов химической кинетики
осуществляется подбор высокоэффективных катализаторов.
Рассмотрим какую-нибудь химическую систему, например, смесь СО и
Н
2
в определенных соотношениях. В этой системе могут протекать различные
химические реакции. Встает ряд вопросов: в каком направлении
преимущественно будет идти химический процесс при заданных температуре и
давлении? Какие условия надо создать, чтобы в результате процесса получить,
например, метиловый спирт? Какие свойства системы определяют ее
реакционную способность?
Реакционная способность химической системы при заданных условиях
характеризуется скоростью и возможной глубиной химической реакции.
Направление и глубина химической реакции определяется законами
химической термодинамики, согласно которым условия направленности и
равновесия химической реакции при постоянных Р и Т записываются в форме
0G
r
≤∆ . В качестве меры химического средства реакции принимается значение
нормального (стандартного) сродства )298(G
0
r
∆
. Нормальное сродство может
быть меньше и больше нуля. Термодинамически наиболее вероятны реакции, у
59
которых значение нормального средства наиболее отрицательны. Однако
химическое сродство определяет только возможную глубину процесса, но не
характеризует полностью реакционную способность системы. Примером этого
является смесь Н
2
и О
2
, для которой кДж 61,228)298(G)298(G
0
rr
−=
∆
≈
∆
,
следовательно, реакция должна идти практически до конца. Опыт же
показывает, что смесь Н
2
и О
2
при нормальных условиях может существовать
практически неограниченно долгое время без заметного образования воды.
Таким образом, реакционную способность химической системы нельзя
характеризовать только значением )Т(G
r
∆
. Термодинамическое условие
протекания реакции 0G
r
〈∆ при постоянных Р и Т можно принять как
термодинамический критерий реакционной способности химической системы.
Это условие является обязательным, но не достаточным. Если в смесь Н
2
и О
2
ввести катализатор в виде платиновой черни, то реакция заканчивается в
течение долей секунды. Это указывает на то, что есть еще какие-то факторы,
которые ускоряют химический процесс и тем самым дают возможность за
короткий отрезок времени проявиться химическому сродству, или, наоборот,
затрудняют реакцию, и термодинамические возможности не реализуются. Что
же можно выбрать в качестве характеристики кинетического критерия
реакционной способности химической системы? Наиболее общим
кинетическим критерием реакционной способности химической системы
является, конечно, скорость реакции.
Химическая реакция (химический процесс) состоит в превращении
одного или нескольких химических веществ, называемых исходными
веществами, в одно или несколько других химических веществ, называемых
продуктами реакции. В большинстве случаев химический процесс
осуществляется не просто путем прямого перехода молекул исходных веществ
в молекулы продуктов реакции, а состоит из нескольких стадий. В качестве
примера рассмотрим окисление Fe
2+
молекулярным кислородом в кислом
растворе. Стехиометрическое уравнение реакции записывается в виде:
60
OH2Fe4OH4Fe4
2
3
2
2
+
→
+
+
+++
Прямое столкновение 9 частиц, восемь из которых имеют положительный
заряд – событие крайне маловероятное. Более вероятным является протекание
приводимой ниже последовательности стадий:
2
3
2
2
ОFeOFe
•
−++
+⇔+
2
2
ОННО
•
+
•
−
⇔+
−+
•
+
+→+
2
3
2
2
НОFeОНFe
222
ОНННО
⇔
+
+−
НОFeООНFe
2
22
2
•
++
+Η→+
+
•
+
Η
→
+
22
FeОНОFe
+++
+
⇔
+
Η
3
2
2
FeОННFeО
требуется взаимодействие двух частиц (взаимодействие одноименно
заряженных, последняя стадия). Совокупность стадий, из которых
складывается химическая реакция, называется механизмом или схемой
химической реакции.
Количественные характеристики и закономерности протекания
химической реакции во времени неразрывно связаны с их механизмом. В этом
состоит отличие кинетических (временных) характеристик химической реакции
от термодинамических характеристик –
ср
К ,К ,G ,S ,
∆
∆
∆
Η – не зависящих от
пути, по которому протекает химическая реакция.
Характерной особенностью большого числа сложных химических
реакций является образование промежуточных частиц. Они могут быть
реакционно-способными валентнонасыщенными молекулами (Н
2
О
2
), ионами
(НО
2
-
), свободными радикалами ( НО ,ОН
2
••
), ионами радикалами (
2
О
•
−
).
Химическая реакция, протекающая в пределах одной фазы называется
гомогенной, протекающая на границе раздела фаз, называется гетерогенной
химической реакцией. Сложная химическая реакция, в которой одни стадии
