Гетьманчук Ю.П., Сиромятніков В.Г. Практикум з полімерної хімії
Подождите немного. Документ загружается.


логарифмічній формі lnk
еф
= lnA – E/RT, де k
еф
– ефективна
константа швидкості полімеризації, що визначена методом
описаним у лабораторній роботі № 4. Згідно рівнянню 2.4
k
еф
∼
5,0
3
1
2
k
k
k
звідки ln
RT
E5,00,5E E
A
A
Aln
k
k
k
312
5,0
3
1
2
5,0
3
1
2
−+
−=
, тобто
Е = Е
2
+ 0,5Е
1
– 0,5Е
3
(2.6 )
Лімітуючою стадією радикальної полімеризації є
ініціювання – воно має найбільшу енергію активації. Для
більшості ініціаторів, що гомолізуються термічно Е
1
складає
величину порядка 110 – 150 кДж/моль. Енергія активації росту
ланцюга Е
2
знаходиться в межах 20 – 40 кДж/моль, а обриву (Е
3
)
– найменша і складає 8 – 20 кДж/моль. Таким чином, сумарна
енергія активації Е при термічному ініціюванні знаходиться в
межах 80 – 90 кДж/моль. Це відповідає дво- або трикратному
збільшенні швидкості процесу при підвищенні темератури на
10
о
С. При інших способах ініціювання сітуація різко
змінюється. Так при окиснювально-відновному ініціюванні Е
1
складає лише 40 – 60 кДж/моль, тобто Е не перевищує 40
кДж/моль. Ще менша сумарна енергія активації (близько 20
кДж/моль) при фотохімічному ініціюванні. Тут температура
практично не впливає на швидкість полімеризації
Ефективні константи швидкості полімеризації k
еф
одержують, досліджуючи кінетику полімеризації в конкретній
системі (мономер – ініціатор - розчинник, концентрації -
постійні) при 2-х або більше температурах (Т - абсолютна
температура в кельвінах). Методика дослідження кінетики
полімеризації наведена в лабораторній роботі № 4. Якщо
полімеризація проводилася при двох різних температурах T
1
і Т
2
і визначені відповідні константи k
еф.1
та k
еф.2
, енергію активації
Е знаходять за формулою:
31

( )
)T (T e lg
k lgk lgTRT
E
12
21
еф.1еф.2
−
−
=
(2.7 )
де R = 8,314 Дж•моль
−
1
•К
−
1
; lg e = 0,4343.
У практиці, для одержання більш надійних величин Е,
вимірюють швидкість полімеризації при 3 та більшій кількості
температур. У цьому випадку розрахунок проводять графічно
шляхом побудови залежності lg k
еф
від 1/Т•10
3
. Тангенс кута
нахилу одержаної прямої дорівнює −E/8,3314 звідки
розраховуємо значення Е в кДж/моль.
2.6. Лабораторна робота №8. Визначення порядку
реакції полімеризації за ініціатором
Порядок реакції за ініціатором (α) можна розрахувати,
виходячи з рівняння швидкості радикальної полімеризації 2.4.
Якщо концентрацію мономеру [M] витримувати постійною то
єдиною перемінною у цьому рівнянні стане концентрація
ініціатору [I] і воно може бути записано, як v
2
= K•[I]
α
, де К =
][
k
k2
k
5,0
3
1
2
Μ
•
f
. Використовуючи це рівняння у логарифмічній
формі - lg v
2
= lgK + α lg [I] знаходять порядок за ініціатором α
як тангенс кута нахилу прямої залежності Ig v
2
від lg [I] до осі
абсцис.
Проводять полімеризацію мономеру в розчині з різними
кількостями ініціатора (наприклад, 0,5; 1,0; 1,25; 1,5 мас.%).
Кінетику полімеризації реєструють гравіметрично або
дилатометрично (відповідно до методик лаб.роб. №4 та №6) і
по прямолінійним ділянкам кінетичних кривих для кожної
концентрації ініціатора, знаходять відповідні значення
швидкостей полімеризації v
2
в моль/ л •с
−
1
.
2.7. Додатковий матеріал для семінарських та
контрольних робіт по кінетиці радикальної полімеризації.
Розгляд теоретичної частини теми "Радикальна полімеризація"
32
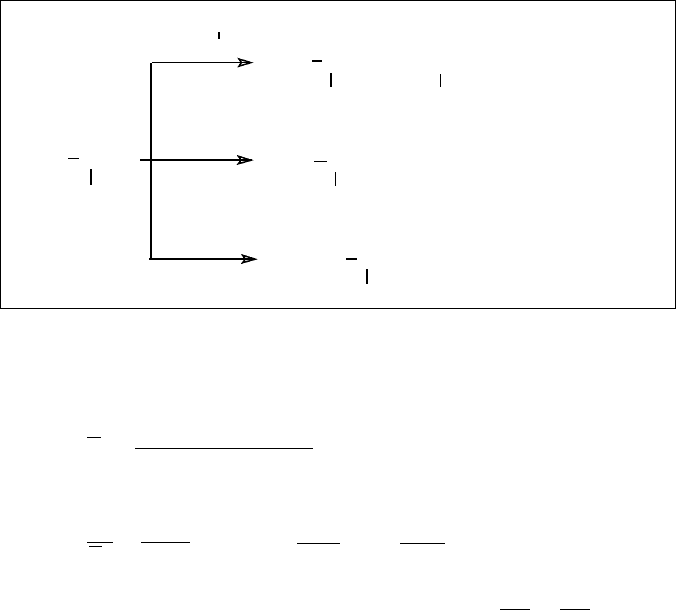
передбачає контрольну роботу, після успішного виконання якої,
студент допускається до лабораторної роботи. До цієї роботи
обов'язково входять кінетичні задачі, для вирішення яких
потрібно знати ще деякі реакції та кінетичні залежності.
На молекулярну масу полімеру (ступінь полімеризації),
крім розглянутих вище реакцій ініціювання, росту та обриву,
можуть впливати також реакції передачі ланцюга на мономер,
ініціатор (І) та розчинник (S):
Середній ступінь полімеризації залежить від
співвідношення швидкостей цих реакцій :
Ρ
n
v
v v v v
2
3 4M 4 4S
=
+ + +
I
, (2.8)
або при підстановці:
1 1
2
Ρ
n
C
M
=
+
+
λ
ν
+
C C
S
I
I ]
[M ]
S ]
[M ]
[ [
+
, (2.9)
де ν (середня довжина кінетичного ланцюга) =
v
v
2
3
=
v
v
2
1
;
λ (від 0 до 1) - частка реакції диспропорціювання;
С
М
, С
І
та C
S
- відносні константи передачі, що дорівнюють
відповідно k
4M
/k
2
, k
4I
/k
2
та k
4S
/k
2
.
Важливе значення у кінетиці радикальної полімеризації
мають також середній час життя кінетичного ланцюга, який
визначається з допомогою виразів
33
І
.
.
.
n
n
n
S
M
S
M
X
.
.
.
+
+
+
S
S
I
I
M
X
X
X
+
X
X
k
4
k
4
k
4
CH
2
=CH
~
CH
2
CH
2
S v
4
= k
4
[M ][S]
~
CH
2
CHR R v
4
= k
4
[M ][I]
~
CH
2
CH
2
CH=CH v
4
= k
4
[M ][M]
~
CH
2
CH
.
І
;
;
;
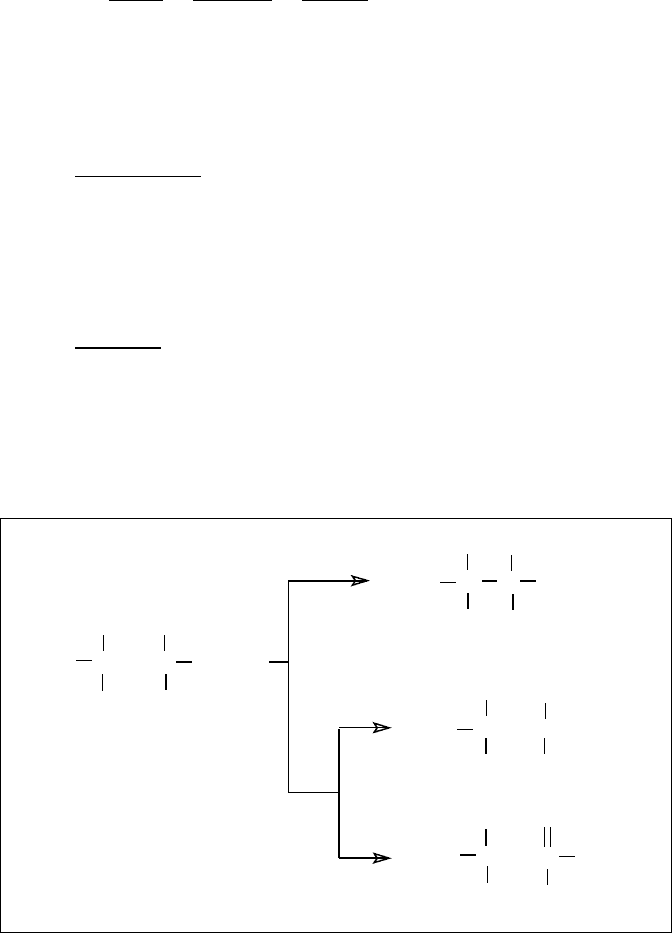
τ =
[M
v k M
k M]
k v
n
n3 3
2
3 2
•
•
= =
]
[ ]
[1
, (2.10)
та час життя одиничного радикала (час, за який ланцюг
збільшується на одну ланку) τ
1
= τ/ν.
Наведемомо типові приклади задач.
Приклад 1. Частка реакції диспропорціювання при
обриві макрорадикалів поліметилметакрилату становить 0,5.
Визначити середню довжину кінетичного ланцюга, час
існування кінетичного ланцюга та середню молекулярну масу,
якщо v
2
=8,1∙10
-6
моль∙л
-
1
∙с
-
1
; v
1
=1,2∙10
-9
моль∙л
-
1
∙с
-
1
;
k
3
=2,3∙10
6
моль
-
1
∙л∙с
-
1
; С
М
= 5,6∙10
-5
.
Рішення. Починати обов'язково треба із схем реакцій.
При їх відсутності задача вважається невирішеною. У даному
випадку необхідно звернути увагу на непомірно високу частку
диспропорціювання при полімеризації метилметакрилату (у
більшості мономерів вона не більше 0,1) і зобразити два
варіанти диспропорціювання, які можливі для цього
макрорадикалу:
34
диспропорціювання
рекомбінація
~
CH
2
C C CH
2
~
~
CH
2
CH C=CH
~
H
3
C
CH
3
OOC
CH
3
COOCH
3
+
~
CH
2
C C CH
2
~
CH
3
OOC COOCH
3
H
3
C CH
3
~
CH
2
CH C CH
2
~
H
3
C CH
3
CH
3
OOC COOCH
3
H
3
C CH
2
CH
3
OOC COOCH
3
k
3
k
3
д
р
.
.
+
+
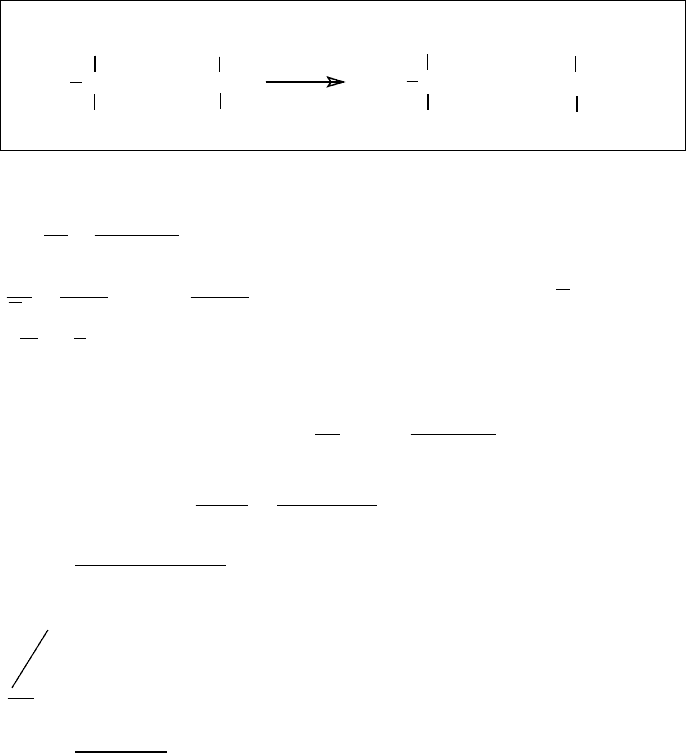
Специфічно для метилметакрилату проходить і реакція
передачі ланцюга на мономер:
Знайдемо середню довжину кінетичного ланцюга
ν
= =
•
•
=
−
−
v
v
2
1
8 1 10
1 2 10
6750
6
9
,
,
і підставимо її у рівняння 2.9:
1 1
2
1 5
13500
5 6 10 11 10
5 4
Ρ
n
C
M
=
+
+ = + • = •
− −
λ
ν
,
, ,
. Звідси
Ρ
n
=
9000
і
Μ Ρ
n n
m = 9000 100 = 900000 (m -
= • •
молекулярна маса
елементарної ланки). Виходячі з умов стаціонарності (v
1
= v
3
=
k
3
[
M
n
•
]
2
), знаходимо
[ ]
,
,
,
,
,
M
v
k
n
1
3
•
−
−
=
=
•
•
= •
0 5
9
6
0 5
8
1 2 10
2 3 10
1 73 10
моль/л, звідки τ
= =
•
•
≈
• −
−
[ ] ,
,
M
v
c
n
3
1 73 10
1 2 10
14
8
9
.
Приклад 2. Яка кількість полівінілацетату ([M]=4
моль/л) утвориться через 10 хвилин полімеризації у
присутності динізу ([I]=0,1моль/л), якщо
k
k
k C
2
3
0,5
1 M
= • = = • = •
− − −
2 10 0 6 1 6 10 6 10
2 6 3
; , ; , ;f
? Яка буде
Μ
n
?
Рішення. Треба записати всі реакції, які тут
відбуваються:
35
M
k
4
.
.
+
+
COOCH
3
COOCH
3
COOCH
3
COOCH
3
CH
2
CH
3
CH
3
CH
3
~
CH
2
C CH
2
=C
~
CH
2
CH CH
2
=C
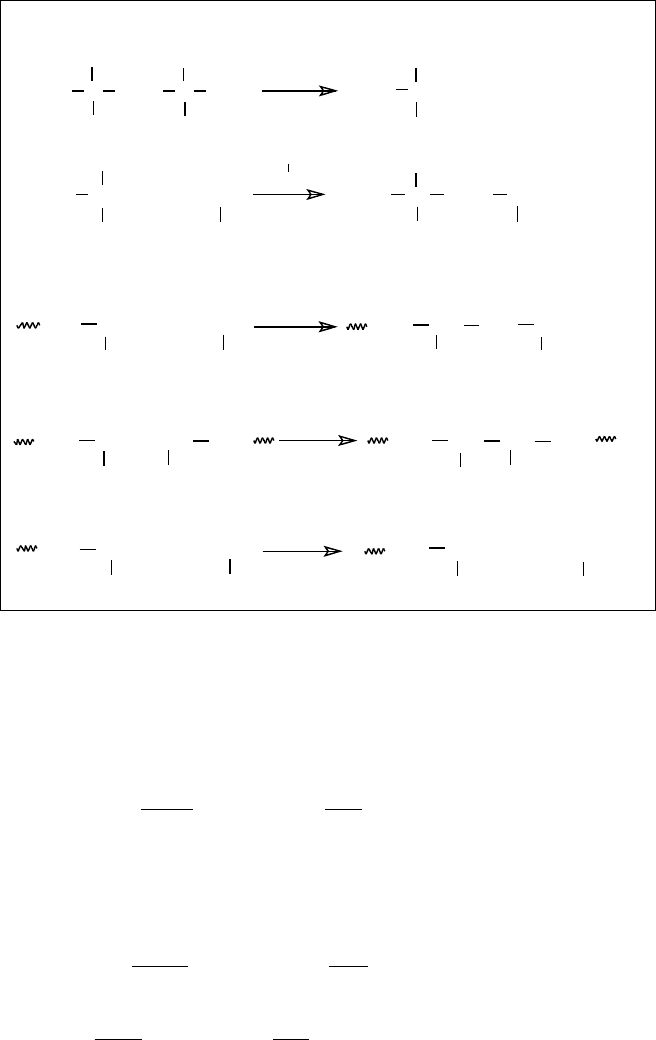
(Якщо в умові задачі не вказується про способ обриву, то
припускаємо, що це тільки рекомбінація).
Про кількість мономеру, що прореагував за 10 хвилин,
дізнаємося з диференційного рівняння швидкості:
v
d[M]
dt
k
k
k
M][I]
2 1
2
3
0,5
0,5
= − = •
( ) [
,
2
0 5
f
.
Нехтуючи зміною концентрації ініціатора, яка дуже
мала, інтегруємо рівняння від [M]
0
до [M] та від 0 до 600 с:
− = •
∫ ∫
[M]
[M]
d[M]
[M]
k
k
k
I] dt
1
2
3
0,5
0,5
600
( ) [
,
2
0 5
0
f
, звідки
ln
[M]
[M]
k
k
k
I]
0
1
2
3
0,5
0,5
= • •
( ) [
,
2 600
0 5
f
, або
36
2
CH
3
C N=N C CH
3
CH
3
C N
2
CN
CN
CH
3
CH
3
CH
3
C CH
2
=CH CH
3
C CH
2
CH
CN CN
CH
3
CH
3
OAc OAc
CN
CH
3
+
+
.
.
.
k
1
k
1
1.Ініціювання
2. Ріст ланцюга
СH
2
CH CH
2
=CH CH
2
CH CH
2
СH
OAc OAc
OAc
OAc
+
.
.
k
2
3. Обрив ланцюга
CH
2
CH CH CH
2
CH
2
CH CH CH
2
OAc OAc
OAc
OAc
.
.
+
k
3
4. Передача на мономер
CH
2
CH CH
2
=CH CH
2
CH
2
CH
2
=C
OAc
OAc
OAc
OAc
+
+
.
.
k
4
M

[M] = [M]
0
∙exp[-(2ƒk
1
)
0,5
∙
k
k
I]
2
3
0,5
0,5
[
∙600] = 3,99 моль/л.
Концентрація полімеру [M]
0
− [M] ≈ ≈ 0,001 моль/л.
Далі знаходимо ν =
v
v
та
2
1
n
Ρ =
2
ν
2.8. Задачі для самостійного вирішення.
13. Яка ефективність ініціювання 2,2
1
-азо-біс-(2,4-
діметилвалеронітрилу), якщо у присутності 0,5 г цього
ініціатора одержано 104 г полістиролу, що містить 0.035%
азоту? Конверсія ініціатора 80%.
14. Визначіть швидкість реакції ініціювання
полімеризації акрилонітрилу пероксидом бензоїлу при 80
о
С,
якщо індукційний період у присутності 0,01 г бутилмеркаптану
становить 1 годину. Інгібітор повністю подавляє ініціювання.
15. Період напівроскладу пероксиду ацетилу при 80
о
С
дорівнює 85 хвилин. Визначити швидкість ініціювання при цій
температурі , якщо [I]
0
= 0,02 моль/л. Ефективність ініціювання
0,75.
16. Через який час концентрація динізу зменшиться у
чотири рази, якщо k
1
=4•10
-5
?
17. При радикальній полімеризації вінілацетату, що
проходить з початковою (стаціонарною) швидкістю 4•10
-5
л/моль•с, час за який ланцюг збільшується на одну ланку
складає 0,0012 с. Визначіть v
1
, якщо середній час росту
кінетичного ланцюга складає 2 с.
18. Визначити
n
Μ
поліхлорвінілу, що містить 20, 30 і
50% фракцій із ступенями полімеризації 200, 300 і 500
37

відповідно. Як зміниться
n
Μ
цього полімеру якщо у тих же
умовах його одержання додати передатчик ланцюга ССІ
4
, якщо
С
S
= 0,2•10
-3
; [S]/[M]=2?
19. При полімеризації метилметакрилату до 30%-ної
конверсії швидкість реакції після стаціонарного стану
збільшилася у 1,8 рази, причому k
2
залишилася незмінною, а k
3
зменшилася на 72%. Визначити співвідношення часів існування
кінетичного ланцюга (τ
0
/τ
30
) на початку реакції і при 30%-ній
конверсії.
20. Яка потрібна концентрація акрилонітрилу для
утворення середньої довжини кінетичного ланцюга 500, якщо
концентрація ініціатора (пероксиду лаурилу ) 4,54•10
−
4
моль/л; k
1
= 6,0•10
−
4
с
−
1
; k
2
/k
3
0,5
= 0,07 л
0,5
х (моль•с)
−
0,5
?
21. Якою мусить бути концентрація динізу при
полімеризації ММА у масі, щоб
n
Μ
становила 200000, якщо
С
М
= 0,12•10
-4
; 60% обриву – диспропорціювання; k
2
/(k
3
)
0,5
=
1,36•10
-2
л
0,5
•(моль•с)
0,5
; k
1
= 4•10
-5
; ƒ = 0,6 ?
22. Знайдіть С
S
регулятора молекулярної маси при
полімеризації ММА ([M] = 5,7 моль/л), якщо при концентрації
цього регулятора 0,8•10
-3
та 2•10
-3
утворюються полімери з
n
Μ
відповідно 2,57•10
4
та 1,26•10
4
.
23. Як зміниться швидкість полімеризації стиролу та
молекулярна маса полімеру, якщо вихідний розчин мономеру
та ініціатора розвести у 3 рази?
24. Яка середня довжина кінетичного ланцюга при
полімеризації тетрахлоретилену, якщо час існування
кінетичного ланцюга 0,52 с , а час життя одиничного радикалу 2
38
•10
-3
с ? Яка
n
Μ
, якщо обрив на 15% іде
диспропорціюванням?
25. Визначити ступінь конверсії акрилонітрилу (%) через
3 години полімеризації у присутрості пероксиду бензоїлу, якщо
практично незмінними за цей час залишаються v
1
= 8•10
-7
моль•
(л•с)
−1
та
3
k
k
0,5
3
2
=
л
0,5
•(моль•с)
-0,5
.
26. Для одержання полівінілхлориду з
n
Μ
= 45000 в
систему додано 1,2 % (мол) регулятора – трихлоретилену (по
відношенню до мономеру). Без регулятора
n
Μ
= 60625.
Визначити C
S
. Регулятор у кополімеризацію не вступає.
27. Виведіть співвідношення, що пов’язує ступінь
конверсії мономеру із ступенем конверсії регулятора з
допомогою системи диференціальних рівнянь для v
2
та v
4S
Скільки регулятора СBr
4
залишиться непрореагувавшим (%)
при ступені конверсії вінілхлориду 0,4, якщо C
S
= 4,7?
28. 1 г/моль ММА полімеризуєтся у присутності 0,002
г/моль пероксиду ацетилу. Після закінчення реакції залишилося
10% мономеру та 25% ініціатора. Знайти
n
Μ
, якщо
ефективність ініціювання 0,7, а обрив іде рекомбінацією.
Література.
1. Гетьманчук Ю.П. Полімерна хімія. (ч. І. Радикальна
полімеризація). – К.: ВЦ “Київський університет”, 1999 – 143с.
2. Иванчев С.С. Радикальная полимеризация. – Л.:
Химия, 1985 – 280с.
3. Берлин Ал.Ал., Вольфсон С.А., Ениколопян Н.С.
Кинетика полимеризационных процессов. – М.: Химия, 1978 –
320с.
39

4. Лабораторний практикум з хімії та технології
полімерів. Під ред. Ірени Сповіковської. – Варшава.:
Варшавська політехніка, 1999 – 244с.
3. КОПОЛІМЕРИЗАЦІЯ
3.1. План колоквіуму. Кінетична схема бінарної
кополімеризації. Діференційне рівняння "миттєвого" складу
кополімеру Майо-Льюїса. Форми кривих складу кополімеру в
залежності від значень констант кополімеризації. Ідеальна та
альтернантна (чергуюча) кополімеризація, як граничні
варіанти статистичної бінарної кополімеризації. Точка
40
