Скляров Е.В. (ред.) Интерпретация геохимических данных
Подождите немного. Документ загружается.


140
Интерпретация
геохимических данных
железистые;
У/116—
карбонатистые,
железистые;
Vllle
—
высоко-
железистые (с =
25—40
%');
карбонатистые (с =
25—50
%);
ферросиаллиты
(с > 40 %
Fe
3
O
3
),
мергели
сиаллитовые;
сиаллитовые
карбонатолиты,
Vllle —
карбонатолиты
с примесью
сиаллитового
материала;
IX—
латериты;
IXa
~
слабожелезистые'
1X6
— железистые;
1Хв
~ высокожелезистые
(с
=
25—40
%
Fe,0
)•
/Хг
—
ферролатериты;
X—
латерит-бокситы:
Ха
— слабожелезис-
тые;
Хб—
железистые; Хв — высокожелезистые
(с
=
25—40
%
Fe.,0
);
Хг —
ферролатерит-бокситы;
XI — бокситы:
Х1а
— слабожелезис-
тые;
XI6
— железистые;
Х1в
— высокожелезистые (с =
25—40
%
Fe
2
0
3
).
На рис. 4.2 приведена диаграмма a— b расположения полей
составов вулканитов и некоторых интрузивных образований. Поля
составов:
1 — ультракислые
липаритоиды
($
4
3
)и
липаритоиды
(s
4
5
);
2 -
липарит-дацитоиды
(s
4
');
2а
—
трахилипарит-дациты
(п
> 0,21);
3 —
дацитоиды
(s
3
3
);
За —
трахидациты
(п > 0,21);
36
— щелочные
дациты
—
бостониты
и др. (п > 0,30);
4—
андезит-дацитоиды
(s
3
3
);
4а —
трахиандезит-дациты
(п > 0,17);
46—
андезит-дацитовые
тра-
хиты (п > 0,21); 5 —
андезитоиты
(s
3
');
5а
—
трахиандезиты
(п >
> 0,17);
56—
трахиты,
фонолитовые
трахиты и др. (п > 0,21);
6-
андезит-базальтоиды
Ц
4
);
6а
—
трахиандезит-базальты
(п > 0,17);
66 — щелочные андезит-базальты (андезит-базальтовые трахиты,
фонолиты
и др., п > 0,21); 6в —
толеитовые
андезит-базальты
(п =
=
0,07—0,13);
7
—
базальтоиды
(s\)\
7а
—
трахибазальты,
спилиты
(п
=
0,17—0,21);
76—
щелочные базальты (базальтовые трахиты,
фонолиты и др., п =
0,21—0,40);
7в — толеитовые базальты, трап-
пы (п < 0,10); 7г — габбро-анортозиты; 7д — анортозиты; 7е -
пикритовые
базальты; 8 —
базанит-базальтоиды
(s
2
2
);
8a
—
трахи-
базанит-базальты
(п
=
0,17—0,21);
86—
щелочные
базанит-базаль-
ты
(п > 0,21); 8в — лунные
базанит-базальты
(а > 0,400); 8г
"
толеитовые базанит-базальты; 8д — пикритовые базанит-базаль-
ты; 9 —
базанитоиды
(s,
1
);
9а
—
умереннощелочные
оливиновые
базаниты
(«щелочные оливиновые базальты» океанов), п —
0,10'
0,13;
9б~
трахибазаниты
(п =
0,13—0,17);
9в — щелочные базани-
ты (п >
0,17);
9г —
пикритовые базаниты;
10
—
пикритоиды
(sfY*
Юа
—
коматииты
пикритовые,
меймечиты
и их интрузивные
ана-
логи;
106
—
пикриты;
10в и Юг — умереннощелочные
пикриты
(анкаромиты,
лимбургиты
и др.);
10д
~ щелочные пикриты
(не-
фелиниты,
авгититы
и др.), п =
0,13—0,30;
10е —
габбро-анорто
зиты
лунные;
10ж
— анортозиты лунные;
11
—
меймечитоиды
(s
а
4.
Использование
геохимических данных при
изучении
метаморфических пород
141
ц
а
- кимберлиты (а > 0,1,
/
= 0,25-0,45),
лерцолиты;
116
-
меймечиты;
lie
— перидотиты,
гарцбургиты,
дуниты,
серпенти-
и
иты,
малоглиноземистые меймечиты;
Иг—
щелочные меймечи-
тоиды
(нефелин-мелилитовые,
мелилитовые
и др.).
4.2. Диаграмма FAK
А. А. Предовский
[51]
предложил диаграмму FAK для рекон-
струкции первичного состава
метаморфизованных
алюмосиликат-
ных
магматических и осадочных пород, основанную на общих
чертах различий составов осадочных и магматических пород (рис.
4.3). Данная диаграмма имеет вид сдвоенной бинарной диаграммы
с координатами
KF
и AF, где
F—
фемичность породы, А — част-
ная глиноземистость, К — соотношение щелочей: F =
(Fe
2
O
3
+
+ FeO +
MgO)/SiO
2
;
A
-
А1
Э
О
3
~
(К
2
О
+
Na
3
O
+
СаО');
СаО'
=
= СаО —
CO.,
— поправка на карбонатность породы; К =
К,О
—
-
Na,O.
Все параметры рассчитывают в молекулярных количествах.
На диаграмме А. А. Предовского состав породы отображается
фигуративными точками в зонах
AFw
KF,
при этом поле
^/•'явля-
ется основным, а поле
KF
— вспомогательным и контрольным.
Следует иметь в виду, что диаграмма должна применяться только
в совокупности с комплексом геологических данных, а эффек-
тивность ее использования повышается при исследовании серии
анализов пород, а не единичных образцов. В пределах основных
зон диаграммы (KF
\\
AF)
на основе обработки большого количе-
ства опубликованных материалов и оригинальных данных (около
5000 анализов магматических пород, более 4000 анализов
немета-
морфизованных
и
слабометаморфизованных
и
1500
метаморфизо-
ванных осадочных пород) А. А. Предовский выделил поля пород
различного состава.
На диаграмме
FAK
наблюдается поле перекрытия кислых
кластогенных
алюмосиликатных
осадочных пород (субграувакк и
а
ркозов)
и магматических пород близкого им состава. Для их раз-
Деления А. А. Предовский предложил диаграмму в координатах
А1
2
0
3
И
(К
?
О
+
Na,O)
(рис. 4.4), основанную на том, что при разруше-
н
ии
кислых магматических пород продукты их разрушения {арко-
ЗЬ
0
всегда обогащаются кварцем. В 1996 г. Я. Э. Юдович [81] опуб-
ликовал
диаграмму для разделения метааркозов и метариолитов,
к
°торая
рассматривается ниже.
142
Ингерпретация
геохимических данных
K
;
O-Na
2
O
+я
-и-10'
-/НО'
.
•
.
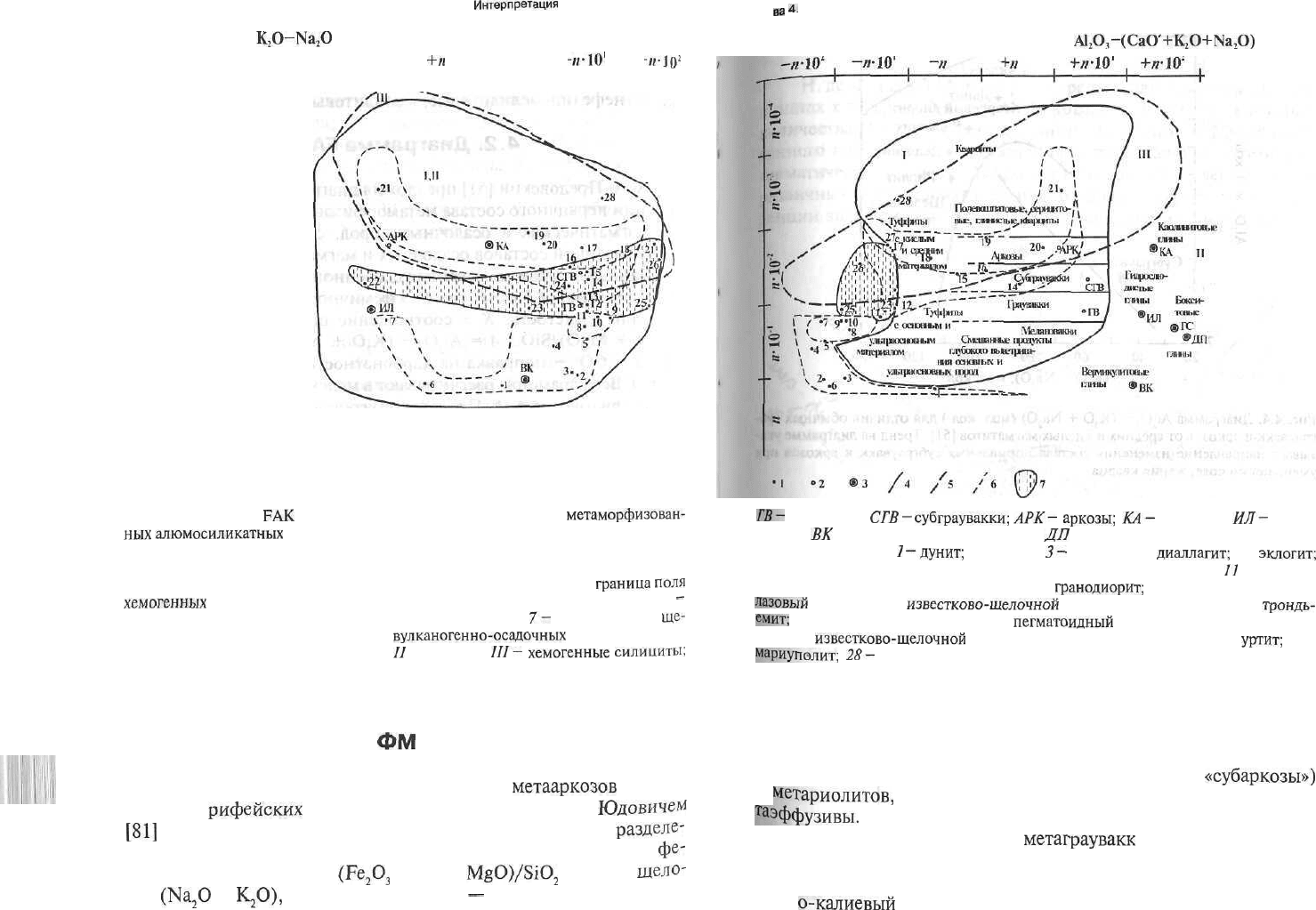
Рис. 4.3. Диаграмма
FAJC
для реконструкции первичного состава
метам
орфизован-
ных
алюмосиликатных
магматических и осадочных пород (Предовский, 1980):
точки составов: / — изверженные породы; 2 — осадочные породы; 3 — минералы;
4 — границы поля зернистых осадочных пород (в правой части диаграммы) и
объединенного поля обломочных пород и глин (в левой части); 5 —
граница
поля
хемогенных
силицитов; 6 — границы полей магматических пород (снизу вверх
-
ультраосновных, основных, средних и кислых, кислых);
7-
границы поля
ще-
лочных магматитов. Поля осадочных и
вулканогенно-осадочных
пород: / - зерни-
стые осадочные и смешанные породы;
//
— пелиты;
///—
хемогенные
силиииты;
•
4.3. Диаграмма
ФМ
- сумма щелочей
На основе петрохимического изучения
метааркозов
и мета-
риолитов
рифейских
толщ Приполярного Урала Я. Э.
Юденичем
[81]
была предложена общая модульная диаграмма для
разделе-
ния этих пород (рис. 4.5). Диаграмма строится в координатах:
ф
е
'
мический модуль ФМ =
(Fe
2
O
3
+ FeO +
MgO)/SiO
2
— сумма
щел°'
чей
(Na
2
O
+
К
2
О),
содержания оксидов
—
в массовых процентах.
аа
д.
Использование геохимических данных при изучении метаморфических пород
AIA-(CaO'+K
2
O+Na,O)
•А
143
,
ГВ-
граувакки;
СГВ-
субграувакки;
АРК~
аркозы;
КА~
каолинит;
ИЛ~
гидро-
слюды;
ВК
— вермикулит; ГС — гиббсит;
ДП
— диаспор. Точки средних составов
изверженных пород:
/
—дунит;
2— верлит;
3—
пикрит; 4 —
диаллагит;
5—
эклогит;
б— кимберлит; 7— лейцитит; 8— габбро; 9— спилит; 10— эссексит;
//
— бесквар-
цевый диорит; 12 - кварцевый диорит; 13 —
гранодиорит;
14 — дацит; 15 — олигок-
лазовый
гранит; 16 —
известково-щелочной
гранит; 17— комендит; 18—
трондь-
емит;
19 - аплит; 20 - риолит; 21 —
пегматоидный
гранит; 22 — витербит; 23 —
средний
известково-щелочной
сиенит; 24 — трахит; 25 — луяврит; 26 —
уртит;
27—
мариуполит;
28—
анортозит
На диаграмме выделены поля метааркозов (включая
«субаркозы»)
и
Метариолитов,
под которыми авторы понимают все кислые ме-
таэффузивы.
Кроме того, для сравнения на диаграмме пунктир-
линиями показаны поля
метаграувакк
и кварцитов, однако
их диагностики Я. Э. Юдович предлагает использовать диаг-
в координатах ГМ (глиноземистый модуль) - НКМ (на-
о-калиевый
модуль). Более подробное описание модулей при-
144
Интерпретация
геохимических
дац
Н
ы
170
150
130
90
70
+Андезит
+ Дацит
+
Кварцевый диорит
+
Риодацит
+ Делленит
+ Риолит
Щелочные
граниты
Субграувакк
*
20 40 60 80 100 120 140
(К,О + Na,O), мол. кол.
1
7
2
"
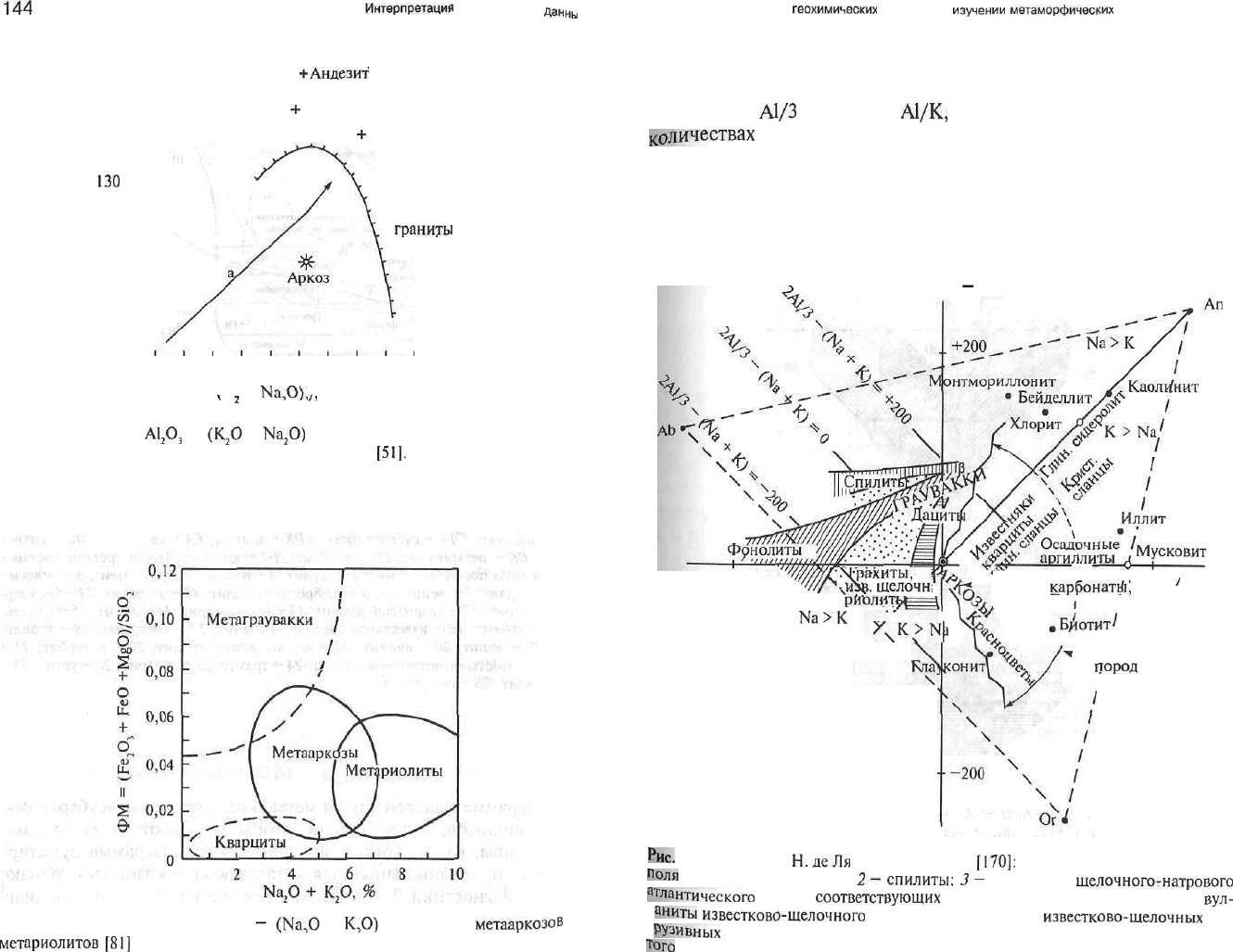
Рис. 4.4. Диаграмма
А1
2
О
3
—
(К
2
О
+
Na
;
0)
(мол. кол.) для отличия обычных суб-
граувакк и аркозов от средних и кислых магматитов
[51].
Тренд на диаграмме ука-
зывает направление изменения состава нормальных субграувакк и аркозов при
уменьшении содержания кварца
i
i
Рис. 4.5. Модульная диаграмма ФМ
-
(Na,O
+
К,О)
для отличия
метааркозов
И
метариолитов
[81]
лава 4. Использование
геохимических
данных при
изучении
метаморфических
пород
1 45
4.4. Диаграмма Н. де Ля Роша и М. Рубо
Н. де Ля Рош и М. Рубо [170] предложили диаграмму в коор-
динатах х —
А1/3
— Na, у =
А1/К,
которые рассчитаны в атомных
количествах
(рис. 4.6). На основании различного дифференциро-
ванного геохимического поведения натрия, калия и алюминия в
магматических и осадочных процессах на диаграмме выделены поля
различных типов магматических и осадочных пород, а также тен-
денции эволюции составов вулканических и осадочных серий.
А1/3
-
К
-200
^N-рахиты,
\ЙЭ6.
щелочи;
рйолит.
№>К
-VONb
\
Кварц,
карбонатш;
'
оксиды Fe
,
/
,Биотит/
-»
Сектор осадочных
пород
р
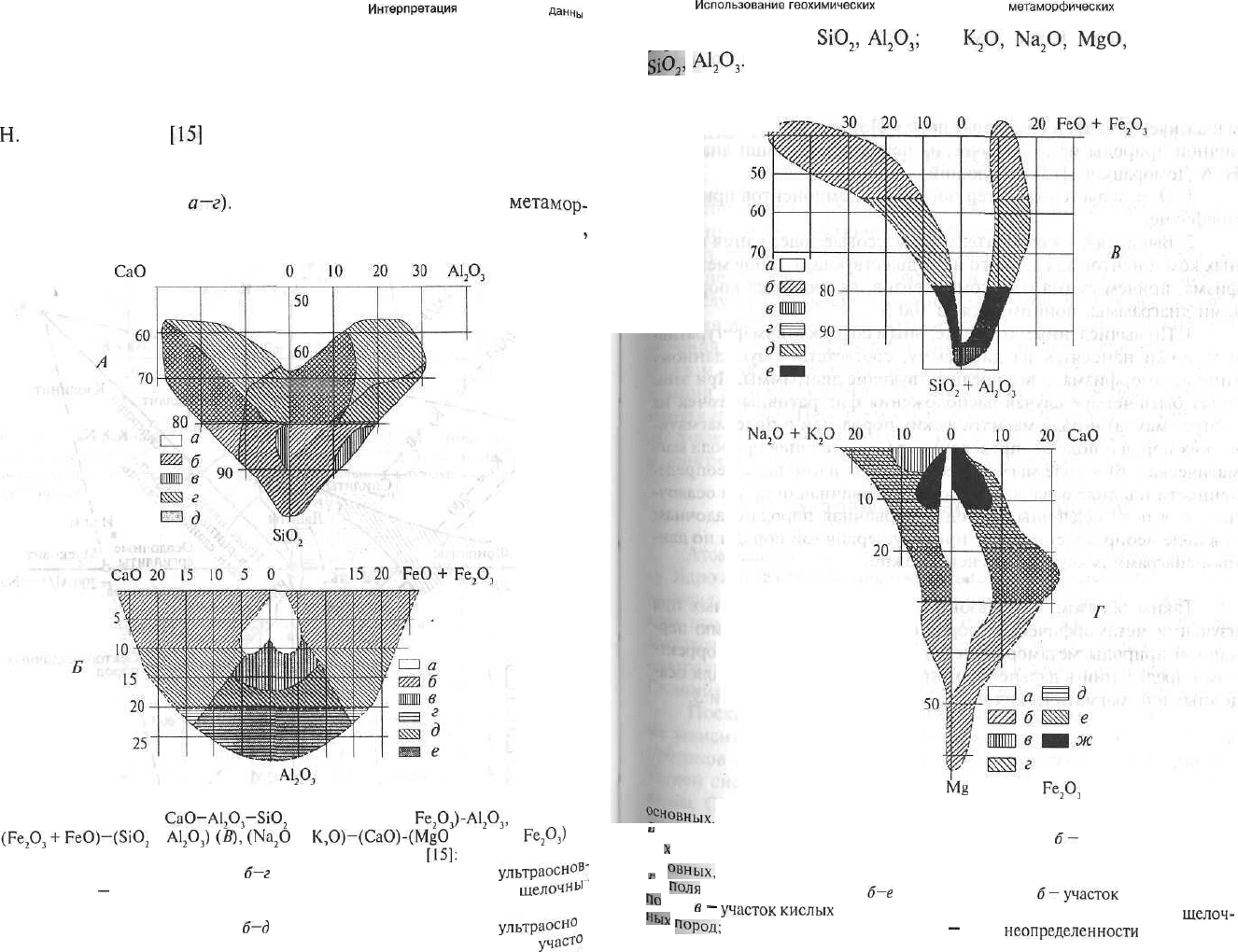
ис.
4.6. Диаграмма
Н.деЛя
Роша и М. Рубо
[170]:
п
оля
составов: / - базальты;
2-
спилиты;
3—
вулканиты
щелочного-натрового
а
тлантического
типа (и
соответствующих
щелочных интрузивных пород); 4—
вул-
а
ниты
известково-щелочного
тихоокеанского типа (и
известково-щелочных
ин-
Рузивных
пород); 5 — вулканиты промежуточного типа (и интрузивных пород
т
°го же состава)
146
Интерпретация
геохимических
данны
4,
Использование
геохимических
данных при изучении
метаморфических
пород
147
4.5. Диаграммы Н. А. Доморацкого
Для выяснения первичной природы метаморфических пород
Н.
А. Доморацкий
[15]
предложил серию диаграмм в координатах,
учитывающих ряды подвижности компонентов [24] и типы мета-
морфизма, характеризующиеся определенными инертными ком-
понентами (рис. 4.7,
а—г).
Всего им выделено пять типов
метамор-
физма, при которых инертными компонентами являются: /— SiO
,
СаО
30
20 10
5 10
1520
FeO
+
Fe
;
O
3
Рис. 4.7. Диаграммы
CaO-A!
2
O
3
-SiO
2
(A), CaO-FeO +
Ре
2
О
3
)-А1
2
О
3
,
(Б),
(Fe
2
O
3
+
FeO)-(SiO
2
+
А1
2
0
3
)
(Я),
(Na
2
O
+
K,O)-(CaO)-(MgO
+ FeO +
Fe
2
O
3
)
(
для выяснения первичной природы магматических пород
[15]:
А — поля пород: а - осадочных;
б—г
~ магматических; б — участок
ультраосноБ'
ных пород: в
-
участок кислых пород; г - участок основных, средних и
щелочнЫ
пород; д ~ поле неопределенности;
Б — поля пород: а - осадочных;
б—д
— магматических: б — участок
ультраосно
ных пород; в — участок кислых пород; г — участок щелочных пород; д -
участ°
), СаО,
Si0
2
,
A1
2
0
3
;
У-
К
3
О,
Na
3
O,
MgO,
FeO, СаО,
*>j6
2
,
А1
2
О
Г
Поля составов магматических и осадочных пород на
диаграммах нанесены с учетом обработки большого количества
MgO
30
40
•
Mg
+ FeO + Fe
2
O
3
средних и щелочных пород; е - поле неопределенности;
"
поля пород: а - осадочных; б—д — магматических:
6-
участок ультраоснов-
*
пород; в - участок кислых пород; г - участок щелочных пород; д - участок
^
°
в
ных,
средних и щелочных пород; е — поле неопределенности;
По
Поля
пород:
а -
осадочных;
б~е
—
магматических:
б-участок
ультраосновных
«Ых
в
~~
участок
кислы
х
пород;
г -
участок основных пород;
д -
участок
щелоч-
пород;
в - участок средних пород; ж
~
поле
неопределенности

148
Интерпретация
геохимических
данных
материала. Всего на диаграммах выделяются три поля: поле магма-
тических пород с участками ультраосновного, основного, сред-
него, кислого и щелочного составов; поле осадочных пород и поле
неопределенности, где располагаются фигуративные точки как
магматических, так и осадочных пород. Порядок определения пер-
вичной природы метаморфических пород при помощи диаграмм
Н. А. Доморацкого [15] следующий:
1. Определяется характер поведения компонентов при
мета-
морфизме.
2. Вычисляются относительные массовые содержания инерт-
ных компонентов для данного и предшествующих типов метамор-
физма, причем сумма всех компонентов, являющихся координа-
тами диаграммы, принимается за 100
%.
3. По вычисленным относительным содержаниям фигуратив-
ные точки наносятся на диаграмму, соответствующую данному
типу метаморфизма, и все предшествующие диаграммы. При этом
могут быть четыре случая расположения фигуративных точек на
диаграммах: а) в поле магматических пород или в поле магмати-
ческих пород и поле неопределенности — первичная природа маг-
матическая; б) в поле магматических пород или в поле неопреде-
ленности и в поле осадочных пород — первичная природа осадоч-
ная; в) в поле осадочных пород — первичная порода осадочная;
г) в поле неопределенности — природу первичной породы
подан-
ным диаграммам определить невозможно.
* *
Таким образом, использование геохимических данных при
изучении метаморфических пород сводится к определению пер-
вичной природы метаморфизуемого субстрата. При его коррект-
ном определении в дальнейшем применяются методики для оса-
дочных или магматических пород, рассмотренные в гл. 2 и 3.
|
Глава 5. ИСПОЛЬЗОВАНИЕ РАДИОГЕННЫХ
ИЗОТОПОВ
Использование радиогенных изотопов в геологии основано
на
принципе
радиоактивного превращения элементов. Поскольку
скорость радиоактивного распада является постоянной величи-
ной и не зависит от температуры и давления, то этот процесс
может служить в качестве геологических часов. В то же время соот-
ношения изотопов некоторых элементов чрезвычайно важны для
решения вопросов образования пород различного генезиса. Таким
образом, в целом выделяются два основных направления исполь-
зования радиогенных изотопов: абсолютная геохронология и изо-
топная
геохимия.
Перед тем как перейти к рассмотрению этих двух
направлений следует кратко остановиться на базовых принципах
и понятиях, а также на аналитических методах.
.
5.1.
Базовые принципы и понятия
Атом каждого элемента включает ядро и электронную оболоч-
ку. Ядро атома сложено положительно заряженными частицами —
протонами и незаряженными частицами — нейтронами. В состав
ядра входят также ряд других элементарных частиц, но для нас
Достаточна упрощенная модель. В атоме, находящемся в электро-
нейтральном состоянии, число протонов и электронов одинаково.
Синонимом атома является термин нуклид (от лат. нуклеус — ядро).
Поскольку масса покоя электрона очень мала, то масса ато-
ма
зависит от числа протонов
(Z)
и нейтронов
(N)
в ядре. Число
^ротонов
соответствует атомному номеру элемента в Периоди-
ческой
системе элементов Д. И. Менделеева и определяет заряд
ат
ома.
Сумма протонов и нейтронов называется массовым числом.
большинство
химических элементов имеют различное число ней-
ронов
в ядре и, следовательно, характеризуются различными мас-
С
°БЫМИ
числами. Различные массовые числа одного
и
того
же
эле-
^
е
нта
называются изотопами (от греч. то же
место,
поскольку
^И
находятся на одном и том же месте в Периодической системе
^Ментов).
150
Интерпретация
геохимически
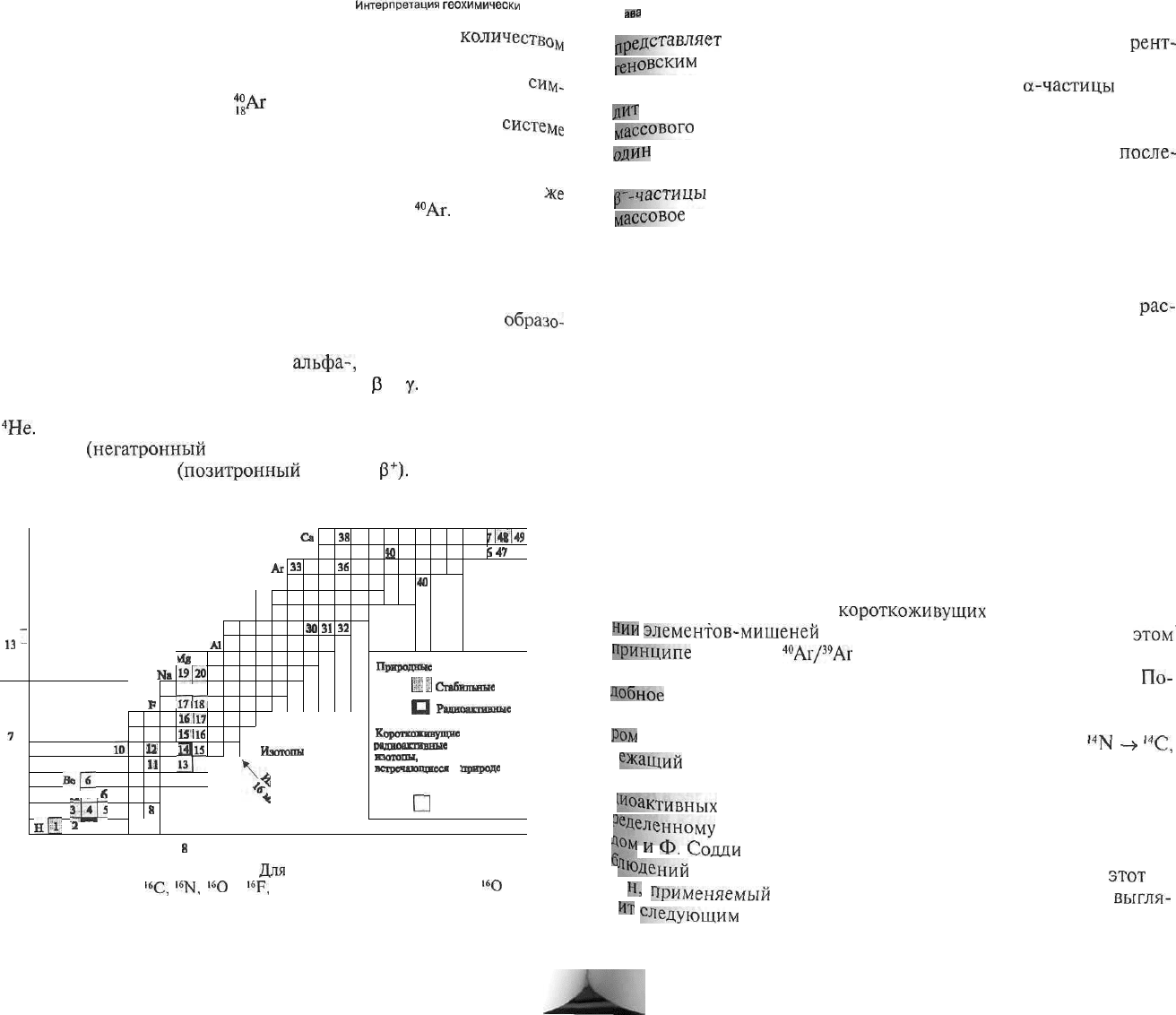
Атомы одной и той же массы, но с различным
количество^
протонов называются изобарами. Рис. 5.1 дает наглядный пример
изотопов и изобар. Для удобства строение атома записывается
сим-
волами. Например, запись
^JAr
означает, что данный изотоп явля-
ется атомом аргона (порядковый номер в Периодической
системе
элементов Д. И. Менделеева 18) с массовым числом 40, т.е. он
имеет в своем составе 22 нейтрона. Так как у всех изотопов одного
и того же элемента число протонов остается постоянным, ту
ж
е
запись можно сделать в более краткой форме —
40
Аг.
Всего известно около 1700 изотопов, из которых только 264
являются стабильными. Ядра неустойчивых атомов самопроизволь-
но распадаются до тех пор, пока не достигнут стабильной формы.
Такой самопроизвольный распад, сопровождающийся эмиссией
различных частиц, излучением энергии и приводящий к
образо-
ванию новых атомов, называется радиоактивностью. В зависимос-
ти от типа излучения выделяется
альфа-,
бета- и гамма-радиоак-
тивность, обозначаемые соответственно а,
[3
и
у.
Альфа-частицы
представляют собой один атом гелия с зарядом 2 и массой 4, т.е.
4
Не.
Бета-частицы идентичны электронам в случае отрицательно-
го заряда
(негатронный
распад, р~) и позитронам в случае поло-
жительного заряда
(позитронный
распад,
р
+
).
Гамма-излучение
19 -
~
17 -
15 -
13
:
11 -
9 -
7
-
3 -
1 -
' 1
N&
О
N
С 9
W
В 8 9
BojT 7 71
Li 5
*
Т
не aUJs 6
н|'1-
а
И
№
р
13
12
11
10
9
8
14
13
U
11
10
9
К
17
16
15
14
13
12
11
S
Р
Si
А1
•IB
[21
щ»
18 19
ТтКГ
1617
15116
Н|15
ш~
HI
22
21
20
19
18
17
16
25
24
23
22
21
20
19
18
*
26
25
24
23
22
21
20
\
•
Аг
а
29
28
27
26
23
24
23
22
30
29
2В
27
26
25
24
Са
К
33
32
31
30
29
28
27
26
34
33
32
31
30
29
28
37
36
35
34
33
32
31
30
38
37
36
35
34
33
32
39
38
37
36
35
34
Изотопы
углерода
40
39
38
37
36
41
W
39
38
37
42
41
40
39
38
43
42
41
40
44
43
42
45
44
43
464
45 +
7«|49
6
47
Природные
изотопы
L
J
Стабильные
Q
Радиоаиивнне
Короткожявущис
радиоактивные
изотопы,
не
встречающиеся
в
природе
О
О 2 4 6
В
10 12 14 16 18 20 22 24 26 28
Рис. 5.1. Фрагмент таблицы атомов.
Идя
примера стрелками показаны изотоп
углерода и изобары
|6
С,
I6
N,
'Ю
и
L6
F,
среди которых только изотоп
|6
О
являет
стабильным и представлен в природе в значительном количестве
авэ
5. Использование радиогенных изотопов
151
Представляет
собой электромагнитное излучение, подобное
рент-
геновским
лучам.
При альфа-распаде каждая эмиссия одной
а-частицы
приво-
дит
к уменьшению атомного номера на две единицы и снижению
массового
числа на четыре единицы. При негатронном распаде
О
дцн
нейтрон превращается в протон и электрон, причем
после-
дний выбрасывается из ядра. Следовательно, при эманации одной
р--частицы
атомный номер увеличивается на одну единицу, а
массовое
число остается прежним. При позитронном распаде, на-
оборот, сокращается на одну единицу число протонов в атоме, а
число нейтронов увеличивается на единицу, т.е. массовое число
остается постоянным. Отдельно выделяется радиоактивный рас-
пад в результате захвата орбитального электрона. При таком
рас-
паде, как следует из названия, один электрон внутренней обо-
лочки атома захватывается ядром, при этом происходит анниги-
ляция позитрона и электрона, сопровождающаяся образованием
одного нейтрона и нейтрино. Нейтрино покидает атом. Соответ-
ственно, как и при позитронном распаде, число протонов в ядре
сокращается на единицу, а массовое число остается прежним. После
радиоактивного распада атом обычно находится в возбужденном
состоянии и переходит в основное состояние, сопровождается гам-
ма-излучением.
Бомбардировка атомов стабильных изотопов различными
частицами, такими как протоны, нейтроны, а-частицы и др.,
может привести к тому, что стабильный изотоп перейдет в неста-
бильное состояние. Это явление хорошо известно и широко ис-
пользуется для получения
короткоживущих
изотопов при облуче-
нии
элементов-мишеней
в ядерном реакторе. Например, на
этом'
принципе
основан
40
Аг/
39
Аг
метод датирования, который будет
Рассмотрен более детально в одном из последующих разделов.
По-
Лобное
преобразование атомов происходит и в природе под воз-
Действием космического излучения. Наиболее известным приме-
ром
такого преобразования в природе является переход
14
N
->
14
С,
е
жащий
в основе радиоуглеродного метода датирования.
Независимо от вида радиоактивного распада, скорость ра-
1и
°активных
превращений нестабильных атомов подчиняется оп-
^Деленному
закону, который был сформулирован Е. Резерфор-
б
°
м
и
Ф-
Содди
в 1902 г. [76] в результате экспериментальных на-
Л|
°дений
активности солей тория. В окончательном виде
этот
за-
Н
'
применяемый
для целей абсолютной геохронологии,
выгля-
Ит
следующим
образом:
152
Интерпретация
геохимических
5.
Использование
радиогенных
изотопов
153
где
D/P
— отношение дочернего к материнскому изотопу в
насто.
ящий момент времени;
X
— постоянная радиоактивного распада
материнского изотопа; t ~ время. Дочерний изотоп
по-другому
называется радиогенным, так как он образовался в результате
ра-
диоактивного распада.
Для определения длительности протекания процесса
выра-
жение (5.1) может быть переписано в следующем виде:
1).
(5.2)
Из уравнения (5.2) видно, что для того, чтобы определить
возраст какого-либо минерала или горной породы, необходимо
знать два параметра: 1) соотношение дочернего и материнского
изотопов; 2) постоянную распада материнского изотопа. Первый
параметр является уникальным для каждого исследуемого образ-
ца и зависит от начальной концентрации материнского вещества
и времени. Соотношение дочернего и материнского изотопов из-
меряется масс-спектрометрическим методом, принцип которого
будет кратко охарактеризован в следующем разделе. Второй пара-
метр является характеристикой радиоизотопной системы.
Обычно используется еще один параметр, называющийся
периодом полураспада
(Г
1/2
).
Период полураспада соответствует вре-
мени, за которое количество материнского изотопа сокращается
вдвое. Постоянная распада обратно пропорциональна периоду
полураспада
Г
1/2
-1п(2)Д.
(5-3)
Поскольку периоды полураспада большинства
радиоактив-
ных изотопов, применяемых в геохронологии, очень велики, то
их определение сопряжено с определенными трудностями. Долгое
время многие лаборатории пользовались различными константа-
ми, и, таким образом, прямое сопоставление получаемых
возра-
стов было невозможно. В 1976 г. на Международном геологическом
конгрессе в Сиднее была достигнута
договоренность
об использо-
вании одинаковых констант радиоактивности [230]. Далее в текст
и таблицах, где не оговорено дополнительно, приводятся
имени
эти константы.
С развитием масс-спектрометрической техники назрела на
сущная
потребность в уточнении констант распада многих
ко используемых в геохронологии радиоактивных изотопов.
На-
пример,
при современных исследованиях аналитическая точность
О
пределения
большинства изотопных отношений достигает 0,5 %
О
т
возраста
породы, а при специальных исследованиях — 0,1
%.
В
Т0
же время неопределенность в определении постоянных распа-
да,
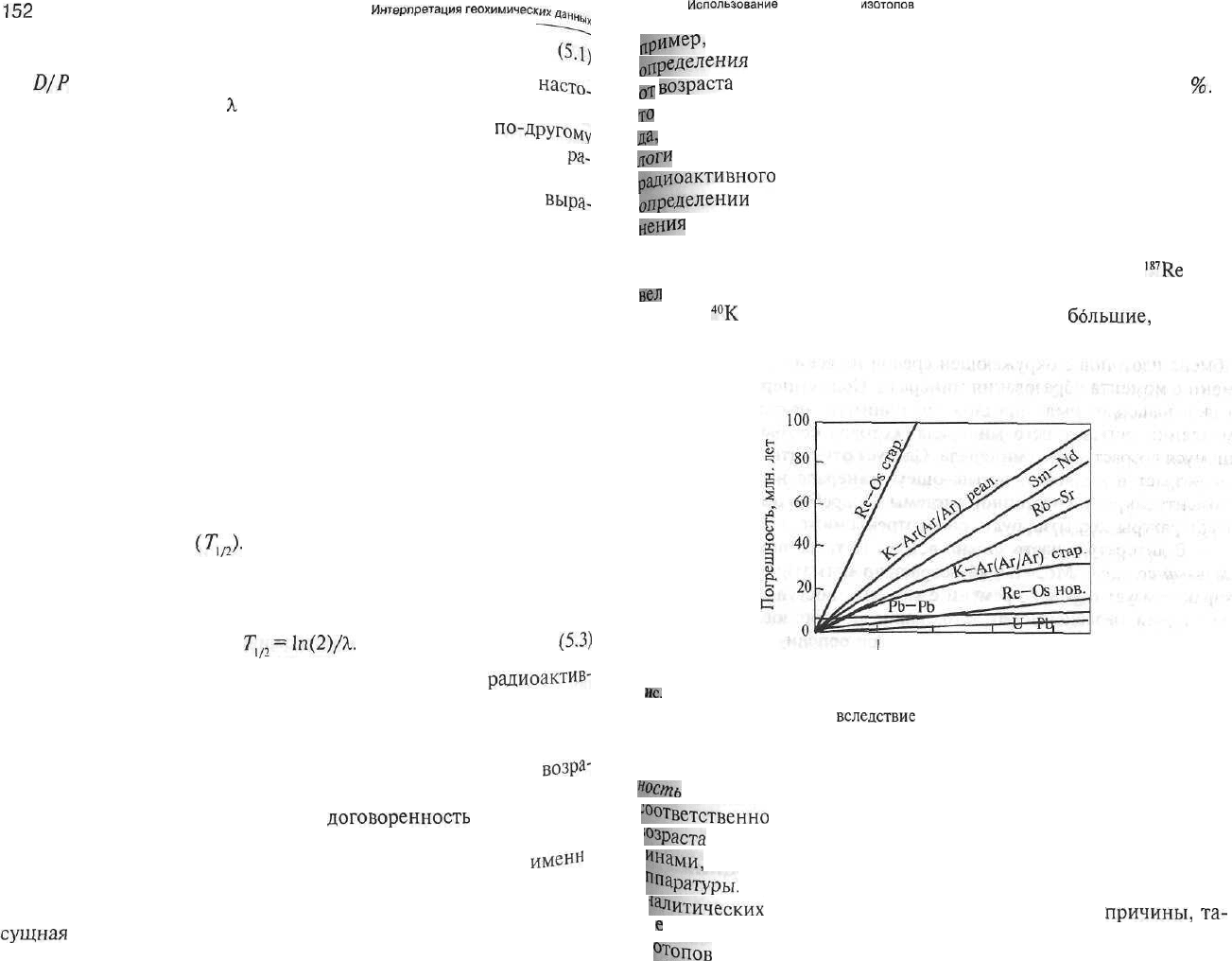
как правило, составляет несколько процентов. Более того, гео-
логи
и физики до сих пор пользуются различными константами
радиоактивного
распада [218]. На рис. 5.2 показано, как ошибка в
определении
возраста датируемого образца растет по мере удрев-
н
ения
в зависимости от неопределенности констант радиоактив-
ного распада. Наиболее известны константы радиоактивного рас-
пада урана. Пересмотр констант радиоактивного распада
IK7
Re
при-
вел
к их улучшению, тогда как новые константы радиоактивного
распада
40
К
указывают на более реалистические
ббльшие,
погреш-
ности. Рис. 5.2 модифицирован после П. Р. Ренне [218] с учетом
новых данных.
2 з
Возраст, млрд. лет
Ис
-
5.2. Зависимость погрешности при абсолютном датировании от возраста да-
тирования объекта (растет
вследствие
неопределенности определения констант
Радиоактивности)
Наиболее часто встречающимися являются два понятия: точ-
ность
и погрешность измерения возраста (в английском варианте
^ответственно
precision и accuracy). Под точностью измерения
'°
3
Раста
понимают ошибку, связанную с аналитическими при-
Инами,
такими как, например, чувствительность измерительной
"Паратуры.
В расчет погрешности определения возраста, помимо
1а
литических
причин, включаются геологические
причины,
та-
6
как неоднородность образца, частичное перераспределение
°
т
опов
и т.д. Таким образом, при чтении геологической литера-

154
Интерпретация геохимических
лэ
*"
5.
Использование радиогенных изотопов
155
туры, в которой используются абсолютные датировки,
нухц
0
обращать
внимание на то, что подразумевается под ошибкой в
определении возраста.
Следует остановиться на таких понятиях, как истинный воз-
раст, кажущийся
возраст,
закрытость
и температура
закрытия
изотопной системы. Под истинным возрастом породы (или мине-
рала) понимают промежуток времени между ее кристаллизацией
и настоящим временем. Очевидно, что измеренный возраст поро-
ды, т.е. рассчитанный по формуле (5.2) из измеренного
отноше-
ния материнского к дочернему изотопов, может не
соответство-
вать истинному возрасту породы. Такой измеренный возраст на-
зывается кажущимся. Если измеренный (кажущийся) и истинный
возрасты соответствуют друг
другу,
то это означает, что исследу-
емая изотопная система оставалась закрытой, т.е. не происходило
обмена изотопов с окружающей средой на всем промежутке
вре-
мени с момента образования минерала. Под температурой закры-
тия изначально было предложено понимать некую температуру
медленно остывающего минерала, которая соответствует кажу-
щемуся возрасту этого минерала. Следует отметить, что кажущий-
ся возраст в медленно остывающем минерале не соответствует
моменту закрытия изотопной системы. Подробно понятие и смысл
температуры закрытия будут рассмотрены ниже.
В литературе часто можно встретить такое понятие, как мо-
дельный возраст. Модельный возраст по магматическим породам
характеризует отрезок времени с момента поступления вещества
из мантии независимо от того, какие преобразования (плавле-
ние, метаморфизм и др.) эти породы претерпели в последующем.
По сути дела, модельный возраст не несет информации о возрас-
те самой исследуемой породы, а указывает на возраст
плавящего-^
ся субстрата или, по-другому, возраст
протолита.
Модельный
возраст по осадочным породам дает информацию о нижней воз-
растной границе размывавшихся
верхнекоровых
пород, в источ-
нике сноса осадочных бассейнов. В этом случае наряду с термином
возраст
протолита,
обычно используется другой термин
возрв
с
*
провинции.
5.2. Mace-спектрометрические измерения
Впервые
существование
изотопов было
экспериментальН
подтверждено Дж. Дж. Томпсоном в 1914 г., он анализировал
по"
ток заряженных частиц газообразного неона и обнаружил лини
интенсивности
20 и 22 масс. Несколько позже трудами
Ф.
В. Асто-
н
а
было положено начало новой области знания —
масс-спект-
ммемрии-
Прототипом современных масс-спектрометров являет-
ся конструкция, созданная в 1940 г. А. О. Ниром [76, 123]. Им же
были определены изотопные составы большинства природных эле-
ментов,
широко используемых сейчас в абсолютной геохро-
нологии.
.Масс-спектрометрические
измерения основываются на прин-
ципе
разделения потока движущихся заряженных частиц (ионов)
под действием силы Лоренца. Ускоренные в вакууме ионы,
про-
ходя через постоянное магнитное поле, начинают двигаться по
окружностям различного радиуса
(/•)
в зависимости от массы и
заряда иона:
fi
=
(m/e)2V/№,
(5.4)
•
где
т/е
— отношение массы иона к его заряду; V — потенциал
ионизации; Я — напряженность магнитного поля. Легкие массы
отклоняются больше, а тяжелые меньше.
На рис. 5.3 показана принципиальная схема масс-спектро-
метра секторного типа, иногда называемого
нировским
масс-спек-
трометром, он включает: 1) ионный источник, в котором проис-
ходит ионизация частиц и их ускорение под действием разности
потенциалов на катоде и фокусирующих пластинах; 2) трубу (ка-
меру) анализатора, проходящую сквозь постоянное магнитное
поле, создаваемое электромагнитом; 3) приемник ионов.
Из формулы (5.4) видно, что, зная геометрию трубы анали-
затора,
легко подобрать такие параметры ускоряющего напряже-
ния
(обычно несколько киловольт) и напряженности магнитного
поля, чтобы на коллектор попадали только ионы с необходимой
Электромагнит
Ионный
источник
°г
блока
Нап
Ряжения
м
v
\
К вакуумному
Катод
и система насосу
фокусирующих
пластин—«линз»
Приемник
- ионов
К
ком-
пьютеру
'3.
Схематическое изображение масс-спектрометра секторного типа

156
Интерпретация
геохимических
д
ан
g 5,
Использование
радиогенных изотопов
157
массой.
Для
исследования нескольких изотопов напряженность
маг~
нитного поля медленно изменяется и, таким образом, произво-
дится сканирование спектра масс. Масс-спектрометры с
одниц
коллектором называются сканирующими. Возможно также исполь-
зование нескольких коллекторов для одновременного приема ион-
ных пучков с различными массами. Такая система называется
мно~
гоканалъной.
При анализе изотопов газов, газовая фракция из анализи-
руемого образца выделяется отдельно, например, путем его плав-
ления в высоковакуумной печи. Затем выделившийся газ очища-
ется от примесей
активных
компонентов и вводится в ионный
источник. Система для анализа изотопного состава газов получила
название газового масс-спектрометра. Фотография комплекса для
выделения и последующего изотопного анализа благородных га-
зов и гелия при помощи сканирующего газового масс-спектро-
метра приведена на рис. 5.4.
•
Рис. 5.4. Сканирующий газовый масс-спектрометр
МАР-216,
приспособлен^
для
41)
Аг/*'Аг
датирования. Слева от электромагнита виден ионный источник,
которому через систему высоковакуумных вентилей присоединены:
ИОННЫЙ
сое
для поддержания высокого вакуума в камере анализатора (на переднем
не) и трубки,
идущие
от высоковакуумной печи и камеры лазерной абляции,
производится выделение газа из датируемого
образца
(находятся за
снимка).
Справа от магнита находится приемник ионов. Прибор установлен
^
боратории изотопной геохимии аргона фламандского Свободного
Брюсселя (снимок воспроизведен с
разрешения
доктора А. Бовена)
В случае изотопного анализа элемента, находящегося в твер-
дом
состоянии, этот элемент изначально выделяется в чистом виде
п
утем
химического разделения на
хроматографических
колонках.
Выделение
чистого элемента необходимо по ряду причин. Во-пер-
вых,
это делается для избежания изобарных наложений. Напри-
мер, самарий и неодим имеют общие изобары 144, 148 и 150 масс.
Во-вторых, присутствие других элементов может приводить к уве-
личению
потенциала ионизации и снижению стабильности изме-
рений. Выделенный чистый элемент наносится на катод ионного
источника.
Ионизация происходит в результате испарения веще-
ства при нагреве катода. Такая система получила название
масс-
спектрометра с термальной ионизацией (сокращенно TIMS, от англ.
thermal
ionisalion
mass spectrometer). Многоканальный масс-спект-
рометр с термальной ионизацией, предназначенный для
иссле-
дования изотопного состава стронция, неодима и свинца, пока-
зан на
рис.
5.5.
Во многих случаях необходимо знать не только изотопный
состав того или иного элемента, но и абсолютные количества рас-
сматриваемого состава. Для этого в пробу вносят известное коли-
чество того же элемента с известным изотопным составом. Такой
метод измерения концентраций вещества получил название изо-
топного разбавления. Следует отметить, что метод изотопного раз-
бавления является наиболее точным при определении малых ко-
личеств вещества.
При химическом выделении элементов предъявляют особые
требования к чистоте реагентов и
условиям
работы. Например,
Для изотопного анализа свинца в минералах с его низкой концен-
трацией
даже обыкновенный атмосферный воздух будет являться
загрязнителем,
ухудшая качество анализа и затрудняя интерпре-
тацию
полученных значений.
Чтобы избежать проблемы пробоподготовки, в настоящее
в
ремя
для изотопного анализа минералов широко используют
*
И|
Фозондовые
масс-спектрометры. В этом случае поверхность
"'Инерала
испаряется обычно при воздействии пучка отрицатель-
0
заряженных
атомов кислорода, после чего испаренную пробу
т
°РИчно
ионизируют и затем анализируют. В зависимости
оттех-
ческого
исполнения такая система называется:
масс-спектро-
^
т
Р
с вторичной ионизацией (сокращенно
SIMS,
от
англ.
Secondary
s Spectrometer) или чувствительный ионный зонд высокого
ия
(
сок
Р
а1
Д
е
нно
SHRIMP,
от
англ.
Sensitive
High
Resolution
icroProbe). Использование
микрозондовых
масс-спектромет-

158
Интерпретация
геохимических
с Использование радиогенных изотопов
159
Рис. 5.5. Многоканальный масс-спектрометр
Finnigan
MAT262, приспособленный
для анализа изотопов
стронция,
неодима и
свинца.
Слева от магнита
находится
источник ионов в виде камеры с барабаном,
содержащим
тринадцать катодов,
что позволяет анализировать до тринадцати проб без разгерметизации системы.
Снизу к ней прикреплен
турбомолекулярный
насос для поддержания высокого
иакуума.
Справа от магнита иидна камера с заключенными в нее приемниками
ионов. Прибор используется в рамках Центра коллективного пользования инсти-
тутов земной коры СО РАН, геохимии СО РАН и Бурятского геологического
института СО РАН
ров позволяет проводить датирование по единичным зернам
ми-
нералов и анализировать изотопный состав включений
микро-
ного размера.
Для изотопного анализа ряда элементов также
используй
современные модели (например — Element 2)
масс-спектр^
6
.
ров с
индуктивно
связанной
плазмой
(1CP-MS,
от
англ.
Inctiv
Coupled Plasma Mass
Spectrometer),
которые традиционно
няют при определении абсолютных концентраций широкого
тра микроэлементов.
.
v
Для изучения
космогенных
изотопов (см. ниже) применяют-
тандемные
масс-спектрометры с ускорителями (сокращенно
дМ5,
от англ. Accelerator Mass
Spectrometer).
В такой системе ион-
ыЙ
луч после разделения в магнитном поле ускоряется электри-
ческим
полем, а затем вновь разделяется во втором масс-спектро-
метре-
Это позволяет избежать изобарических перекрытий, что не-
возможно
сделать в обыкновенном масс-спектрометре. Например,
таким
способом отделяют
|4
С
от
I4
N
при радиоуглеродном датиро-
вании.
5.3. Методы абсолютной геохронологии
5.3.1-
Методы датирования, основанные на принципе
изохронных построений
(Rb-Sr,
Sm-Nd
и Re-Os)
В этом разделе рассмотрены три различных метода абсолют-
ной геохронологии, которые, однако, могут быть объединены,
поскольку в их основу положен один и тот же принцип изохрон-
ных построений. Для начала вернемся к формуле
(5.1),
переписав
ее в следующем виде:
,!
(5.5)
Поскольку гораздо удобнее иметь дело не с абсолютными
концентрациями, а с отношениями изотопов, правую и левую
части уравнения (5.5) нормируют по какому-нибудь стабильному
изотопу (5), концентрация которого в минерале остается неиз-
менной во времени:
(D/S)
=(P/S)
[exp(?J)
-
I].
(5.6)
v
'
'ЮМ
ч
'
'IIJM'
^
ч
'
На момент запуска радиоизотопных часов, например, после
к
РИсталлизации
минерала, система может характеризоваться не-
<им
количеством изотопа, идентичного дочернему изотопу, т. е.
-
^иэм
=
®pJS
+
(^/^ч-
В
связи
с
эти
м
выражение (5.6) должно
Ь]
ть
переписано следующим образом:
D
/S=(D/S)
+(P/S)
(ехрЯ.Г-1),
(5.7)
рад'
N
'
'
нич
ч
' 'HJM*
Индексы
«изм»
и
«нач»
соответствуют отношениям на момент
чепр.мма
по
прошествии времени
г
и в момент формирования си-
а индекс «рад» указывает на радиогенную
составляющую,
-j,
^равнение
(5.7) аналогично уравнению линейной регрессии
ШУ—a
+
bx.
Следовательно, если рассмотреть систему одновоз-
