Савицкий Е.Г.(ред). Благородные металлы
Подождите немного. Документ загружается.


тАБлицА
4.2в
упРугив
своиствА
БлАгоРоднь]х
мвтАллов
пРи
комнАтнои
твмпвРАтуРв
[9'
261]
!!ро0олоюенше
табл.
4.28
}1е-
талл
67
28
Р1
Аш
с,
[||а
173,2
81
с.
||]а
0,
36
о,42
485
447
Рц
ци
Ра
Ав
Аш
Р6
386,4
123,6
121
80
82
57о
172
153
51
27
29
220
214
0,31
0,
36
0,52
0,367
о
'37
0,28
0.28
тАБлицА 4.29
модуль
упРугости
монокРистАллов
БлАгоРоднь1х мвтАллов
пРи
комнАтнои
твмпвРАтуРв
[9'
262|
Ё'
|||а
Р0
Ав
|г
Ац
А6
Фв
1г
<ттт>|<110>|<100>
!87
115
662
114
129
81
,3
ц7
'4
81
65
43,5
42
тАБлицА 4'30
модуль
упРугости монокРистАллов
[262]
234,1
232,8
227,0
226,6
176,1
177,0
174,3
17б'2
7\,2
70,2
7о
'6
71
,5
-273
-
193
--\73
7
131,4
|24
'о
201
,6
97,3
93,4
169,7
51,
1
46,
1
45,4
-_2|
а
2о
-273
тАБлицА 4.31
мвхАничвскив
своиствА
БлАгоРоднь]х
мвтАллов
твхничвскои чистоть1
в
отожжвнном
состоянии
|9'
26|-264|
Рш
пь
Р0
Ав
Фз
|г
Р|
Ац
2000-3000
! 000-
1300
380-460
245_25о
3000-4000
\7оо_220о
390-420
22о-25о
500-600
400-560
180-200
!40-160
400-500
1 20- 160
120-130
350-400
70-
! 00
50-70
20-25
90-120
60-80
|0-2б
3-10
8-
15
25-35
40-50
0
6-10
40-50
45-50
2-3
20-25
80-85
80-95
0
10- 15
95-
100
90-9б
140
141
нц
ппа
2000
1000
7200
0
66,/т10&
0
4!,%
700
800
+00
800 7200
!,'с
+00
800 7200 1600
т"с
Рис"
4.25.
влияние
темпера-
турь| на твердость
(с
-
свер_
ху вниз: 1г'
&!'
Р[' Р6)'
прочность
(б)'
пластинность
@)
платиновь1х
металлов:
1_поликристалл; 2_мо-
нокристалл
70
20
30
+0
50
0
/000
800
000
+00
200
;\
\
€
\э
+00
ё;у,%
74
50
, +50
550 050
750
{,'с
Рпс. 4,26.
и3ме1'ение
пластичности
литого
серебра
в зависимости
от
температурь1
[29]
[пепень обжапая
,
"А
Руце. 4.27.
измене!1ие
твердости
ро-
дия,
иридия'
рутения
и осм!{я
в
3ависимости от
степени
об>кат;ля
[269]
А1[,
гпа
/',
/п'
|п
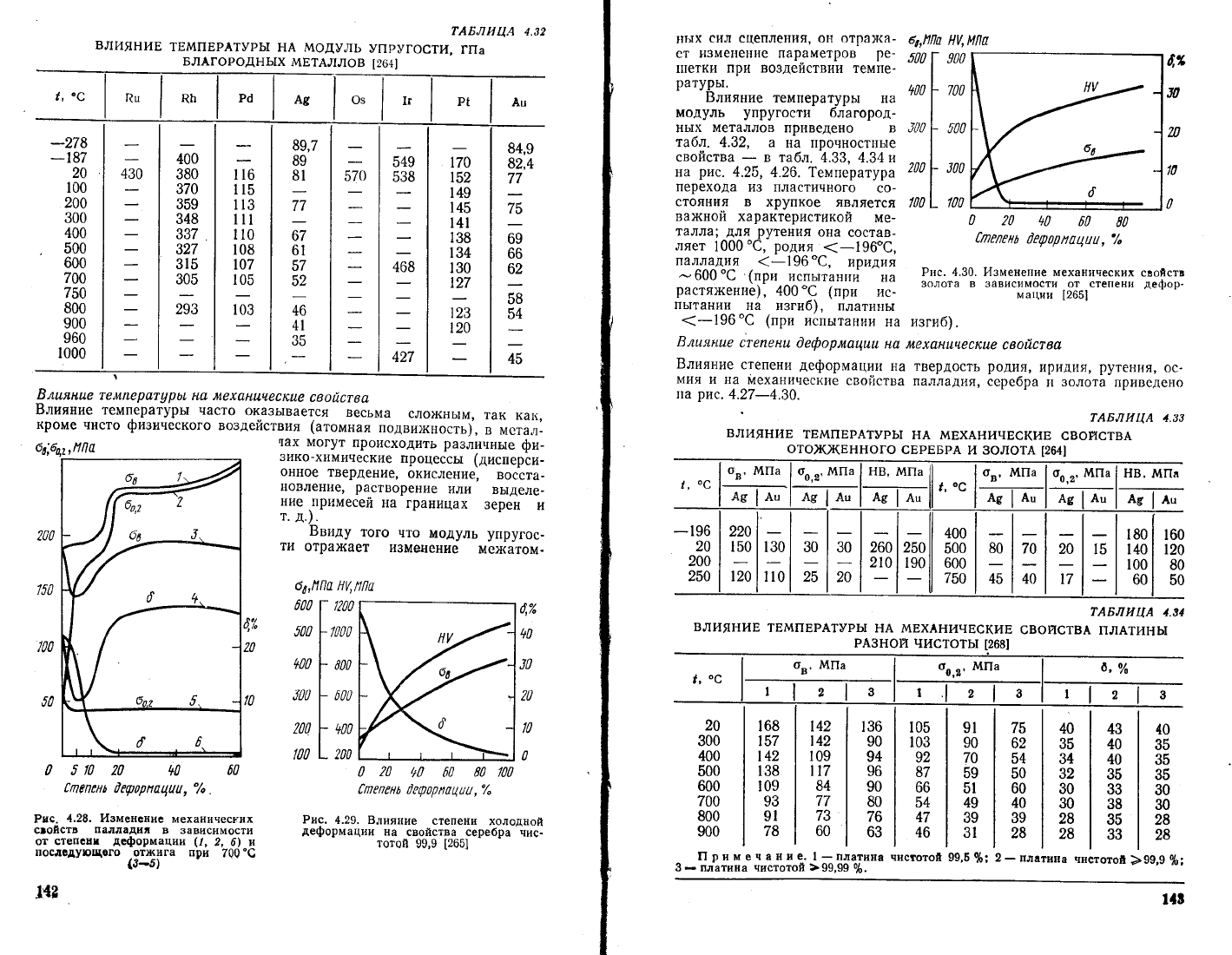
тАБл14цА
4.32
влиянив
твмпвРАтуРь|
нА модулБ
}||Р}|Ф6]!!,
||!а
БлАгоРоднь!х
мвтАллов
|264]
|'.с
-278
-187
20
100
200
300
400
500
600
700
750
800
900
960
1000
400
380
370
359
348
337
327
315
305
293
_
89,7
89
81
;
6?
61
б7
(о
Б
4\
35
468
427
84,9
82,4
77
45
75
69
66
62
тто
\52
149
145
141
138
134
130
127
123
у
Б лшянце
т е мпе
р
ат
! р
ь! на ме ханцце
с
к!!е
с в о
йст
в а
8лияние
температурь| часто
ока3ь|вается
весьма
сло)*(нь|м'
так
ка]{'
кроме
чисто
физинеского
воздействия (атомная
,одв'>кнос'ь1'
.
й.!',
||ах
могут
происходить
разлинные
фи_
3ико-химические
процессы
(дисперси_
онное
твердение'
окисление'
восста_
шовление'
растворение
или
вь1деле-
ние
'примесей
на
границах
зерен
11
т.
д.).
Бвиду
того
что
модуль
уг!ругос_
ти
отражает
и3ме||ение
ме){{атом.
6!,ппа н|/,плс
000
г
7200
4%
40
30
20
70
1000
800
400
+00
200
500
+00
,!00
200
100
|пепснь
0ерорпаццц,
о/о
.
Рис.,{.28.
и3менение
механичес}:их
с!ояств
палдади'
в 3ависимости
от степовп
деформации
(1'
2' 6| 1
послсдующого
отх<ига при
700
"€
(3-5)
1{2
0
20
+0 60
80 700
[пепень 0ерорпацша,%
Рис.
4.29.
3лияние
степени
холодпой
деформации
на
свойства серебра
нис_
тотой
99'9
[265]
510 20
'ть1х
сил с!|епления' он отра)|(а-
ет
изменен|{е параметров
ре-
ш|етки при воздействии темпе-
ратурь1.
Блияние
температурь|
на
модуль
упругости
благорол-
нь|х
металлов
пр|!ведено в
та6л.
4.32, а
на прочност|!ь|е
свойства
-
в табл.
4'33,
4.34и
на
рис.
4.25,
4.26. 1емпература
перехода
и3 пластичного
со_
стояния в
хрупкое является
ва>кной
характеристикой
ме-
талла;
для
рутения
она
состав-
ляет
1000
'€,
родия
<-196"с,
палл-адия
<-196
"с,
14ридия
-
600'€
'(при
испьттании
на
растя>кение),
400"€ (при
ис_
пьттании
на изгиб),
платит|ь!
<-|96
'€
(при
испь1тании
на
Блцянце
степенш
0еформацшш
на 7|ехан11цеск11е
свойства
Блияние
степени
Аеформациц
на твердость
ро^ия'
иР!4д|1я'
рутен'|я'
ос_
м|1я
и
на механичес!{ие
своЁ:ства
паллад\4я'
серебра
и
3олота
приведе}!о
||а
рис'
427-4.3о.
6''ппа
ну'|,!п|!
500
г
900
020+060а0
[пепень
0ерорпаццц|'ь
Рис. 4.30. изменет|ие механттческих
свойств
золота в 3ависимости
от степени
дефор_
ма1!ии
[265|
изгиб).
с%
10
п
10
700
500
300
100
+00
300
200
100
43
40
40
35
33
38
35
33
тАБлицА
,!.33
'л^янивтвмпвРАтуРь1
нА мвхАничвскив
своиствА
260
21о
400
500
600
75о
'в0
{
140 !
100 [
''!
160
\20
80
50
-п
25011
уш
40
35
.'о
бо
30
30
28
28
тАБлицА
1.34
влияниЁ
твмпвРАтуРь|
нА мвхАничвскив
своиствА
плАтинь!
РА3нои
чистоть|
[268|
о"' 1т1|1а
о0,2' мпа
6,%
|'
"с
2о
300
400
500
600
700
800
900
!68
157
142
138
109
93
9|
78
142
142
!09
117
84
77
73
60
105
103
оо
87
66
54
47
46
40
35
34
32
30
30
28
28
91
90
то
59
51
49
39
31
136
90
94
96
90
80
|о
63
75
62
54
50
60
4о
39
28
!|
р
и м е
ч а н и
е.
1
_платипа
чистотой
3
-
платина чистотой
>99'99
06.
99,6
%;
2
_
плати[|а
чистотой
>99,9 %;
отожжвнного
свРвБРА
и
3олотА
[264]
о0'2' мпа
Ё8, /у1|[а
1] {
о",
й||а
1|,

Рекрпсталлнзацля
Рекристаллизац|1я_восстановление
структурь|
и свойств
деформиро-
ванного
металла
при нагреве 3а счет
образования
и
роста
новь|х зерен.
5ависит
от чистоть|
материала' степени'
схемь!
и скорости
деформашии,
температурь1
!1 продол)китель}1ости
отжига или нагрева
(в
слунае
горя-
пей
деформации).
Разлинают первичную
рекристалли3ацию'
при кото-
рой
новь:е
растущие
3ерна
полг1остью
поглощают
деформированньте,
и
вторичную
(или
еобирательную),
при которой
происходит
р6ст
новь:х
зерен.
1емпература
начала
рекристалли3ации
больши}|ства
технически
чисть!х
металлов составляет
0'4-0'5
?,'.
!{ем
чище металл'
тем
ниже
температура
.рекристалли3ации;
например,
3олото чистотой
99'999' под_
вергнутое
99,99
о/о_ной
деформации,
рекристалли3уется
при
комнатнот:т
температуре.
'
1емпература
рекристалл|1зац|1и'
оцененная
по полному
(100
0/6'но_
му)
восстановлению
исходной_твердости,
составляет:
Рп
"(99,9)
после
80%-ной
деформации^при
12{Ф_'€-1300'с,
1ч;
&}г
(99,5)
поёле
50о/о-ной
леф_ормашии
при
600"с-800'€,
1
н
[261].
пь
зонноочищенньтй'после
60_9о_ной
деф_ормации
-
600т,
1
н
[9.|;
Р6 (99,999)
холоднокатань:й
(90%)-600'с,1
н; А9
(99,995)
тяйутое
со
степенью
деформации
99
}6
после_от)кига
при 70"€
в
течение
1 н
дает
50
0/6-ньтй
возвра}
твер-
дости;
|г.^(9_9.,9)
после
теплой
60
о/о-ной
прокатки
при
500'€_
1+00"ё,
1
ч;
Р1
(99,9)
холоднокатаная (80
9')_600"с
0,2 ч;
Р|
(99,999)
после
такой_х<е-
степени
цРформации
-500"с,
0,2
ч;
Аш
(99,99)
холодноката-
::ое (90.у_о)^--290'9'
0'5
ч;
Аш
(99,999)
лри той
х<е степени
деформа-
ции
_
140
"с,
0'5 н
[3].
4.\2.
/хпмпческие
свойства
3лектронное
строен11е
атома
ш
хароктернь.е
степен!]
окшслен!1я
!,имические
свойства
соединений
благородньтх
металлов
во
многом
9пределяются
поло)кением
их
в
период:аческой
системе
элементов
А.
14. }1енделеева.
Фтчетливо
просле)кивается
сходство
свойств
многих
с-оединений
в одинаковь1х
степенях
окисления
в
триадах
Ре-&ш-Фэ,
€о_&}:-1г,
ш|-Ра-Р|,
(ш-А9_Аш
|27|,
272].
'пронность
Бй"зй_"
однотипнь!х
соединениях
в триадах'
как
правило'
растет
по
мере
роста
атомного
номера.
€
увелинением
атомного номера
растет устойни}ость
соединений
в
высших
степенях
окисления
и'
напротив'
по мере
3апол_
нения
/ орбиталей
в периоде
характер}|ь|
}!из!]]ие
степени
окисления
(табл.
4.35)'
например
в
ряду
&ц+Р1.:+Р(+Ая.
(1у)
(11|) (1]) (п
€посо6ьс
рас?воренця
Растворение
благородньтх металлов
необходимо
с
целью
их исполь3о_
вания в
форме разлиннь|х
соединений'
для
приготовления катали3аторов'
порошков
заданной
дисперсности'
получения
покрьттий
и
пленок' оксид_
ных материалов
для
электронной
техники'
в
аналитической
и
техноло_
гической
практике
и т.
д..
Б
табл.
4.36 привеАеньт наиболее широко
используемые
способьт
пеРеведения
аффинированных
порошков платиновь1х
металлов в
рас_
творьт
[273,
274].
Ёеобходимо
отметить'
что
скорость
и полнота
рас-
творения 3ависят
от
способа приготовления порошков'
их
дисперсности'
чистоть( металлов и
поверх11ости'
их
предварительной терминеской
и
144
тАБлицА 4.35
элвктРоннов
стРовнив АтомА
и вго хАРАктвРнь1в
ствпвни
окислвния
|27!_275|
|!одгруппа
элемент
электронное
строение атома
характернь|е
(встре-
ча1ощиеся)
степени
окисления
€о : 3674в9
с1]
.
301.04$1
441бв|
5466в2
4485з|
54?6з9
4а|о
5496з1
4а105$1
5а10651
|у(||' !|1'
|у'
у1!, у|}|)
|у'
у|
(1'
|||'
у'
у1|1)
1|
(0'
|у)
11'
1у
(0'
1|' 1у)
1
(0,
|!1)
1,||1
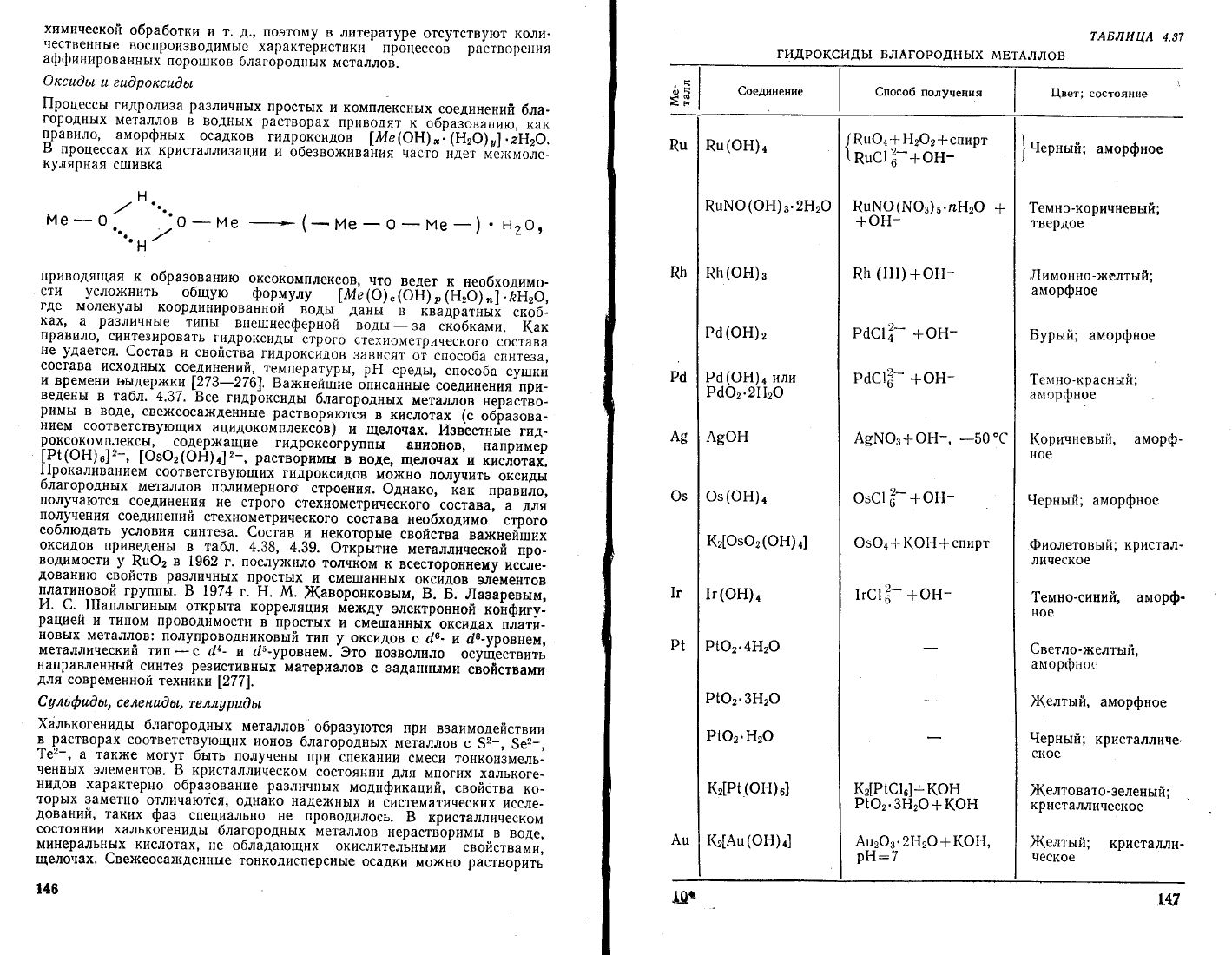
тАБлицА 1.36
спосоБьт
пвРвввдвния
в РАствоР АФФиниРовАннь1х
поРошков
'
БлАгоРоднь]х
мвтАллов
}1еталл
€пособ
переведения
в
раствор
Аш
А9, Аш
А9'
Р6
А9'
Р6'
Ап'
Р{
А9'
Р1-:*'
(п*,
!г*,
Фз**
Ац, Р1'
Р6,
([г*,
Фз*,
1г*,
&ш*
р1' Р0'
Аш'
&ц'
&|:
|г,
Фз
Р1' Р0'
Рц,
1{!т, !г' Фз
Р6'
&ш' &1'т'
1г' Фз' А9
*
частично
растворяется.
.*
9астично
растворя@тся
с
о6разованием ФзФа.
Фбработка хлорной
водой
или
раствором
тиомочевинь|
@бработка
раствором
цианида
или тиосуль-
фата
\а или
(
Фбработка
Ё\Ф3
Фбработка
шарской
водкой
Фбработка
дьтмящей
Ё25Ф1
Фбработка
конц.
}1(|*€!:
{лорирование (фторирование)
в присутст_
в[-1и
твердьтх
галогенидов
щелочнь]х
метал_
лов при 400-600"с
с последующим
рас-
творением
в кислотах
1,лорирование
(фторирование)
в
распла-
вах
галогенидов
щелочнь]х
металлов
с по_
следующим
растворением
в кислотах
€плавление
с оксидами
или
гидроксидами
целоч||ьтх
металлов
в присутствии
азотно-
кисль1х солей
при
500-900
'€
с последую_
щим
растворением
в кислотах
3лектрохимическос
анодное
растворение
10-688
14Б
химическо|]
обработки
и т.
д.,
поэтому
в литературе
отсутствуют
коли_
чественнь1е
воспро|!3водимь1е
характеристики
про!1ессов
растворе11ия
аффинированнь[х
поРо11]ков
6лагороднь|х
металлов.
Фксц0ьс
ш еш0роксш0ьс
|]роцессы
гидролиза
ра3личных
простых
и комплекснь|х
соединений
бла-
городных
металлов
в воднь1х
растворах
приводят
к
образоваг;ию,
ка!(
ър1'_'{9'
аморфнь:х
осадков
гилроксиАоЁ
|/т1е(Ф\1'1
")
(}!эФ)'1
.эЁ:Ф.
]'
процессах
их кристаллизац||и
и обезво>кивани9
1]3ц'1Ф
идег мсх(моле-
кулярная
сшивка
н
./
ме_о_
'о-ме
'о
'/
"н'
+(-м*-о_ме_).
наФ,
приводящая
к
образованию
оксокомплексов'
что
ведет
к
необходимо_
сти
усло}книть
общую
форуулу
[ле
(о)
"
(оЁ)
р
(н2б,;т:ай;б,
где
молекулы
координированной
-
воды
-
дайьт
в квадратйых
скоб_
ках'
а
ра3личнь|е
типь|
внешнесферной
водь|
-
за
скобками.
|(ак
правило'
син_те3ировать
тидроксидь|
строго
стехиометрического
состава
не
удается.
€остав
и свойства
гидроксйдов
3ависят
от способа
синте3а'
состава
исходных
соединений,-температурьт'
рЁ
среды,
способа
сушки
1
"-|:у-.""
в1дер}53
[273-2761.
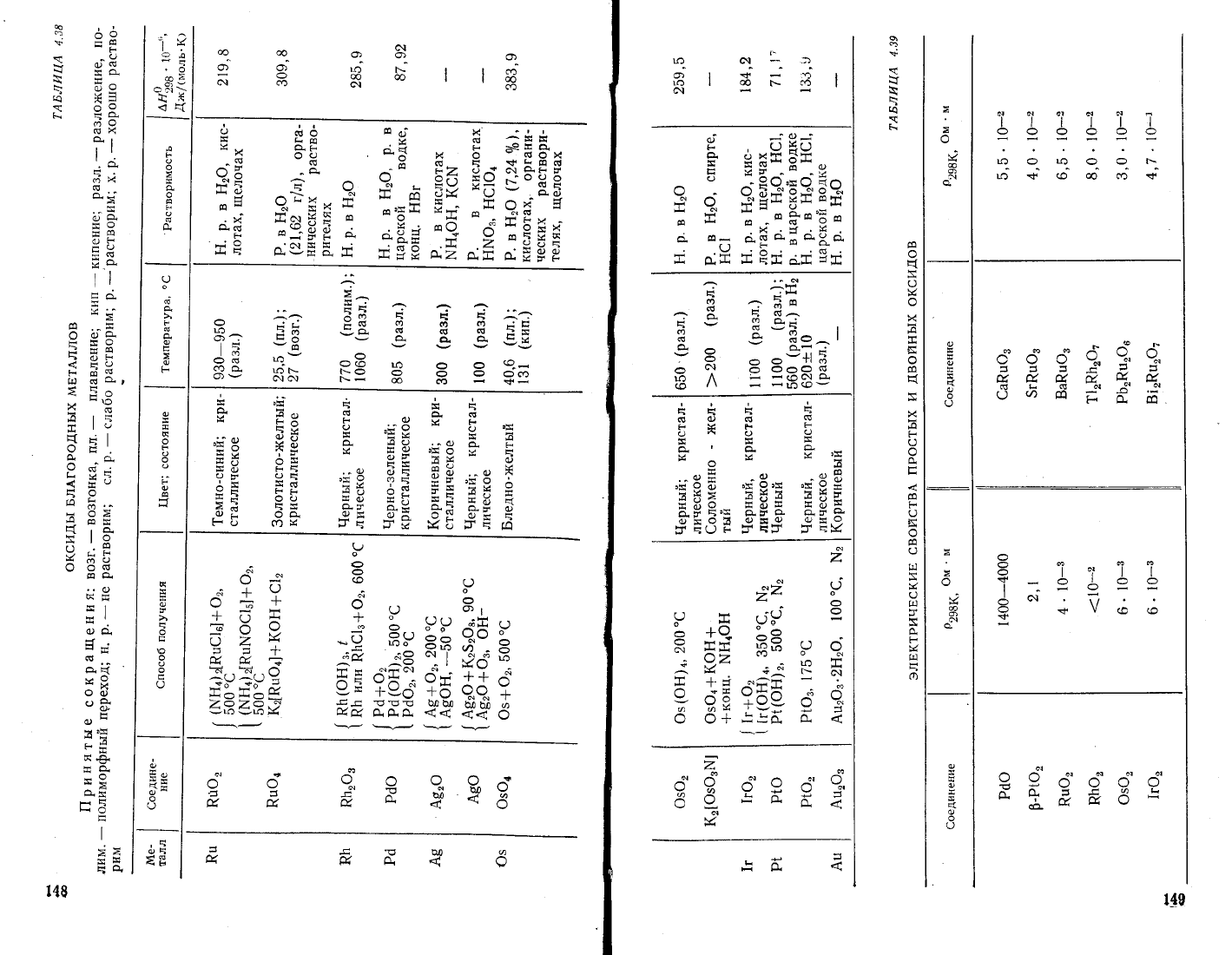
Бах<неййие
о}исанные
соединения
при-
ведены
в табл.
4.37. 3се
гидроксиды
благородных
металлов
нерастйо_
римы
в воде'
свех(еосах<денные
растворяютёя
в кислотах
(с
об!азова_
нием
соответствующих
ацидокомплексов)
и
щелочах.
|4звёстн*е
гид_
роксокомплексы'
содержащие
гидроксогруппы
анионов'
например
[Р1
(он)6.]'}-'
[о9о?(оЁ)1]'-,
растворимы
}"вод",
щелочах
и кислотах.
]-|рокаливанием
соответствующих
гидроксидов
можно
получить
оксиды
благородных
металлов
полимерного
строепия.
б';;-;'-;й
;й;;;",
получаются
соединения
не
строго
стехиометрического
состава'
а
для
получения
соединений
стехиометрического
соётава
необходимо'
с"рого
соблюдать
условия
синте3а.
€остав
и некоторые
свойств|'вах<нейййх
оксидов
прив_еде-нь!
в табл.
4.3в'
4.39.
Фткрытие
металлической
про-
водимости
у
&'пФ:
в
1962
г.
послух{ило
толчйом
к
всестороннему
иссле-
дованию
свойств
ра3личных
прость|х
и
смешанных
оксидов
элементов
платино'!ой
группь|.
в
1974
г.
Ё!. ;{.
)(аворонковым, 8.
Б.
лазарейый,
Р1.
€.
11]аплыгиным
открь!та
корреляция
йе>кду
электропной
й&йу-
рацией
и типом
проводимости
в простых
и смешанных
оксидах
плати_
новых
металлов:
полупроводниковь:й
тип
у
оксидов
е
ёв-
и 78_уровнем,
металлический
тип
_
с 7ц-
и 45_уровнем.
-3то
позволило
осуйёствить
направленный
синтез
резистивных
материалов
с заданными
сЁойствами
для
современной
техникн
|277).
€
ц
ль
фш0
ьо,
о е ле
нц0 ьо,
те ллу
рш0
ьь
[{лькогениды
благородньлх
металлов
образуются
при
в3аимодействии
в
растворах
соответствующих
ионов
благоролньлх
металлов
'
5:-,
$е2-,
|е'-'
а также
могу_т
0ыть получень!
при
спекании
смеси
тонкои3мель-
ченнь!х
элементов.
Б кристаллинеском
состоянии
для
многих
халькоге_
нидов
характерно
образование
ра3личнь:х
модификаций,
свойства
ко-
торь1х
3аметно
отличаются'
од!!ако
надех(нь|х
и систематических
иссле_
дований,
таких
фаз
специаль|{о
не проводилось.
Б
кристаллинеском
состоянии
халькогенидь!
благородньлх
металлов
нерастворимь|
в
воде'
минеральных кислотах'
не
обладающих
окислительнь:ми-
свойствами,
щелочах.
€ве:кеосажденнь|е
тонкод}|сперсные
осадки
мо)кпо
растворить
146
тАБлицА
4.37
гидРоксидь!
БлАгоРодг|ь1х
мвтАллов
.в!
э
ё
!
€оединение
|
€пособ
получения
|
[-1вет;
состоя'!ие
:Ё!
! !
&ц
}
нерны*;
аморфное
1ем но-коринневый;
твердое
.|1и
монно
->келтьтй;
аморфное
Бурьтй; аморфное
1ептно-красный;
ап,:орфное
|(оричтгевьтг],
аморф-
!1ернь:;};
аморфное
Фиолетовьтй;
кристал-
лическое
1емно_синий, аморф-
ное
€ветло-желть::!,
аморф:тос
}(елтый,
аморфное
9ерный;
кристалличе.
с|(ое
)|(елтовато
_зеленый;
кристаллическое
\елтьгй; кристалли-
ческое
&ц(9Ё)ц
&ц}ч{Ф(ФЁ)з.2[|эФ
|
&ц\@(\Фз)ь.аЁ:Ф
кп(он)3
Ра(он),
Р0
(Ф[1)ц
или
Рао2.2г]2о
А9ФЁ
Фз(Ф}1)1
(1[ФвФ9(Ф}|)1]
|г(Ф}!)а
Р{о2.4н2о
Р1о2.3н2о
Р{о2.н2о
к{Р{(он)6]
(:[Аш(он)ц]
ки
(|||)
+он-
Р0с|;*
+он_
Р6с1;-
+он_
Ав\Фз*Ф}|-,
_50'с
овс1
62_
+он-
ФзФ+-]-1(Ф}|*спирт
1гс!]-
+он_
к2[Р{с16]+кон
Р|о9.3н2о+кон
Аш:Фз. 21]:Ф
+
(ФЁ'
рн:7
!
ффо!ы
!1!..!-
о
Ф
-|
ффф
!т]!
'
\/
+у(оФ
|
!
Ё{
о
0
о
ф
о
Ф
!{
о
(,
ч
ч
щ
н
ч
Ф'
ю!
6!
Ё
оЁо
3 9х!ЁБд
Ё у у
-ц
_;
о
о^ _^:^
.(
ч
"^':
у^
;ч
9^
^
9^
9Ё;Ё й#
11 ч.
'г
5 о'
т Ф
цФ-:
й
Ф
*
Ф
-
Ф
9-
Ё
о*
Ё[;].;ё;
ьч
п
о.п
[
3п
;.т
!г
,т
_:#
9
-
аФ
ч
-=
!еЁ !
Ф 5
сФ^|
&
д-]
==!!5.
!: о о
т{
Ф
о
с\
о
оооб
п6
^
:
-Ф6|
с\
(о
/\ Ё
-!о(о-
з
о
о
х'=
_.Ф
.з9-
цх=
цФ:
оз
р
б
ь
о
Ф
б
н
о
,ЁвЁ
.*3,=
=*<
яхя
Ён я,= 19
Ё
Ф5оз
ФЁФ
уБ9н 5Бт
ф .:
ы>9
2^|
9пс'Р=
нЁвьаР?
: 2' ;с{ Р х
:с +.Ё
^эЁ
? яё
?ё9
с' ?
о 0*
53д
о.
1$0
дЁ
148
оо
оо
с\ со
Ф": у'
; а
^хх
;;
Ё
>9Ёо.
х о
-
с!ох
.) {, Ёз3о*аЁЁ
5
п
й';х-9-
о-о3
х
д
"-ьг
э
^
д
о'|
1
к
Ф
Фъ*
*п
Ф
_фб
Р;
Ёх.Ё..з
_6тнЁЁ
аЁ
п9'9д2ыб'{Ё9Р
а
.66
х
!Ф
! оо
\'^
ф=
нъЁ
*Ф
Фн
ч'ё
. х .цб! *
*Ф
_*^ Ф
!;
9
^'с!
з
*ь
ц.9.Ё
*';Ё,,:.]
?
Рч Р , } Ё
ь; 9
'$9
*
ь
'5
Ёё х!
э
;й'нЁЁ н
я! нЁ
'.ч
аЁ
нв .^,
*
:Ё Ё!
'*у:;
**'*9ё
:Ё
нн
до
;Ё
вн
+Ё
+ч }Ёр!Ё
но
соу
]|ч
тй
хс ув
(!
_ь
6*
3
0
к+('*о
-).:-+^'о
:
=€
|г
:
о
Ф>1
т
(]
+
^!
=
^
1_
^
99
йд г 1
о
2
х
-!]
нуя9]+"3
* * Ё #т
^:нт'[
эы9
-(';(';
х Ё
о*
.
о+
++
6
;о
;о
;
9
Ё д(_).9 д]
^,-
:
ана;э
5*
хЁ!
8Р
*Р д
о,
\,
ы<
оо
хй
1ч
.о
^Ёэ
<ч
д
ь
о
5
о
о
&
о
6
о
Ф
Ф
н
ц
о
ь
о
;
Ф
ц
Ф
ю
о
о
о
$
Ёц
.*)
Фб
\
=-
ь
'о
к!
х=
б
^о
Фх
о'!
!!
6х
б
о :_:
,-!
;Ф
;|
-:
9
чх
! ;Ф
й Ёо.,
а:о
х
*9
д
!ч
п|9
нЁ!
^:!
9
{;
{ п*0
;:=
Ё1,а
*
|й
й;ь
о оф
Фо
..Ф
цц
5!
оЁ
^:;
*х
оФ
о$
Ё
Ф
?!!
:э
Ё!
_о
но
!
Ё>
БФ
Ф
а.х
о
0
Фв

тАБл!!цА
4.40
сульФидь|,
свлвнидь1' твллуРидь1
плАтиновь]х
мвтАллов
&ш
пь
Ра
@в
]г
Р1
Рц5э
Р}т5;
[}л'5.;
ц1'5''
Р1-т:5э;
Р!з5в
Р0ц5;
Р6з5;
Р6:5;
Р05;
Р05:
Фэ5я
|г5;
1гэ5з;
1г5:;
1гз5в
Р15; Р15э
Рш5е:
Р}п5е;
Р[::5е';
&[5е:;
&6э5ез; &}гз5ев
Р6д5е;
Р0:5е;
Р05е;
Р05еэ
Фз5еэ
|гэ5ез;
1г5е:;
1гз5ев
Р|5ео,в;
Р15е;
Р[5еэ
Рш1е2
&1т1е;
(!'19"'
&|п[еэ;
&[тэ1еь
Р0ц1е;
Р0з1е;
Р6э1е;
Р6'1е;
Р01еэ
Фэ1еэ
1г1еэ;
|г#ев
Р{1е;
Р11ея
:^:-т]91'*
в,присутствии
окислителя
[271_273,
276].
!,остаточно
на-
де)кно идентифицированнь:е
наиболее
х5рактерные
хайькогенидь:
благо_
родных
металлов
представлены
в
табл.
4.40.
1ростьсе
еалоеенц0ьс
|алогениды
благородньлх
металлов
образуются
в процессах
галогени_
рования
то1{кодисперсных
металлов
и
их-солей,
а 1акх,е
;р;-;;;;'_
ливании
галогенокомплекснь1х
соединений
в
инертной
атмос6|ре
йлй
в
атмофере
соответствую_'щего
галогена.
-о!у,.,,,'е
и3
водных
раство_
3!]:^'^_""'-.'^9!1Р _1ч:!*,'
в своем
составе
Болу,
при
полном
у!алении
которои
начинается
ра3ру,.,:ение
галогеносоединёния'
в кристал1йнесйм
состоянии
безводньте
,р_ч!].
галогенидь|
пр-едставляют'."о"й
!'Б'йй.1,_
ные
цепи'
связаннь|е
галог€номост14ками
|1
образующие
насто
разлинн*е
м-одФикации.
€о
фтором
характерно
образоЁа:тие
соединений
в
вь!сших
степенях
окисления,
с иодом
_
в низших
степенях
окисления
1этэ_э1ь|.
Б
табл.
4.4\,
4.42
представлень1
,рост'е
ф;ьь;1"
и хлоридь|.
|(омплексньое
сое0цненця
11звестньп
многочисленнь|е
классы
комплек!ных
соединений
благород-
|{ь[х
металлов'
в которь|х
лигандами
являются
кислотнь|е
остатки
()ци-
долиганды)
Р-,
€|_,
Бг-,
|-,
шог,
5о?_,
с2о?_,
шс5-,
6ш:,
9*с99-'-шо;'
он-
и лейтральньте
молекулы
н2о,
шн3,
со,
шо,
ш2,
с2н1-,'шн2снэ€Ёэг\{Ёэ,
Р
(с6н5)з,
сн35осн3.
центральный ион
комплексного
соединения
мо'{ет
1{аход1{ться
в
ра3личнь1х
степенях
окисления
[272,
274_276].
8
табл.
1.13_.+..+9
прел-
ставлень!
соединения'
с которь|ми
химикам-те_хнологам
чаще
всего
при:
ходится
сталкиваться
на
практике.
},лоркомплексьт
образуют."
'
-!Б-
цессах
)кидкофазного
и_т_верАофазного
хлорирования
в
_
присутс"Ёии
хлоридов
щелочных
металлов
и неметаллов'
полупроводников,
6тходов
ч
руд'
содержащих
благо!однче-мета.пль|'
а так)!(е
при
раствооении
благороднь:х
металлов
|,73-275,
27в'
2]91
"
й'й..'г[..,;й;""{;;.
1(омплет(сь|
чаще
всего
исполь3уются
в каче1тве
исходнь|х
для
с}1нтеза
различпь|х
соединений.
@ни применяются
для
получения
катали3аторов
в ге'|'ерогс1]пых
и гомогеннь|х
процессах'
при
получении
порошков
бла-
городнь|х
металлов
разлинной диспеРсности и 1.
д.
цсм.'табл.
4.4[).
1д0
€ульфатокомплексь'
благородньтх
металлов
образуются
в
процес_
сах серно|(ислот|1ого
вь1щелачивания
руд'
полупродуктов
ра3л}1ч11ь1х
ма-
териалов в
присутствии
окислителе/г,
гтоэтому
они
ва)кны
как
для
тех-
нологов, так и
для
аналитиков'
кроме
того'
сульфатокомплексь|
успешно
исполь3уют
для
приготовления
электролитов
при
получении
покры_
тий платиновыми
металлами.
!{итрокомплексьт,
содер)кащие
группу
\Ф2,
коо!.(иниРованную
чере3
а3от'
об!азуютсяв
пРоцессах,нитро_
вания
ра3;ичнь|х
соле1]
или
материалов.
Фни
применяю1'ся
в
аффина)ке
платиновь!х металлов и
в аналитической
||рактике.
Аммиа|(ать!
платино-
вь|х металлов'
3олота и
серебра
успеш|{о
исполь3уются для
отделения
их
от
неблагородных
металлов'
получения
металлов
высокой
степени
чис-
тоть|'
в
аналйтической
и лабораторной
практике,
многие
аммиакаты
проявляют
биологинескую
активность
и
н-ашли
применепие
в медицине'
|!ианокомплексы'
особенно
золота и
серебра'
широко
используются
для
получения
гальванических
декоРативных
и
защитных
покрытий
(см.
табл.
4.43_4'47).
Фсобый
интерес
представляют
карбонилы
плати_
новых
металлов'
3олота и
серебра, обРазующиеся
в процессах
твердо_
фазного
и )кидкофазного
карбонилирования
различных
по_лупродуктов'
йа'ер'''',
и
сол|й
платин6вьтх
ме;аллов
(ём.
табл.
4.48)'
1акие
со-
единения
находят все
более
широкое
пРименение
в
качестве
катализа-
торов' а
такх(е исходнь1х
матер,алов
д'я
нанесения
пленок
и
покрытий
бл!горолными
металлами
из
г|зовой
фазы_.
Б отличие
от
дРугих
благо-
'роднйх
металлов
при
нитровании
ру,ений-
и
осмийсодерх(ащих
полу'
',ролуктов,
концентратов,
материа'оь
и
соединений
образуются
ояе_нь
уётойни"''е
нитрозо!<омплексньгё
соединения
ука3аннь1х
элемеЁтов
[274,
276]
(см.
табл.
4.49).
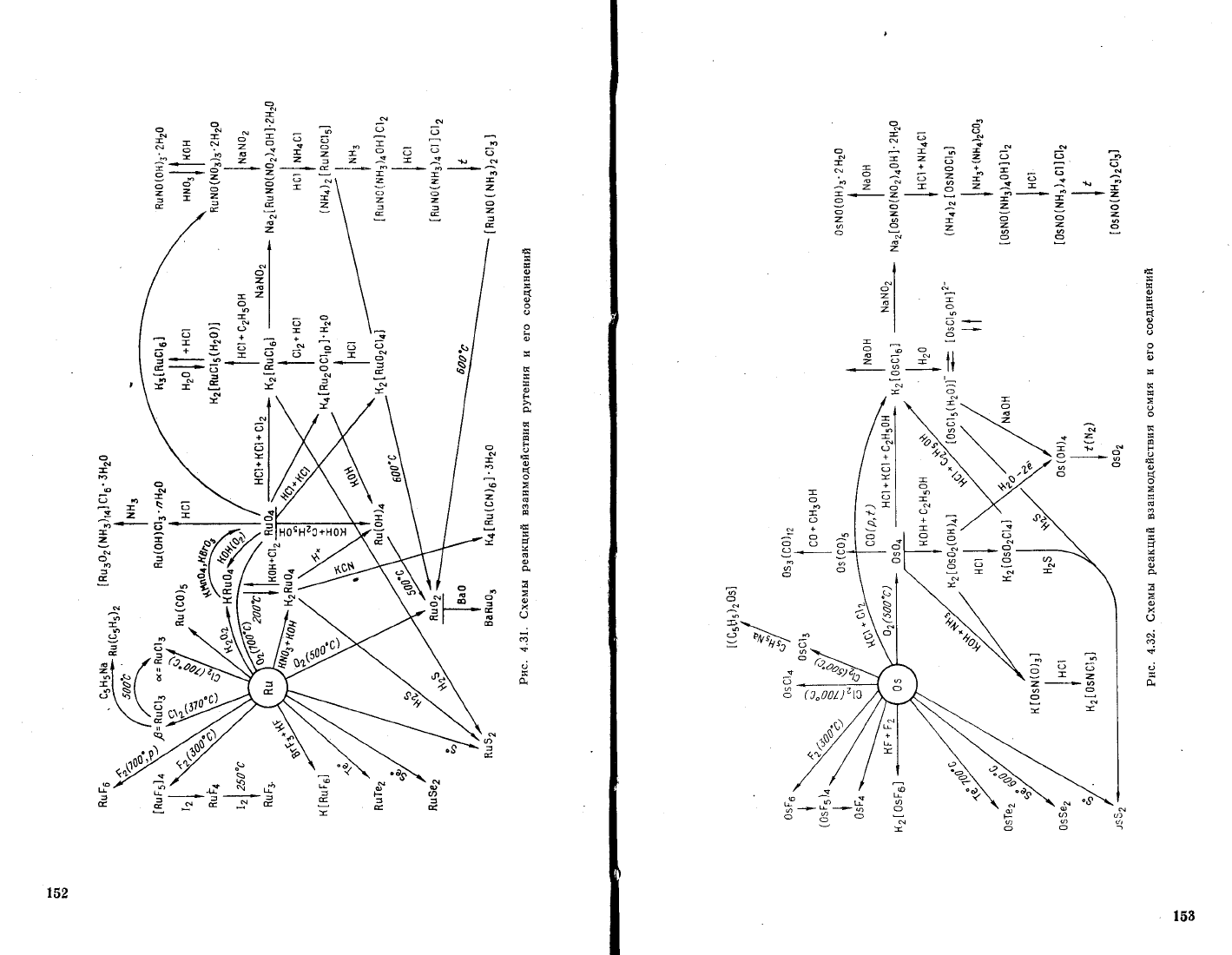
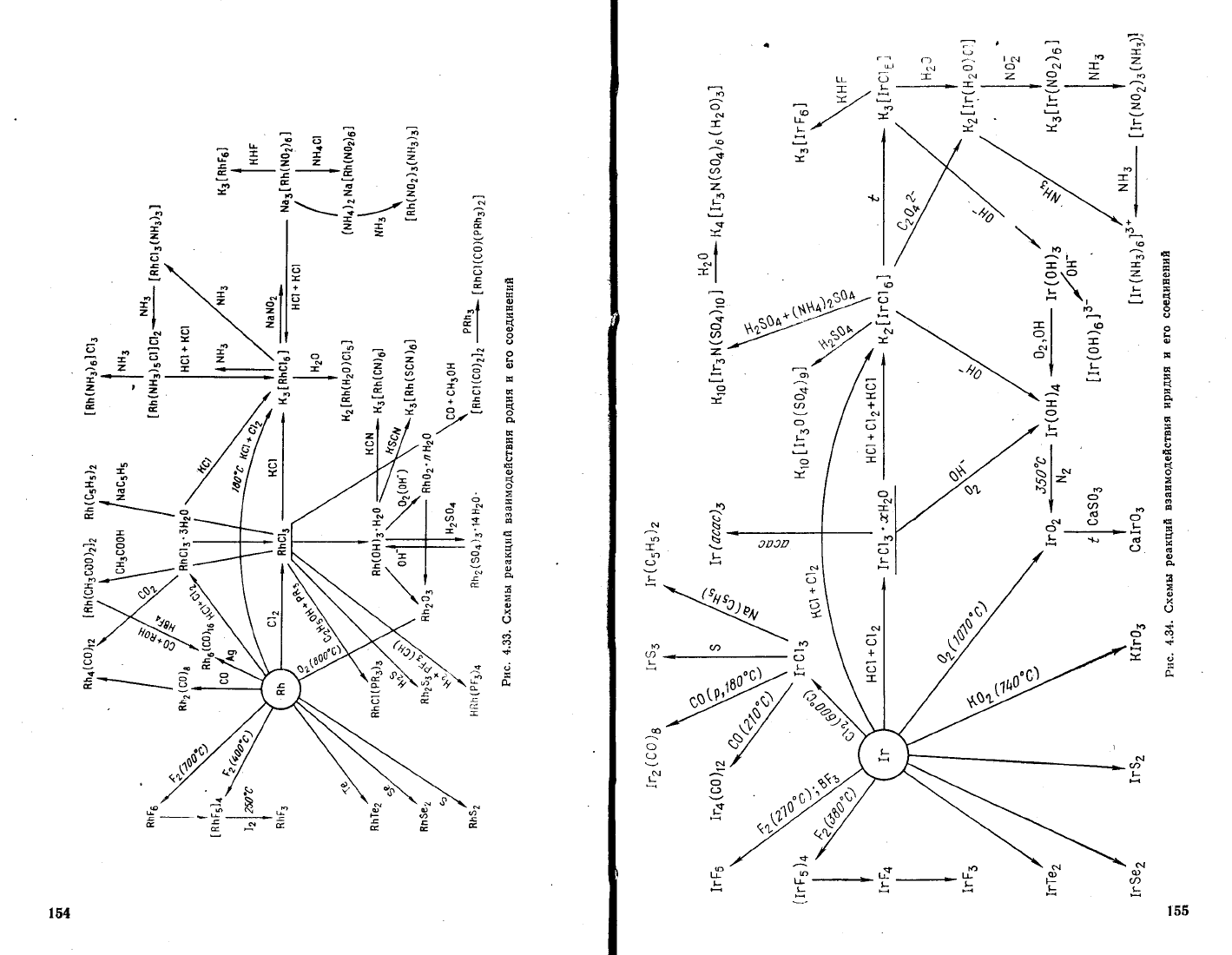
_Реакции
взаимодействия
металлов
платиновой
группы
и
их
соеди_
нений схематично
представлень|
на
рис.
4.31_4_36.
Ёаправление
реакцит}
замещения лигандов во внутренней
сфере
координационнь!х
соединений платиновых металлов опреде_ляется
3ако-
номерностью трансвлияния,
открь|той академ]{ком
Р1. 14.
9ерняевым
в
1926 г.
.[|ля
комплексов платины
([|)
рял
о-тРансвлия1{ия
3аписывает_
ся так:
он_<
\Ёз{
€1_<
8г_
<
сш-<
шс5_
<Р(с6н6)9.
1(а>кдьтй последующий
член
ряда
вытесняет
из внутренней
сферы
комплекса предьтдущий
в-
равнь|х условиях.
3та закономерность
от1{рь|-
ла перспективь! в
ра3ра0отке
теории
направленного синте3а координа_
ционнь|х
соедиттепий
платиновь!х
металлов
с 3аранее 3аданнь|ми
свой_
ствами' 3ада}1ного строения
|27
4-2761.
[!апример,
реакция
в3аимодействия
н1ш
-
пнз нзш,
'
с'|
"/ /
"
-/
/
/
р+
/
+Ё61*/пранс-
/
Р+
/
////
нзш
--
шнз
с]
-
шн3
приводит
к образованию
диаминодихлороплатината
(||)
-транс-и3омера'
а
реакция
взаимодеиствия
с1{-7
с1
с17____-----7
г!н3
/
Р+
/
+[\Ё{3
+ццс-
/
Р{
/
с1
/-----_--_---
с1
(1
-
!''|
цз
приводит
к образованию
а|{алогичного
цис-изомера.
|Б1
Ф
Ё{
Ф
о
о
Ф
к
=
о
[(
Ф
н
Ф
Ё{
о
Ф
:{
Ф
А
Ф
*
о
ы
ч
с;
.=
БФ
о
!2
2+Ф
х-
о)
*.8
о
Ф
ц
о
х
с
о
-
о
о
=
",..\
н
о
'"./
!
Ф
о
о
]
о
т
о
хо
оо
о
о
ъ_\-
о ь!-х
=
'4?9;-
б
Ф
3'(э"ооу)1уэ
-
Ф
о
р
в
е
5
1б8
."8\
*
сл
ц
1б2
Ф
€
у
о
з
7
э
е
-
т
о
с
,+9
Ф
+
Ф
у
+
-
о_
!д 9
!б
о
е
*)
Ф
е
-
!-
/ь*
/\
ф
чё(
т
2
Ф6
т2
23
-^
т
о
5
фЁ
ъх
ч2
т
о
"!
-!/о?
Ё=о
Ф2
2
-
+
о
оо
@т5
Ё-_;
о=
х
р
ъ
.ц=&е
;
-3*;
ой
\\/
-г
Ф
к
Ф
о
о
Ф
н
а
б
ф
н
Ф
к
о
Ф
!
Ф
Ф
!
о
о
е
!
нсэ+н0н
о
-
.Ф
6и=
!\
ъ+
Ё'
-^
=-
о
о5
фс
з
с
$
Ф
о
:
Ф
:"Ф2
ч
\,
(
-
(
ь
Ё
ц
э
Ё
*
т
2
о
2
ь
.1
}
@
т
ь
'-
@
!ф
Ф
оп:г
'2Ф=
+7-
ь
-ю
х
т!
=!
{
@
т
ь
Ё!
Ф
{
Ф
о
о
Ф
х
в
в{
д
б
Ф
н
Ё
Ф
к
о
:
я
Ё
Ф
д
д
А
о
ф
д
ю
о
ь
Ф
ф
-
[
ф
у
о
(!
'д
@
!!
[
:с
о
ф
т.
*
о
(!)
2
о
!
<г
=
-{
н!
-!
|
ю
ь
о
?
ю"
^|
дд
о\о
!\,
!ъ
!^
-!
т
'!
э
!:
^<[
-
д
о
Ф
о
о
=
+
ф
о
+
о
-
о
<л
о
ю
ь
Ф
х
о
ф
-
у
}о
\
ц
ф
о
+
о
:г'
эрэр
н
=
о
о
+
Ф#
Ф
Ф
(л
ь
-:]Фю
Ф-['-ш
!-!
!
н
Ф
|-
р
(_)
[
у
*,,
,7
|55
{,\
";
1б4
Ф
о
о
о
д
Ё
-{
е!
Ф!
!
--Б
т-
оо
.д
о
от
Ф{
Ф
Ф
2
Ф
2
д
Ё
=
Ф
А
е
-
т
2
Ф
Ф
=
Ё
2
т
=
Ф
о
-
с
€
х
х6
Фд
Ё:
{-.-_
!
!_
!?
11*
с#
-
1
!
!
!
!
!
-'/
Ф
т
-
Ф
6
д
в
-!
т!
21
,
е
:6
ой=
+о
-Р-
й
2,=
=,
еа
*
Ф
{
Ф
о
о
Ф
о
о
д
н
к
Ф
к
о
Ф
Ф
а
Б
Ф
х
о
о
т
:
Ф
Ё
с
!
т
+
Ф
с
уу\
":"'\
Ё
е
Ф
с
Ё
/;"
&
п;
с
Ф
о
5
е
е
р
.Ф
е
о
:(
тб
Фо
'аРд
ФэЁ
4-9--"-'-

Ф
о
Ф
Ф
в
Б
в
Ф
н
Ф
<
о
Ф
р
Б
о
Ф
ц
&
1
[
!
#
+
нт
\!-
Ё з55
-а
6€:.
э
!';;Ё?
;--1Ё
&
!!-э-{
\ \ !-
=
-э
9
+
\ \т
э
3 / ч
\\к
,з-$/
\}
\ъ- //
,\ъ^
// Ф
"\\
//э---=--
\\/
€'
'а \\/, ц
с \']
3
о
9'.;
;,{}
5-з*з
Ё
*
Ф
-.!
д
з-з-;
;!{
-1
?
*
-^}
!!!'
|!
;-.-ёЁ1
ц,| 9= *
]
;э3;"Ё
{]
$
Ё-з*з
5
:/ /\
Ё
*;
_1 {-?т=
+
!
Ф
о
х
б
о
Ф
х
т
+
:
-
/
€
1Б7
|56
-*
'$
он9
--$
6
2-
тч
хв
Ёс
р*
*Ё
\
\
ы\
=
о
99
бб
!Б
[Ф
ъ\
"\
'е\'.\
ъ'\А
о\
в1
с\
т\'
1!\
9!!_е
!!ос
!!-
.
_ !!ь
з9'.-
3
|
9.дэ
с+-.*
'-*
$0шн
у
А
р%)
'-\
?;
--{
.ъ\,
у

Ё
Ё
;нЁ
:н
ёвв *
:ЁЁ-
3
!
|
$
!в$Ё' Ёв
!,|
;=Ё,
Ё
нЁян
ЁЁ двдЁ3Ё$нн
дЁвЁ$,*ЁЁ
58 8
3ё
Ё
}.
м
х
ч*
Ёц9
9 Ё9;Ё
!
, ЁЁ*
| !
+
!
!!
о?
ах|
!
!
|
!Ё$
$
хп
Ёв
-
=
н
'
н у
ь
Рч
Ф=у х
ох
п:
ц;\оч/
(,
!-
о
в
в
евв€
э
Р3
в
эвЁв
Ёвв€в
в
$
;
;й;5
к
;Ё
ё
чй;Ё
й*Ё5*
;
;3
*
ёЁ
ЁЁ
е:!
я Ё Ё Ё + Б
,
а! Ф
=
*
Ё
Ё
Ё}
Ё|}Ё'Ё;}3=
ф'= хзэ
чэ Р
!.=,
3
.;ЁЁ*Ё
'Ён
ЁЁ!зтЁ3ЁЁвя
-й
Ё !
х
х
Б 5- Б!1Б-;
Б
38'.9
"
Бз
!с) !.!ч^
Р-
!-ч
х х* хэ*хе*Ё
ё
*3ё,Ёё
у
9 з
9
3
..
'@о^т9
ьо.Рао
*с, в
*
Б3
--п]Р
д9
9
^
ф1\
6 ф з
?ч*
тЁт
Ёа
Ё''1
ё#8 896 8е
36!
оо
(о
[о
!
!?чч
|ч
ч
!!ч
?
! !
!
о! 6! с\
о.
159
Ё
ар
* р
ъф**
*Ё'Ё
Ё'=нн
Ё
нн$9Ё
авЁ,=
.$н:а
!!
.ё
;
&*:
[
ЁннЁ,=Ё['{
?рэ';
'Р
3Ё
3'энЁЁзЁР;'*3'
#нёяЁ
*
й,г
аяддвяЁ5ЁнЁн
Ф
п
/
о
чоФ
<й
! в* я
?,
Ё
аБ
,! ! а
!
1
!
!а
н 9> !'
|
Ф
Ф
:о ё о
РЁ3;
&
Р
!
т';:
Р
оЁв}Ё6
'т-:^
.-Ё';
!
^
^;
Ё
с
-:
Ф
;
ёё:ё
!!
ё:
€3:
:
!!
э
+^'?г_
о
о
ф
о
йв],6п
г-
б
о)
кй6,!
Ё
(о
е !ь 63
*
ё
н
вЁ
3
Ё Ё3 Ёх.-
о.
ь
о.
БФ
о.
Ё в Ё:
еЁ'Ё 1н3
]*Ё€*
"
*э Р з
э'н
.-в
э
5."
"
*}*х.
н
5ЁвЁ
ЁЁ
Ё'в'3Ё$ЁЁ ЁЁ';Ё
Ё=
д
ЁЁ
Ё
*95Р$д
$5'Ёё*9'ЁЁ'ЁЁ
д
Ё
.]
Ё
]
0 х
йв
г]
1й+кБ
8ыА,:ц,--Ф
б
.
-0е
._к
+
в+
ы
к
,9я
*.ц:_
ц
=-
!:-
ц
++ !!
"33
*.Ёд?€
Ё
*
1
ЁЁ
1
'Ён
ньэБ$Ё $
хцх,хйо(.
д-з5
ЁР 4€ЁпЁ ц'3с Ё
йх'йЁхйхо.9с[
4.
о"
н
у
з
ч
ц
{
к
оо
}!фо)!
!.
с\ 6]
Ф
о
Б
!-
ш
х
д
Ё{
о
о
!
!!
д
<
д
о
н
0
щ
д
д
к)
Ёо
:
Ф
н
Ф
.в
о
н
о
н
Ф
ф
Ф
Б
о
ю
о
о
Ф
Ф_
о
о
