Реферат - Біофізика білка
Подождите немного. Документ загружается.


встановлено, що у разі поганої розчинності вуглеводнів у воді зміна вільної енергії
позитивно, і, отже, ентропія системи зменшується.
3
Що ж означає зменшення ентропії при розчиненні?
Прямими фізичними дослідженнями було показано, що при цьому відбувається збільшення
частки кластерів. При розчиненні молекули вуглеводів втискуються в порожнині всередині
тетраедричних осередків кластерів і витісняють звідти неструктуровану воду. Остання
утворює нові кластери, і впорядкованість системи збільшується, а значить, ентропія
зменшується. Тому гідрофобні взаємодії є результатом властивостей води, а не якихось
особливих сил, що зв'язують неполярні групи один з одним. Таким чином, асоціація
неполярних молекул у воді за рахунок гідрофобних взаємодій визначається виштовхує дією
води на неполярні сполуки, що обумовлено тенденцією молекул води до досягнення стану
максимальної невпорядкованості.
3.4. Гідрофобні взаємодії та структури білків.
Всі амінокислотні залишки, що входять до складу поліпептидного ланцюга умовно
поділяються на дві групи:
-Неполярні (гідрофобні)
-Полярні (гідрофільні)
Ступінь гідрофобності залишку визначають по різниці вільних енергій розчинення
амінокислоти в слабополярном розчиннику і воді (зазвичай використовують етиловий
спирт).
Отримані таким чином величини різниць вільних енергій, що припадають на білкову групу
амінокислоти при перенесенні з спирту у воду, наведені в таблиці:
Ступінь гідрофобності амінокислотних залишків
Гідрофобні
F кДж/моль
Три Иле Тир Фен Про
12.50 12.40 12.00 11.10 10.85
Гідрофобні
F кДж/моль
Лей Вал Лиз Гис Нет
10.10 7.06 6.27 5.85 5.45
Гідрофільні
F кДж/моль
Ала Арг Цис Глу Асп
3.05 3.05 2.71 2.50 2.26
Гідрофільні
F кДж/моль
Тре Сер Гли Асн Глн
1.84 0.17 0.00 -0.04 -0.42
33 Назви залишків: глиця, аланіл, валив, Лейца, ізолейцил (мулі), фенілаланіл (фен), пролив,
трітофоніл (три), серил (сер), треоніл (тре), метионит (мет), аспарагін (асп), глутамініл ( глн),
цистин, аспаргіл, глутаміл (гли), тирозил, гістіділ (гіс), лізил (ліз), аргініл (арг).
Гіпотеза про визначальну роль гідрофобних взаємодій була доведена в 1944 році. Ідея
полягала в тому, що гнучка молекула білка у воді згортається в глобулу (оскільки полярні
залишки білка прагнуть до максимального контакту з водним оточенням, а неполярні - до
мінімального контакту). З геометрії відомо, що мінімальною поверхнею при заданому обсязі
володіє кулю. Прагнення неполярних залишків утворити всередині білкової частини якусь
подобу кулястої краплі, а полярних - зосередитися на її поверхні, і призводить до утворення
компактного тіла - глобули з гідрофобним ядром і гідрофільної поверхнею.
11
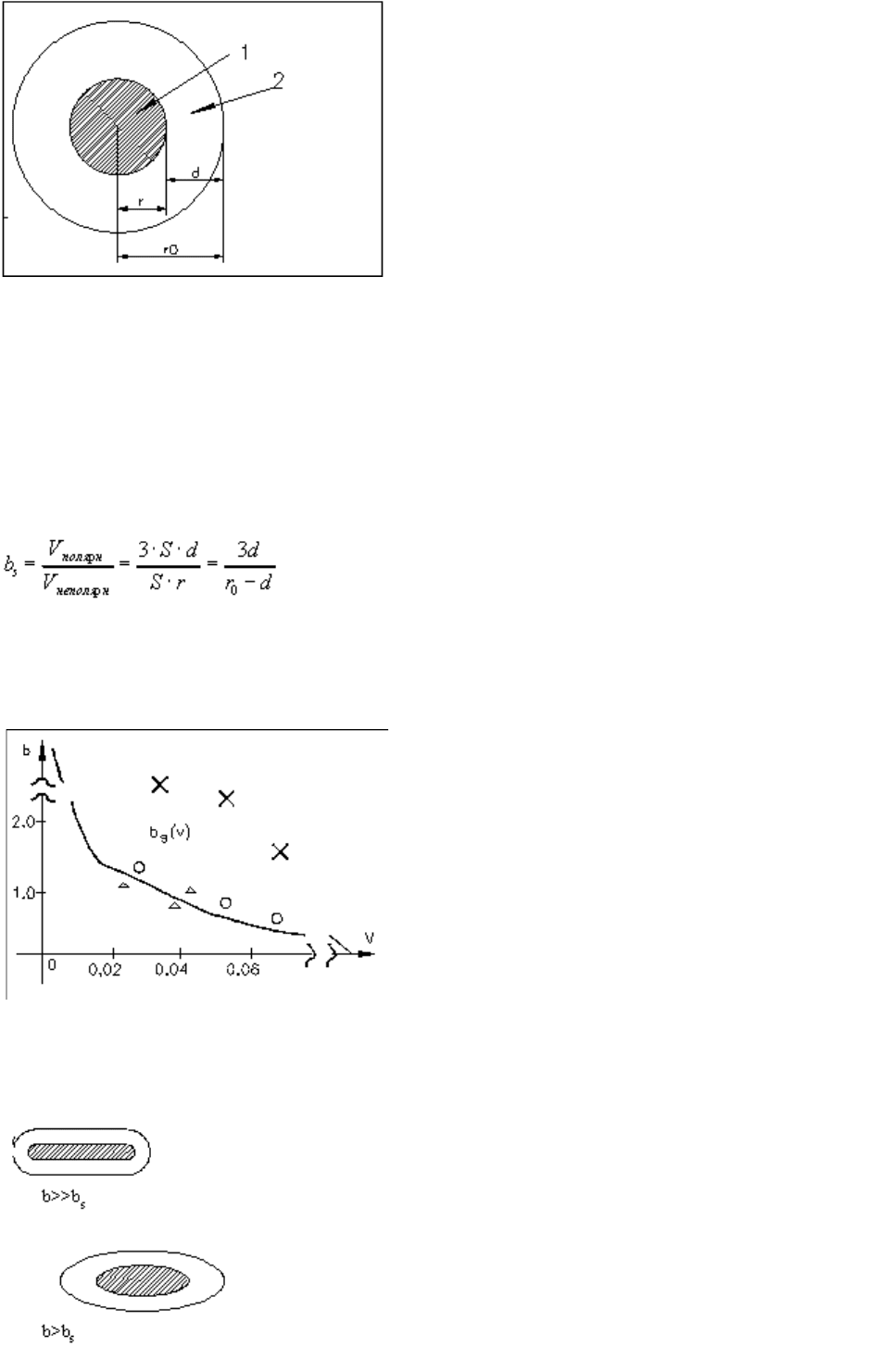
3
1 - гідрофобна ядро
2 - гідрофільна оболонка
У 1964 році Фішер встановив, що, знаючи загальне число амінокислотних залишків у ядрі і
ставлення полярних залишків до неполярних, можна передбачити форму глобули. Для
простоти будемо вважати, що всі залишки мають однакові обсяги. Знайдемо відношення
числа полярних залишків до неполярних, яке позначимо bs. Будемо вважати, що радіус
глобули r0, і кулька покрита мономолекулярним шаром полярних залишків товщиною d
(Фішер вважав, що d ~ 4-5A). При зроблених припущеннях відношення числа полярних і
неполярних залишків дорівнює відношенню обсягів сферичного шару і центрального ядра:
3
Отже, чим менше r0, тим більше повинна бути відносна гідрофільність білка. На малюнку
наведена теоретична крива (крива Фішера) значень параметра b від обсягу глобули (V =
4/3r03), а також експериментальні значення.
3
Кулька може бути сферичної, строго кажучи, лише за b = bs (відповідає кривої Фішера на
графіку). Якщо b> bs, тобто число полярних залишків у білку більше, ніж необхідно для того,
щоб покрити гідрофобна ядро гідрофільним шаром, то кулька витягується у вигляді
еліпсоїда і має велику поверхню, ніж у випадку сфери.
3
12

b>> bs виникают фібрилярні структури (позначено x на графіку)
b <bs гідрофільні залишки не повністю закривають гідрофобне ядро і гідрофобна взаємодія
між такими відкритими ділянками призводить до агрегації білків і виникнення
надмолекулярних структур (позначено на графіку).
3
Таким чином, білки, для яких значення b лежать вище кривої Фішера, представляють собою
еліпсоїди і фібрили, значення лежать на кривій представляють собою глобули. Під кривої
розташовуються білки, що утворюють надмолекулярну структуру. Формування
гідрофобного ядра в глобулярних білках має принципове значення для їх функціонування.
Білки при їх величезній молекулярній масі мають порівняно компактною структурою перш
за все, завдяки гідрофобним взаємодіям.
Висновок
13

33333Загальноприйнятою є класифікація білків по їхніх функцій. Особливо важливе значення
мають білки, що функціонують як ферменти, так як вони забезпечують протікання
практично всіх хімічних реакцій у клітині і організмі. Однак така центральна роль ферментів
не зменшує значущості інших білків: наприклад, без інсуліну виникає діабет, а без
гемоглобіну клітини не забезпечувалися б киснем.
33333Білки виконують настільки різноманітні функції, що їх навіть важко перерахувати. Які
особливості структури визначають їх універсальність? Чи можна запропонувати якийсь
загальний механізм їх функціонування? Загальну схему функціонування білка можна
представити в наступному вигляді:
33333333333333333ЗВ'ЯЗАТИСЯ → ТРАНСФОРМУВАТИСЯ → ПОСЛАБИТИ.
Синтез білкового ланцюга на рибосомі триває близько хвилини. Після цього білок відразу
ж готовий до функціонування. Це означає, що згортання поліпептиду і формування його
просторової структури відбувається дуже швидко. Природно припустити, що згортання білка
може починатися ще на рибосомі, до закінчення повного синтезу всієї білкової ланцюга.
Основні завдання біофізики білка
1. Теоретичні та експериментальні дослідження білкових молекул, а також надмолекулярних
систем, які ними утворені.
2. Встановлення зв'язків первинної структури білка, тобто послідовності амінокислотних
залишків, та просторової будови молекул білків.
3. Вивчення фізичних механізмів біосинтезу білка.
4. Дослідження фізичних процесів, що лежать в основі біологічних функцій білків.
Список використаної літератури
14
