Магеррамов А.М., Ахмедова Р.А., Ахмедова Н.Ф. Нефтехимия и нефтепереработка
Подождите немного. Документ загружается.


318
В 1980 году более 50 % производимого изопропи-
лового спирта использовали для получения ацетона. К 2000
году эта доля снизилась до 6 %. Установки, выдающие од-
новременно фенол и ацетон, почти полностью вытеснили
технологию получения ацетона из изопропилового спирта.
В настоящее время изопропиловый спирт применяется
в первую очередь как растворитель для красок, синтетиче-
ских смол, при производстве электронной техники. Он
используется также для получения изопропиловых слож-
ных эфиров и пероксида водорода.
На основе пропилена получают н-бутиловый и изобу-
тиловые спирты реакцией оксосинтеза.
Оксосинтез – это гомогеннокаталитическая реакция,
протекающая в жидкой фазе в присутствии карбонилов ко-
бальта в качестве катализатора:
CH
3
CH
3
-CH=CH
2
+CO
CH
3
-CH
- CH
2
C
O
+ H
2
CH
3
-CH
2
-CH
2
CHO
CH
3
-CH-CHO
При этом образуются масляный и изомасляный альде-
гиды, при гидрировании которых получаются н-бутиловый
и изобутиловый спирты.
CH
3
-CH
2
-CH
2
CHO
+ H
2
CH
3
-CH
2
-CH
2
-CH
2
OH
Н-бутиловый спирт применяется в качестве нетоксич-
ного и не горючего растворителя для лаков. Другие облас-
ти его применения – пластификаторы и производствопро-
стых и сложных эфиров, используемых в покрытиях на
водной основе и клеях.
На основе масляного альдегида возможно получение
2-этилгексанола.
CH
2
-CH
3
2CH
3
-CH
2
-CH
2
CHO
+ H
2
CH
3
-CH
2
-CH
2
-CH
2
-CH-CH
2
OH
Наиболее важным направлением применения 2-этил-
гексанола является производство пластификатора, исполь-
зуемого для повышения гибкости поливинилхлорида.
319
Производство глицерина на основе пропилена
Больший практический интерес представляет процесс
окисления пропилена в непредельный альдегид — акроле-
ин. Процесс ведут при 350-400 °С в присутствии катализа-
тора, например, окиси меди. Чтобы предотвратить даль-
нейшее окисление и полимеризацию акролеина, берут зна-
чительный избыток пропилена; отношение пропилен : ки-
слород составляет от 4:1 до 10:1; кроме того, реакционную
смесь разбавляют азотом или углекислым газом так, чтобы
концентрация кислорода не превышала 4-8 % (объёмных);
O
H
CH
2
=CH-CH
8
+
O
2
CH
2
=CH-C
+ H
2
O
Наиболее перспективным использованием акролеина
является получение из него глицерина по бесхлорному ме-
тоду. Глицерин, как известно, получают уже давно в каче-
стве побочного продукта при производстве мыла из при-
родных жиров, которые представляют собой сложные эфи-
ры глицерина и высших жирных кислот. На получение 1 т
глицерина требуется более 10 т растительных или живот-
ных жиров — ценных пищевых продуктов. В связи с рос-
том потребности в глицерине, который используется для
получения алкидных (глифталевых) смол, нитроглицерина
(для динамита и бездымного пороха) и многих косме-
тических препаратов, а также из-за меньшего использова-
ния жиров для производства мыла в связи с увеличением
производства синтетических моющих средств (детерген-
тов), очень остро встал вопрос о разработке процессов по-
лучения синтетического глицерина из пропилена. Ниже
приведена схема получения глицерина через акролеин:
CH
3
CH
CH
2
C=O
CH
CH
2
H
C=O
CHOH
CH
2
OH
H
CH
2
OH
CHOH
CH
2
OH
O
2
H
2
O
2
OsO
4
H
2
Ni
Разработаны и другие процессы получения глицерина
из пропилена. Так, при заместительном хлорировании про-
пилена при 500-530
0
С получают хлористый аллил.
Реакция протекает по радикально-цепному механизму:
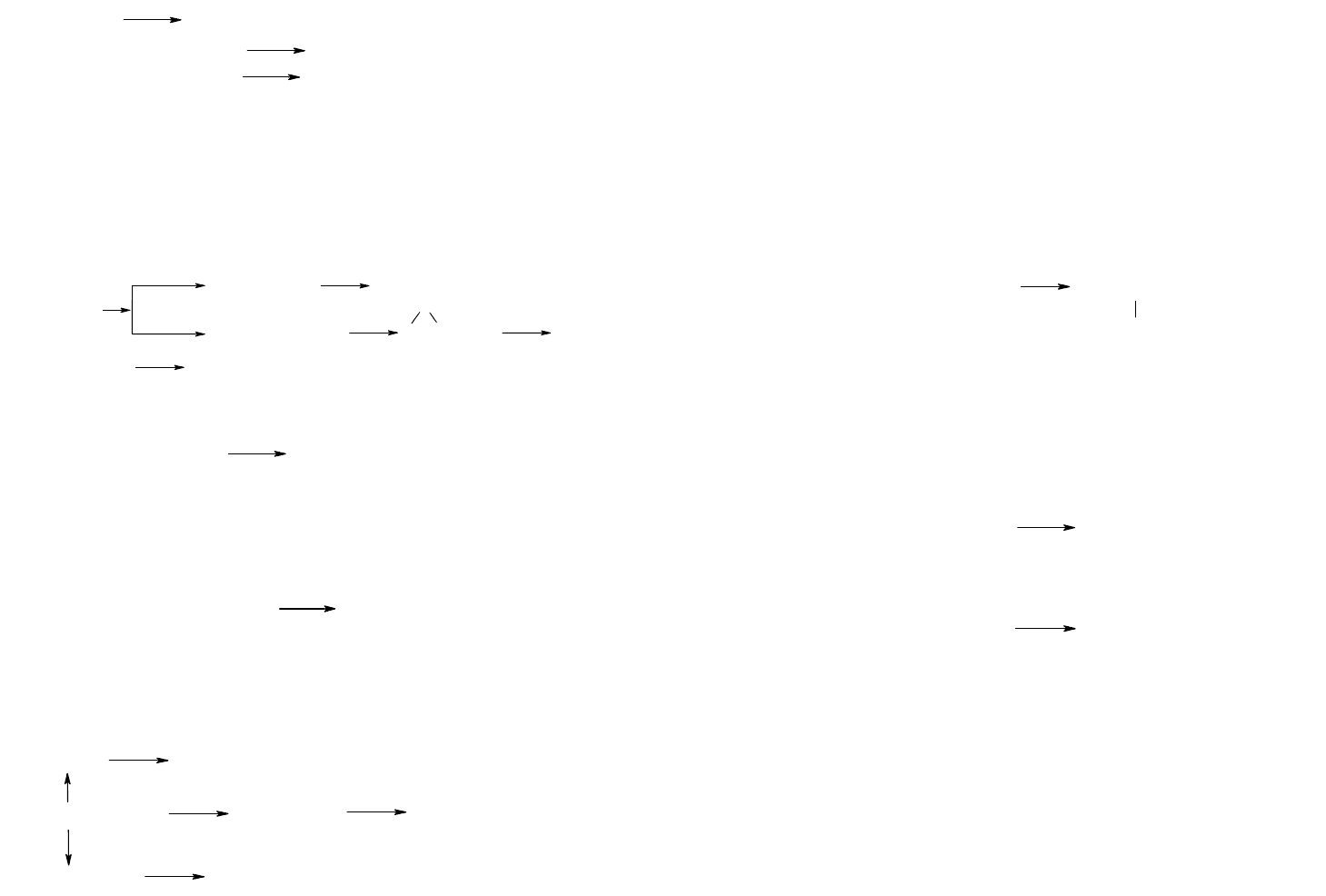
320
Cl
2
2Cl
.
500
0
C
CH
3
-CH=CH
2
+
Cl
.
.
CH
2
-CH=CH
2
+HCl
.
CH
2
-CH=CH
2
+
Cl
2
CH
2
-CH=CH
2
Cl
+Cl
.
Процесс проводят в избытке пропилена при соотно-
шении С
3
Н
6
:Сl
2
= 3:1-5:1. Выход хлористого аллила около
80 % по хлору.
Хлористый аллил является важным промежуточным
продуктом для получения некоторых ценных соединений.
Из него получают аллиловый спирт, аллиловые эфиры,
эпихлоргидрин, глицерин.
O
NaOH
HOCl
CH
2
-CH=CH
2
Cl
CH
2
-CH=CH
2
OH
ClCH
2
-CH(OH)-CH
2
Cl
CaO
аллиловые эфиры
CH
2
-CH-CH
2
Cl
H
2
O
2
CH
2
OH-CHOH-CH
2
OH
Ca(OH)Cl
Глицерин можно получать также окислением аллило-
вого спирта перекисью водорода:
CH
2
-CH=CH
2
OH
H
2
O
2
CH
2
OH-CHOH-CH
2
OH
Окислительный аммонолиз пропилена
При окислении смеси пропилена с аммиаком образу-
ется акрилонитрил – важный мономер для получения син-
тетического каучука и волокон
CH
3
-CH=CH
2
+NH
3
+ 3/2O
2
CH
2
=CHCN
+3H
2
O
Процесс проводится в псевдоожиженном слое катализатора
(оксиды сурьмы и урана UO
2
Sb
3
O
7
) при температуре 425
0
С и
давлении 2,1 атм, мольное соотношение пропилен:аммиак:кис-
лород = 1:1:2. Выход акрилонитрила 70 % в расчёте на пропилен.
Этот процесс протекает по следующей схеме:
HCHO
HCN
CH
3
-CH=CH
2
O
2
CH
2
=CH-CHO
NH
3
CH
2
=CH-CN
CH
3
-CHO
NH
3
CH
3
CN
O
2
O
2
Наряду с акрилонитрилом образуются в качестве по-
321
бочных продуктов метилнитрил и цианистый водород.
Этот метод получения акрилонитрила настолько экономи-
чен по сравнению с другими способами получения акрило-
нитрила (из оксида этилена и HCN, из ацетилена и HCN),
что вытеснил их из промышленности.
Эта реакция распространена также на получение ме-
такрилонитрила из изобутена.
Около половины всего произведённого акрилонитрила
перерабатывается в акриловые волокна — орлон, акрилон,
динель, которые являются полимерами или сополимерами
акрилонитрила
CN
n CH
2
=CH-CN
-[-CH2-CH-]-
n
Эти волокна находят широкое применение в произ-
водстве одежды, в обивке мягкой мебели, а также в про-
мышленности для получения сополимера стирола и акри-
лонитрила (САН) и тройного сополимера – акрилонитрил-
бутадиен-стирол (АБС). Эти пластмассы недороги, они об-
ладают высокой ударной прочностью и долговечностью.
При гидролизе акрилонитрила образуется акриловая кислота.
CH
2
=CH-CN + 2H
2
O + H
2
SO
4
CH
2
=CH-COOH + NH
4
HSO
4
Промышленное применение находят эфиры акриловой
кислоты – акрилаты. Наиболее важным среди акрилатов
является этил-, бутил-, 2-этилгексил- и метилпроизводные.
CH
2
=CH-COOH + C
2
H
5
OH
CH
2
=CH-COOC
2
H
5
+ H
2
O
Наиболее существенные рынки сбыта этих соедине-
ний связаны с изготовлением покрытий, клеев, мелованной
бумаги, добавок к цементу.
Диспропорционирование пропилена
Фирма Phillips Petroleum Co разработала процесс «Triol»,
посредством которого пропилен диспропорционируется на
кобальтовых и молибденовых катализаторах при температуре
150-210 °С и давлении 1 МН/м
2
(10 атм), превращаясь в эти-
лен и н-бутилены.
Полагают, что в этой реакции быстро устанавливается

322
обратимое равновесие между пропиленом и продуктами
его диспропорционирования, которое включает образова-
ние на поверхности металлического катализатора квази-
циклобутанового комплекса
CH
3
CH
3
CH=CH
2
CH=CH
2
CH
3
CH
3
CH - CH
2
CH - CH
2
CH
3
CH
3
CH
CH
CH
2
CH
2
M
M
M
10.3.3. Синтезы на основе бутиленов
Углеводороды С
4
содержатся в продуктах пиролиза
тяжёлых фракций нефти. Эти изобутан, н-бутан, бутадиен,
изобутилен, бутен-1 и бутен-2 (таблица 10.3).
Таблица 10.3
Структура Название
1 2
CH
3
-CH-CH
3
CH
3
Изобутан
CH
3
-CH=CH
2
CH
3
Изобутилен
СН
3
-СН
2
-СН=СН
2
Бутен-1
СН
3
-СН=С=СН
2
Бутадиен-1,2
СН
2
=СН-СН=СН
2
Бутадиен-1,3
СН
3
-СН
2
-СН
2
-СН
3
н-Бутан
CH
3
H
CH
CH
H
CH
3
транс-Бутен-2
CH
3
H
CH
CH
CH
3
H
цис-Бутен-2
Стандартная смесь С
4
-углеводородов, выходящая из
установки пиролиза газойля имеет следующий состав:
Изобутан 5 %
323
н-Бутан 5 %
Бутадиен . 42 %
Изобутилен 18 %
Бутен-1 18 %
Бутен-2 12 %
Для разделения этих углеводородов обычное фрак-
ционирование не подходит ввиду близости температур ки-
пения некоторых из них. Поэтому применяются методы
экстракции, абсорбции и химические реакции.
Бутилены в нефтехимическом синтезе
Бутилены получают дегидрированием бутана в при-
сутствии алюмохромкалиевого катализатора (0,6 % К
2
О,
17,4 % Cr
2
O
3
, Al
2
O
3
) при температуре 560-620
0
С.
CH
3
-CH
2
-CH
2
-CH
3
CH
2
=CH-CH
2
-CH
3
+ H
2
CH
2
-CH=CH-CH
3
+ H
2
При дегидрировании изобутана образуется изобутилен.
CH-CH
3
CH
3
CH
3
CH=CH
3
CH
3
CH
3
-H
2
Бутилены широко используются для получения бута-
диена. Кроме того, они применяются и для других целей.
Димеризаций бутиленов получают полимер бензин — вы-
сокооктановый компонент моторного топлива.
Но в настоящее время этот процесс вытеснен катали-
тическим алкилированием изобутана бутиленами с целью
производства алкилатов — компонентов высокооктанового
топлива.
Реакцию каталитического алкилирования проводят в
присутствии кислых катализаторов, например, серной или
фтористоводородной кислоты. Реакция протекает по ион-
но-цепному механизму через промежуточное образование
карбкатионов. Поскольку последние легко изомеризуются,
конечный продукт представляет собой сложную смесь
изомеров.
Протон от катализатора присоединяется к бутену-1, а

324
образовавшийся карбкатион взаимодействует с молекулой
изобутана, в результате чего образуется н-бутан и третич-
ный бутилкарбкатион. Так зарождается цепь; третичный
бутилкарбкатион присоединяется к бутену-1, в результате
чего образуется новый карбкатион, имеющий уже восемь
атомов углерода. При взаимодействии его с изобутаном
получается октан разветвлённого строения, который явля-
ется целевым продуктом, и третичный бутилкарбкатион,
который продолжает цепную реакцию.
Получаемый при этом алкилат (смесь изооктанов) ха-
рактеризуется высоким октановым числом (100) и является
ценным компонентом бензина.
1. Первой стадией процесса (возникновения цепи) явля-
ется протонирование олефина:
2. При высоком отношении изобутан: бутен бутильный
карбоний-ион реагирует в основном с изобутаном с
образованием третичного карбоний-иона:
C-C-C-C + C-C-C
C-C-C-C + C-C-C
+
C
C
+
2а. Возможна также изомеризация первичного бутильного
катиона в третичный без обмена протонами
C-C-C-C
C-C-C-
+
C
+
3. Образовавшийся по реакциям 2 и 2а третичный бу-
тильный карбониевый ион вступает в реакцию с буте-
ном:
4. Далее вторичный октильный карбкатион изомеризует-
ся в более устойчивый третичный:
C
C
C
C
C-C-C-C-C
CC
C
+
+
C-C=C-C + HA
C-C-C-C + A
+
-
325
C-C-C-C-C
C
C
C
C-C-C-C-C
C
C
C
C-C-C-C-C
C
C
C
C-C-C-C-C
C
C
C
+
+
+
+
5. Изомеризованные октильные карбкатионы в результате
обмена протоном с изоалканом образуют целевой про-
дукт процесса – 2,2,4-, 2,3,3- и 2,3,4-триметилпентаны:
Реакции 2, 3, 4 и 5 представляют собой звенья цепи,
повторение которых приводит к цепному процессу.
6. Обрыв цепи происходит при передаче протона от карб-
катиона карбаниону кислоты:
Наряду с основными реакциями С-алкилирования изо-
бутана бутиленами, при которых на 1 моль изобутана рас-
ходуется 1 моль олефина в процессе протекают и побочные
реакции, приводящие к образованию продуктов более лёг-
ких или более тяжёлых, чем целевой продукт, к потере ак-
тивности и увеличению расхода катализатора. К таковым
относят реакции деструктивного алкилирования, самоал-
килирования изобутана, С-алкилирования с участием С
3
и
С
5
алканов и алкенов, полимеризацию алкенов, сульфиро-
вание олефинов с образованием сложных эфиров, кислого
шлама и др.
Деструктивное алкилирование происходит в результа-
те β-распада промежуточных карбониевых ионов и приво-
дит к образованию углеводородов С
5
-С
7
. Скорость этих
реакций снижается с понижением температуры.
Сернокислотной гидратацией бутиленов получают
вторичный бутиловый спирт:
изо-C
8
H
17
+ изо-C
4
H
10
изо-C
8
H
18
+ изо-C
4
H
9
+
+
изо-C
8
H
17
+ A
-
изо-C
8
H
16
+ HA
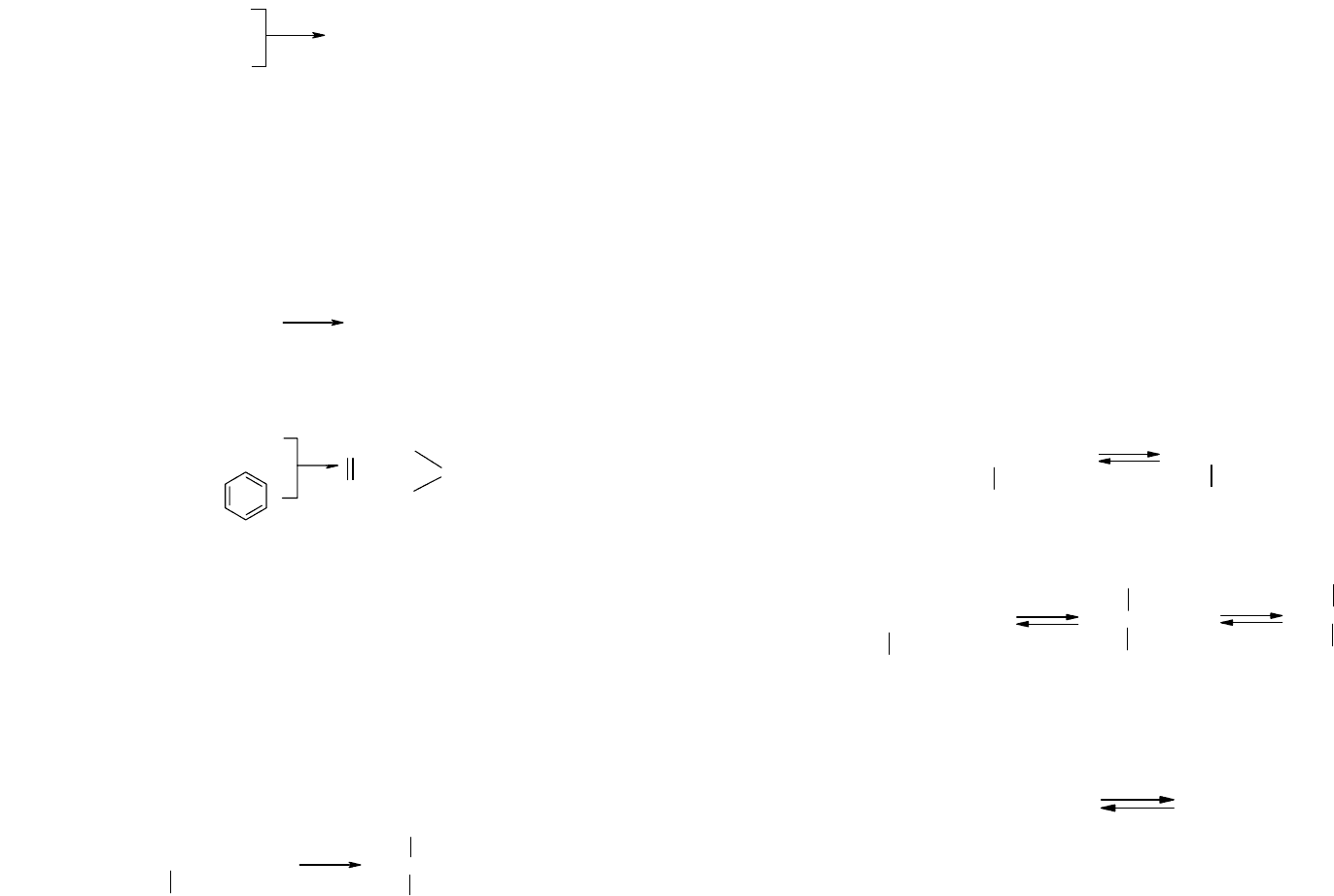
326
CH
3
-CH=CH-CH
3
CH
2
=CH-CH
2
-CH
3
CH
3
-CHOH-CH
2
-CH
3
H
2
O
Его используют в качестве растворителя природных
смол, эфиров целлюлозы, а также для производства мети-
лэтилкетона (МЭК) — ценного растворителя для нитро-
целлюлозы и хлорвиниловых лаков и для депарафинизации
смазочных масел. Метилэтилкетон получают дегидрогени-
зацией, или частичным окислением вторичного бутилового
спирта аналогично тому, как ацетон можно получить из
изопропилового спирта.
CH
3
-CHOH-CH
2
CH
3
CH
3
-CO-CH
2
CH
3
O
2
-H
2
O
Разработаны также способы окисления бутано-бутилено-
вых смесей с целью получения малеинового ангидрида. Пос-
ледний получали раньше парофазным окислением бензола:
CH - CO
CH - CO
O
CH
3
-CH=CH-CH
3
O
2
Малеиновый ангидрид используют для получения не-
которых алкидных смол.
Применение изобутилена
Изобутилен, находящийся в смеси С
4
-углеводородов,
используется для получения метилтретичнобутилового эфи-
ра (МТБЭ), полиизобутилена и бутилкаучука.
Основная область применения изобутилена как от-
дельного нефтехимического продукта – это получение
МТБЭ – компонента бензина, обладающего высоким окта-
новым числом.
CH
3
-C=CH
2
+ CH
3
OH
CH
3
CH
3
-C-O-CH
3
CH
3
CH
3
Присутствие кислорода в молекуле МТБЭ способству-
ет более полному сгоранию бензина в двигателе. В резуль-
327
тате выхлопные газы практически не содержат несгорев-
ших углеводородов.
Процесс получения МТБЭ проводится в реакторе с
твёрдым катализатором – кислотная ионообменная смола,
через который проходит смесь изобутилена и метанола при
температуре 50-95
0
С и давлении 21 атм. В некоторых мо-
дификациях данной технологии в качестве катализатора
используется серная кислота. Выход МТБЭ – 98 %.
Реакция синтеза МТБЭ из изобутилена и метанола
протекает, как и С-алкилирование, по цепному карбоний-
ионному механизму с выделением 66 кДж/моль тепла, а её
равновесие смещается вправо при повышении давления и
снижении температуры.
1. Первой стадией о-алкилирования метанола изобуте-
ном является протонирование последнего гидрид-ионом
кислотного катализатора:
CH
3
-C=CH
2
CH
3
CH
3
-C-CH
3
CH
3
+ H
+
A
-
+
+ A
-
2. Образовавшийся третичный карбониевый ион всту-
пает в реакцию с метанолом (при избытке):
CH
3
-C-CH
3
CH
3
CH
3
-C- OH -CH
3
CH
3
CH
3
CH
3
-C-O-CH
3
CH
3
CH
3
+
+ CH
3
OH
+
-H
+
3. Образовавшийся протон далее реагирует с изобуте-
ном, как и в стадии 1.
4. Причиной обрыва цепи может стать возврат протона
к катализатору
H
+
+ A
-
HA
Помимо основной целевой реакции о-алкилирования,
при синтезе МТБЭ протекают следующие побочные реакции:
– димеризация изобутена с образованием изооктена;
– гидратация изобутилена водой, содержащейся в ис-
ходном сырьё с образованием изобутилового спирта;
– дегидроконденсация метанола с образованием диме-
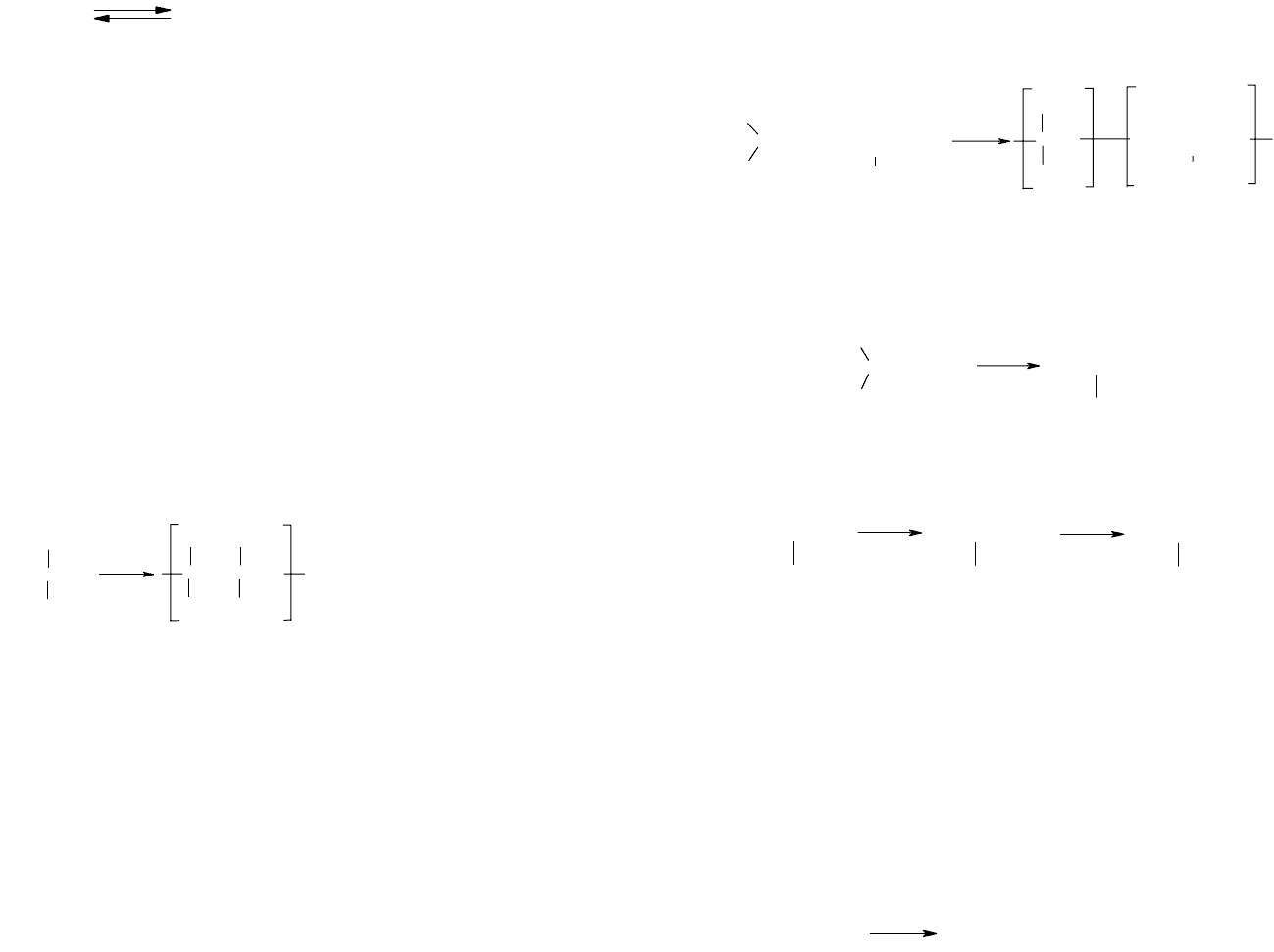
328
тилового эфира:
2CH
3
OH
CH
3
OCH
3
+ H
2
O
– если в метаноле содержится этанол, то образуется
третичный амиловый эфир (ЭТБЭ) и т.д.
Примерно 95 % МТБЭ используется как кислородсо-
держащая присадка к бензину, предназначенная для по-
вышения октанового числа.
В начале XXI века выяснилось, что МТБЭ является за-
грязнителем подземных водоносных пластов. Если резер-
вуар для хранения бензина, содержащего МТБЭ, протекает,
то углеводороды будут располагаться поверх грунтовых
вод или подземного источника воды, в то время как МТБЭ
будет уходить из углеводородного слоя и растворяться в
воде. Он имеет неприятный вкус и, предположительно, яв-
ляется канцерогеном. Кроме того, он вызывает раздраже-
ние глаз и дыхательных путей. МТБЭ имеет низкую темпе-
ратуру вспышки и может быть взрывоопасным.
Изобутилен подвергают полимеризации в присутст-
вии фтористого бора BF
3
при температуре 100
0
С в рас-
творе жидкого этилена
n C=CH
2
CH
3
CH
3
C-CH
2
-C-CH
2
CH
3
CH
3
CH
3
CH
3
n
Полиизобутилены с молекулярной массой ниже 50000
представляют вязкие полужидкие продукты и применяются
в качестве вязкостной присадки к смазочным маслам.
Полиизобутилены с молекулярной массой выше 50000
являются твёрдыми продуктами. Каучукоподобными свой-
ствами обладают полимеры с молекулярной массой
100000-200000.
Отличительными и ценными свойствами полиизобу-
тилена являются высокие диэлектрические показатели и
исключительная стойкость к действию сильных кислот,
щелочей и окислителей.
Изобутилен используется также для производства бу-
329
тилкаучука. При этом изобутилен в присутствии хлористо-
го алюминия, алюминийорганических соединений или
фтористого бора подвергают сополимеризации с 2-3 %
изопрена при температуре -90
0
С.
n C=CH
2
CH
3
CH
3
CH
3
C-CH
2
CH
3
CH
3
CH
3
+ mCH
2
=C-CH=CH
2
n
CH
2
-C=CH-CH
2
m
Этот каучук имеет хорошие механические свойства,
стоек к действию света и химических реагентов, но имеет
малую эластичность при пониженных температурах.
При термическом хлорировании (500
0
С) изобутилена
в газовой фазе получают металлилхлорид:
C=CH
2
+ Cl
2
CH
3
CH
3
CH
2
=C-CH
2
Cl
CH
3
При гидролизе металлилхлорида образуется металли-
ловый спирт, окислением которого получают метакрило-
вую кислоту.
CH
2
=C-CH
2
Cl
CH
3
CH
2
=C-CH
2
OH
CH
3
CH
2
=C-COOH
CH
3
+H
2
-HCl
O
2
-H
2
O
Металлилхлорид применяется в качестве эффективно-
го инсектицида для обеззараживания зерновых, кроме того,
он используется для получения аминов, спиртов, сложных
эфиров, пластмасс и др.
10.3.4. Синтезы на основе бутадиена
В 1932 году впервые в мире был осуществлён промыш-
ленный процесс получения бутадиена по методу Лебедева
из этилового спирта в присутствии катализатора
(Cr
2
O
3
+Al
2
O
3
), обладающего одновременно дегидрати-
рующими и дегидрирующими свойствами.
2C
2
H
5
OH
CH
2
=CH-CH=CH
2
+ 2H
2
O + H
2
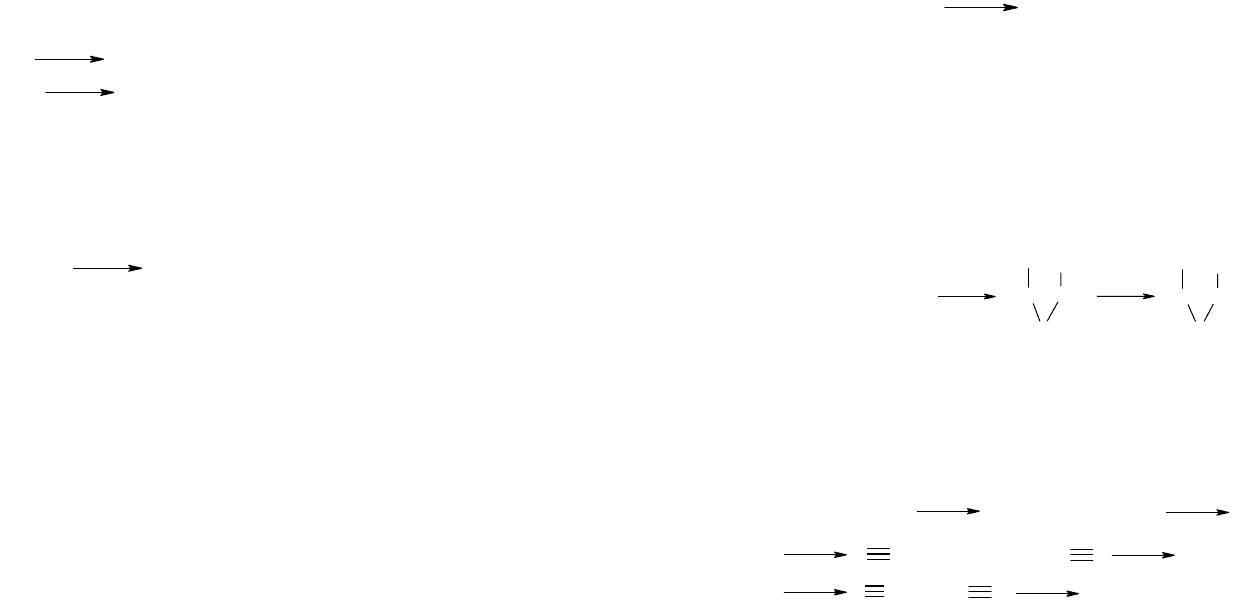
330
В качестве побочных продуктов образуются ацетальде-
гид, бутилены, диэтиловый эфир и другие.
В настоящее время бутадиен получают дегидрировани-
ем бутиленов или одностадийным дегидрированием бута-
на. Кроме того, его выделяют из смесей олефиновых угле-
водородов, получаемых в термических процессах.
Бутадиен получают из бутана и бутилена в присутствии
катализаторов дегидрирования – оксидов или фосфатов
металлов: оксид железа (III), оксид хрома (III) или фосфат
кальция и никеля при температуре 650
0
С и пониженном
давлении.
C
4
H
8
CH
2
=CH-CH=CH
2
+ H
2
C
4
H
10
CH
2
=CH-CH=CH
2
+ 2H
2
Выход бутадиена в этом процессе составляет 60-65 %.
Разработана технология, которая позволяет повысить вы-
ход бутадиена до 89 %. При этом в реактор добавляют не-
которое количество кислорода, чтобы связать выделяю-
щийся водород.
C
4
H
8
CH
2
=CH-CH=CH
2
+ H
2
O
+ 1/2 O
2
Для выделения бутадиена из реакционной смеси, со-
держащей значительное количество других углеводородов
С
4
, используется экстрактивная перегонка. В качестве рас-
творителя применяется N-метилпирролидон и диметил-
формамид.
Cамым дешевым источником бутадиена считается в на-
стоящее время бутиленовая фракция продуктов пиролиза
легкого бензина. Она получается в количестве 10-20 % от
веса сырья и содержит 25-40 % бутадиена. При крупных
масштабах пиролиза и централизованной переработке эта
фракция становится все более важным сырьём для получе-
ния больших количеств бутадиена. Последний можно из-
влекать из фракций методом экстрактивной дистилляции,
используя остальную её часть для каких-либо других целей,
или подвергать её комплексной переработке в бутадиен. В
этом отношении состав С
4
-фракции пиролиза более благо-
приятен, чем полученный при крекинге, так как она содер-
331
жит мало парафинов. При комплексной ее переработке это
позволяет избежать первой стадии дегидрирования, сохра-
няя лишь вторую стадию превращения нормальных бутенов
в бутадиен.
Стоимость бутадиена, выделенного из газов пиролиза,
примерно на 40 % ниже бутадиена, получаемого двухста-
дийным дегидрированием бутана.
75 % бутадиена используется в промышленности для
получения каучуков
n CH
2
=CH-CH=CH
2
n[-CH
2
-CH=CH-CH
2
-]
n
В смеси с другими мономерами получают также бутадиен-
стирольный, полихлоропреновый, нитрильный и другие каучуки.
Эти каучуки в основном используются в производстве
автомобилей – это шины, сальники, изолирующие прокладки.
Бутадиен находит и ряд других применений. Из бута-
диена и сернистого ангидрида с последующим гидрирова-
нием получают сульфолан – селективный растворитель для
экстракции ароматических углеводородов.
CH
2
=CH-CH=CH
2
+ SO
2
CH=CH
CH
2
SO
2
CH
2
CH
2
-CH
2
CH
2
SO
2
CH
2
+H
2
Присоединение одной молекулы хлора к бутадиену с
последующим взаимодействием образовавшегося 1,4-
дихлорбутена-2 с цианистым натрием является одним из
путей производства адипонитрила, а из него — гексамети-
лендиамина, одного из мономеров для получения найлона.
CH
2
=CH-CH=CH
2
ClCH
2
-CH=CH-CH
2
Cl
C-CH
2
-CH=CH-CH
2
-C
N
C(CH
2
)
4
-C
N
H
2
N(CH
2
)
6
NH
2
+Cl
2
2NaCN
+H
2
N
4H
2
N
10.3.5. Синтезы на основе изопрена
Этот продукт может быть получен двухстадийной де-
гидрогенизацией изопентана, содержащегося в попутных
газах и лёгких нефтяных погонах, или одностадийной де-
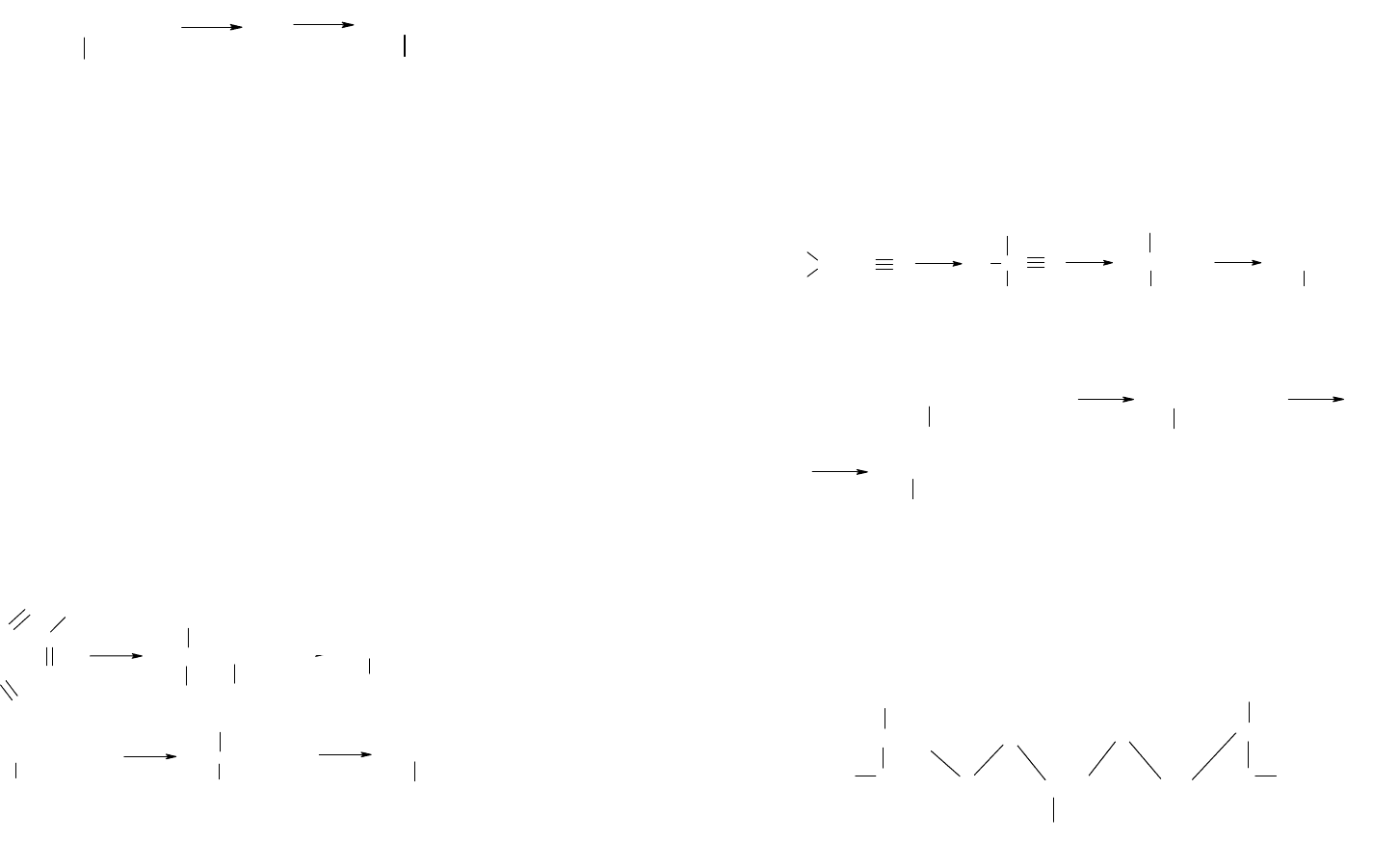
332
гидрогенизацией изопентенов (изоамиленов), образующих-
ся при термическом крекинге. (Процесс аналогичен полу-
чению бутадиена дегидрогенизацией н-бутана и бутенов):
CH
3
-CH-CH
2
-CH
3
CH
3
C
5
H
10
CH
2
=C-CH=CH
2
CH
3
-H
2
-H
2
Однако при этом кажущемся столь простым процессе
трудно получить изопрен высокой степени чистоты, ибо
одновременно образуется много других предельных (ме-
тан, этан, пропан, н-пентан) и непредельных (этилен, про-
пилен, бутилены, н-пентены, пиперилен) углеводородов.
Разработаны процессы получения стереорегулярного
полиизопренового каучука (цис-полиизопрена), практиче-
ски почти идентичного по своим свойствам природному
каучуку и значительно превышающего по качеству поли-
бутадиеновый каучук. Но для этой цели требуется изопрен
высокой степени чистоты.
Поэтому разработаны и другие процессы получения
изопрена. В одном из них сырьём являются изобутилен и
формальдегид. Сначала в присутствии серной кислоты при
20
0
С под небольшим давлением осуществляют конденса-
цию одной молекулы изобутилена с двумя молекулами
формальдегида. Образовавшиеся 4,4-диметил-1,3-диоксан и
в качестве примеси З-метилбутандиол-1,3, в присутствии
катализатора, содержащего фосфорную кислоту, при 220°С
дают изопрен с выходом до 85-95 %:
CH
2
O
O
CH
2
CH
2
C-CH
3
CH
3
CH
2
=C-CH=CH
2
+ CH
2
O + H
2
O
CH
3
CH
3
-C=CH
2
+ CH
2
O
CH
3
CH
3
-C-CH
2
-CH
2
OH
OH
CH
3
CH
2
=C-CH=CH
2
+
CH
3
-C-CH
2
-CH
2
CH
3
O-CH
2
-O-
CH
3
+
20
0
C
H
2
SO
4
220
0
C,
водя ной пар
-H
2
O
2H
2
O
Для этого процесса можно использовать не только
чистый изобутилен, но и бутан-бутиленовую фракцию, по-
лучаемую в процессе каталитического крекинга и содер-
333
жащую 15-20 % изобутилена, или аналогичную фракцию,
получаемую при пиролизе (после извлечения из неё бута-
диена) и содержащую до 35 % изобутилена, поскольку в
реакцию вступает только изобутилен.
Согласно другому процессу конденсируют ацетилен с
ацетоном по методу Фаворского в присутствии твёрдой
щелочи. Реакцию эту удобно проводить в среде жидкого
аммиака, и тогда выход диметилацетиленилкарбинола дос-
тигает 85 %. Затем избирательно гидрируют тройную связь
до двойной, а полученный диметилвинилкарбинол дегид-
ратируют:
CO + HC
CH
3
CH
3
CH
CH
CH
3
C-C
CH
3
OH
CH
3
-C-CH=CH
2
OH
CH
3
CH
2
=C-CH=CH
2
CH
3
KOH
+H
2
-H
2
O
Интересен путь получения изопрена димеризацией
пропилена с последующими изомеризацией и деметаниза-
цией:
CH
2
=CH
2
-CH
3
+ CH
2
=C-CH
2
-CH
2
-CH
3
CH
3
CH
3
-C=CH-CH
2
-CH
3
CH
3
CH
2
=C-CH=CH
2
+ CH
4
CH
3
2
Изопрен применяется для производства синтетическо-
го полиизопренового каучука − аналога натурального кау-
чука. Полимеризация изопрена проводится в присутствии
стереоспецифических катализаторов. Получаемый цис-1,4-
полиизопрен имеет ту же молекулярную структуру, что и
натуральный каучук:
C = CH
CH
3
CH
2
C
H
2
C
H
2
C = CH
CH
3
C
H
2
C = CH
CH
3
C
H
2
CH
2
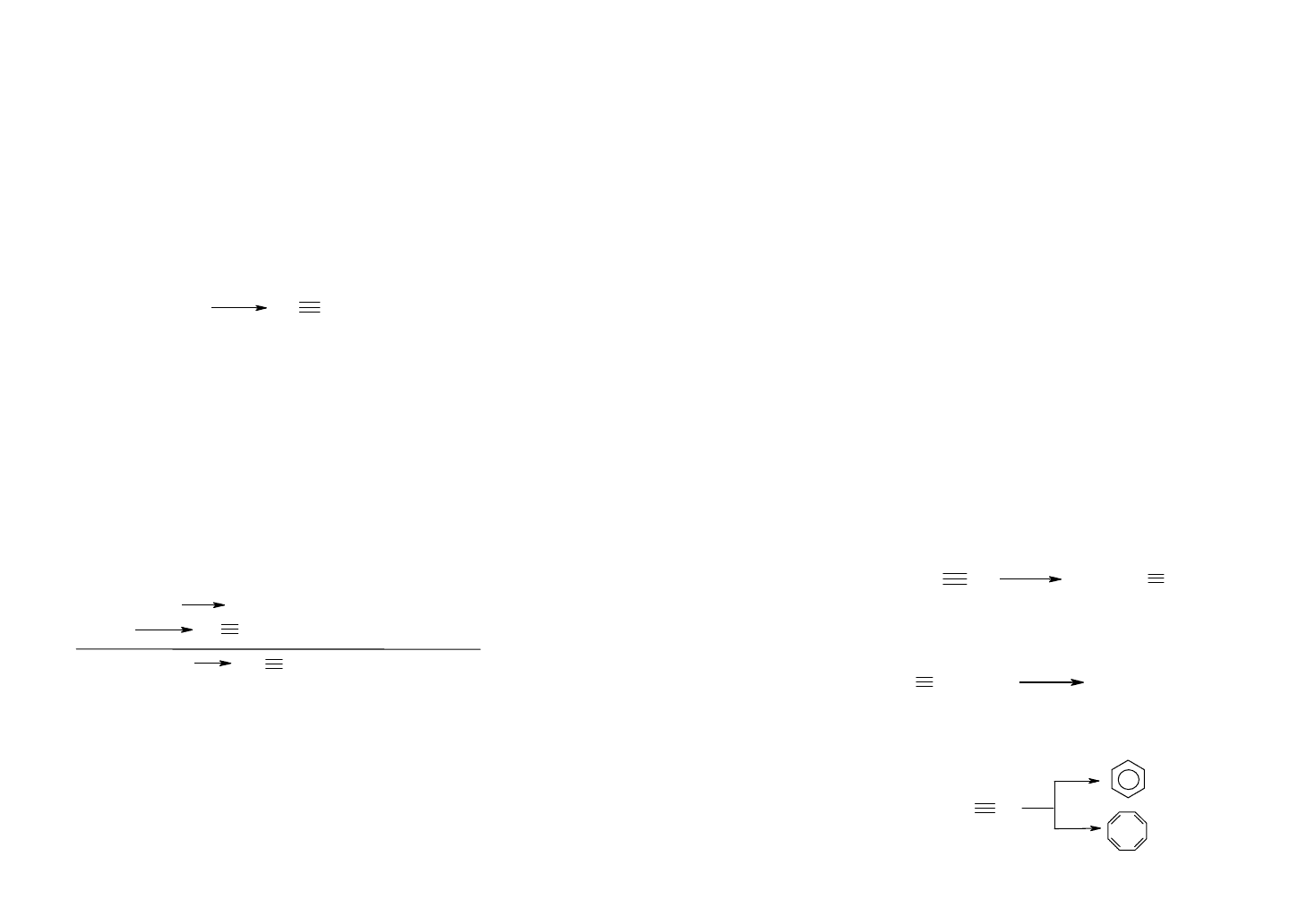
334
10.3.6. Синтезы на основе ацетилена
Старый способ получения ацетилена, по которому и
сейчас производят около 50 % его, это карбидный процесс,
сырьем для которого являются известь и уголь.
Однако значительно более прогрессивным методом
является получение ацетилена из метана или других угле-
водородов. Для получения ацетилена из метана разработан
ряд методов.
Процесс электрокрекинга заключается в том, что ме-
тан пропускают через электрическую дугу, где он распада-
ется и дает ацетилен и водород:
CHCH
2 CH
4
+ 3H2
После кратковременного нагрева до 1400-1600 °С газ
быстро охлаждают. В отходящем газе обычно содержится
не более 12 % ацетилена. Процесс требует значительного
расхода электроэнергии, порядка 12 квт/ч на 1 м
3
ацетиле-
на.
Более перспективным считают окислительный кре-
кинг метана, при котором тепло, затрачиваемое на эндо-
термическую реакцию образования ацетилена из метана,
получают за счёт сгорания части метана в специальных
горелках, где при температуре 1600-2200 °С и образуется
ацетилен;
CH
4
CH
CH
CH
CH
CO + 2H
2
O
+
2CH
4
+3H
2
3 CH
4
+ 3/2 O
2
+ CO + 3H
2
+ 2H
2
O
+ 3/2 O
2
Смесь образующихся одновременно оксида углерода
и водорода после выделения ацетилена представляет собой
синтез-газ — ценное сырьё для ряда синтезов.
Окислительный крекинг этана (и других гомологов
метана) считается более экономичным процессом, чем кре-
кинг самого метана.
Перспективным является также пиролиз углеводоро-
дов в плазме, которая образуется при нагреве газа до очень
высокой температуры. Плазма состоит из заряженных час-
335
тиц — ионов и электронов; физики часто называют плазму
четвертым агрегатным состоянием вещества. На практике в
струю плазмы, образовавшейся из водорода или паров во-
ды в результате прохождения их через электрическую дугу,
пропускают пары бензина или иного углеводородного сы-
рья. При этом до 90 % углеводородов превращаются в
смесь ацетилена и этилена, общее содержание которых в
газе достигает 40 %. Для этого процесса характерны пол-
ное отсутствие сажеобразования и низкий расход электро-
энергии — 4-5 квт/ч на 1 м
3
продукта. Чтобы отделить аце-
тилен, его поглощают жидким аммиаком или диметилфор-
мамидом О=CHN(CH
3
)
2
, в которых этилен не растворяется.
Большое количество ацетилена расходуется для сва-
рочных работ. Но, кроме того, на основе ацетилена осуще-
ствлено огромное количество химических синтезов, многие
из которых нашли промышленное применение.
Ацетилен, благодаря своей высокой реакционной спо-
собности вступает в многочисленные химические реакции
— полимеризации, присоединения, конденсации и др.
Полимеризация ацетилена в зависимости от условий
протекает различно. При пропускании ацетилена через рас-
твор СuCl и NH
4
Cl в соляной кислоте при температуре 80
0
С образуется винилацетилен:
CHCH
CH
2
=CHC
CH
2
Эта реакция имеет большое практическое значение.
Винилацетилен, легко присоединяя НCl, превращается в
хлоропрен (мономер СK):
CH
2
=CHC
CH
CH
2
=CHCCl=CH
2
+ HCl
Возможна полимеризация ацетилена с образованием
циклических соединений (бензола, циклооктатетраена и др.):
CH
n HC
t
Cu
Полимеризационные превращения ацетилена и его за-
мещённых являются эффективными и экономически вы-
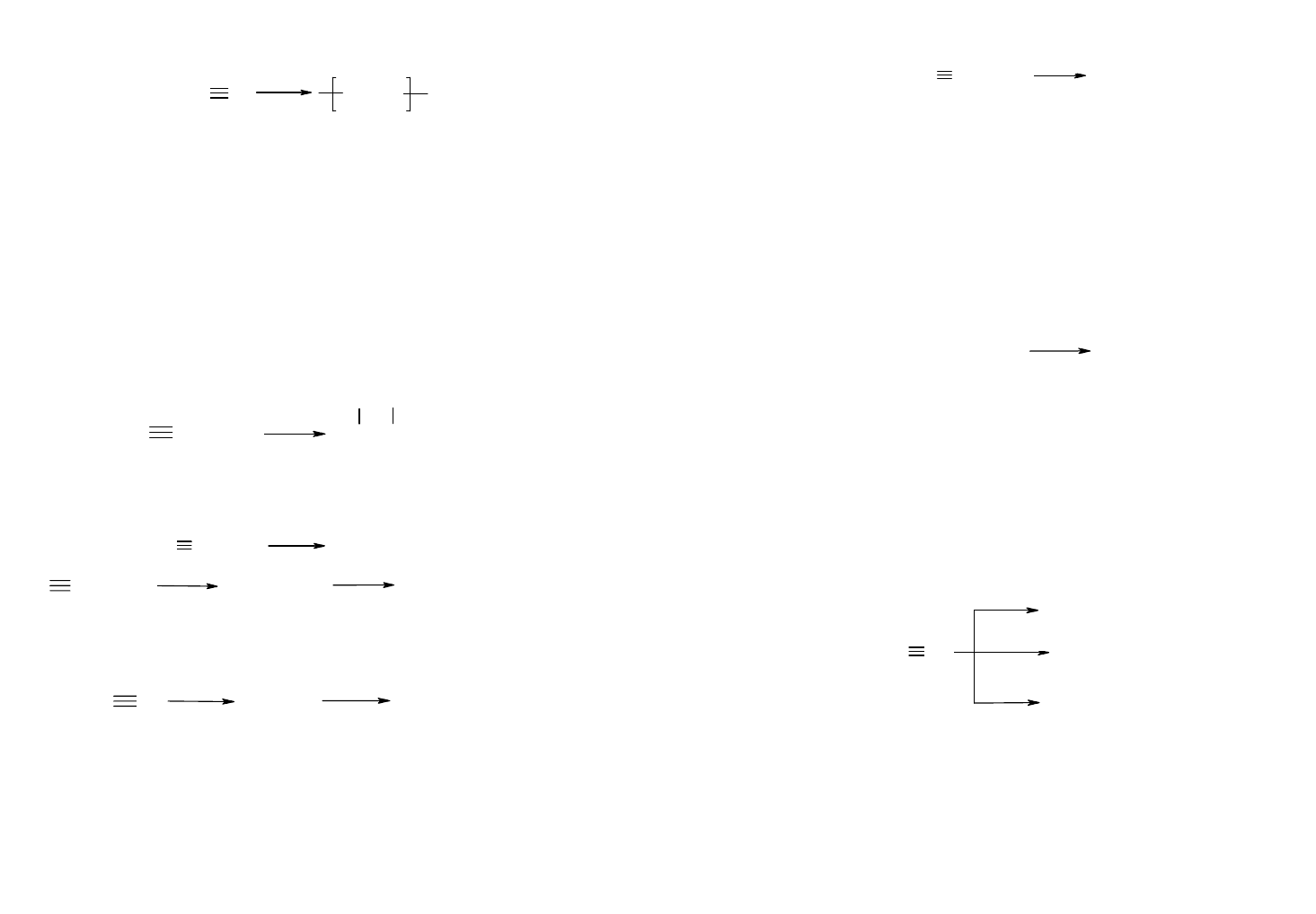
336
годными способами получения полимеров, содержащих в
макромолекулах достаточно протяжённые участки с со-
пряжёнными связями.
CH
CH=CH
n
n CH
Такие полимеры называются полисопряжёнными сис-
темами (ПСС). Они обладают необычными свойствами —
высокой проводимостью, фоточувствительностью, катали-
тической активностью и др.
Изменяя условия полимеризации, можно получать ли-
нейные полимеры ацетилена различной степени кристал-
личности. На их основе получены материалы, обладающие
металлической проводимостью. Они получили название
органических металлов.
Присоединение галогенов к ацетилену используется
для синтеза ряда растворителей:
CH +CH
Cl-CH-CH-Cl
Cl
Cl
2 Cl
2
Гидрохлорированием ацетилена в промышленности
получают винилхлорид — мономер, служащий сырьем для
изготовления пластических масс:
CH
CH
CH
2
=CHCl
+ HCl
HgCl
2
CH + HgCl
2
CHCl=CHHgCl
CH
+HCl
CH
2
=CHCl + HgCl
2
Аналогичным образом к ацетилену присоединяется
фтористый водород в присутствии ртутных катализаторов,
нанесённых на активированный уголь.
CH
CH
2
=CHF
CH
+HF
CH
3
-CHF
2
+HF
В этом процессе наряду с фтористым винилом получа-
ется также этиленфторид: при пиролизе при температуре
700
0
С в присутствии медного катализатора он превраща-
ется в винилфторид. При полимеризации винилфторида
образуются тепло- и светостойкие плёнки.
При гидратации ацетилена образуется ацетальдегид.
Реакция протекает при каталитическом действии солей
337
ртути (была открыта М. Г. Кучеровым и обычно называет-
ся его именем) :
CH
CH
CH
3
-CHO
+ H
2
O
Hg
2+
Ядовитость солей ртути и их летучесть делают этот
процесс нежелательным с точки зрения техники безопасно-
сти, что и вызвало поиски других, не ртутных катализато-
ров гидратации ацетилена. Хорошие результаты даёт при-
менение кальцийкадмийфосфатного катализатора, однако в
настоящее время в промышленности основное количество
ацетальдегида производится окислением этилена.
Окислением ацетальдегида кислородом воздуха в при-
сутствии марганцевых и никелевых катализаторов получа-
ют уксусную кислоту и уксусный альдегид.
CH
3
COOH
CH
3
CHO +
1/2O
2
В настоящее время уксусную кислоту получают также
жидкофазным окислением бутана или прямогонных бензи-
нов.
Ацетальдегид является сырьём для производства ук-
сусной кислоты, её эфиров и других ценных продуктов.
Реакции винилирования — присоединения к ацетиле-
ну соединений с подвижным атомом водорода — исполь-
зуют как способ получения виниловых эфиров, винилаце-
тата, акрилонитрила:
CH
CH
CH
2
=CHOR
CH
2
=CHOCOCH
3
CH
2
=CHCN
HCN
CH
3
COOH
ROH
Винильная группа в продуктах реакции придаёт им
способность к полимеризации, поэтому они используются
как мономеры для производства пластических масс. Наи-
большее значение имеют простые виниловые эфиры
CH
2
=CHOR, винилацетат СН
2
=СНОСОСН
3
, акрилонитрил
CH
2
=CHCN.
Конденсация с карбонильными соединениями приво-
дит к образованию алкиновых спиртов и гликолей. Таким
