Кобзев. Г.И. Применение неэмпирических и полуэмпирических методов в квантово-химических расчетах
Подождите немного. Документ загружается.

11
Теплота образования молекулы Е
h
выражается через теплоты образования
атомов
∆Η
f
и энергию связи Е
СВЯЗИ
:
E
h
= E
СВЯЗИ
-
∑
А
Н
f
A
. (36)
Как и МЧПДП/1, метод МЧПДП/2 предназначен для расчета молекул,
содержащих только атомы Н,С,О,N.
1.1.2.1 Приближение МЧПДП/3 (MINDO/3)
Метод, созданный Дьюаром, позволяет производить расчеты любых
молекул, содержащих до 10 различных атомов, требует 93 атомных и 66
молекулярных параметров. Он применяется для расчетов молекул и
комплексов, содержащих элементы 2, 3 и 4 периодов с замкнутой оболочкой.
Для расчетов систем с незамкнутой оболочкой применимы методы
ограниченного и неограниченного Хартри – Фока (ОХФ, HХФ).
Для незамкнутых оболочек волновая функция не является собственной
функцией оператора
∧
S
z
, однако собственные значения S
z
мало отличаются
от истинных ожидаемых значений.
Метод МЧПДП/3 представляет собой дальнейшее развитие методов
МЧПДП, которое состоит, прежде всего в расширении ассортимента атомов,
составляющих молекулы, до десяти (Н,В,С,N,O,F,Si,P,S,Cl). При этом
воспроизведение экспериментальных теплот образования и геометрии
молекул осталось достаточно хорошим. Оценка интегралов производится
здесь так же, как и в методе МЧПДП/2.
Для интегралов остова выбрано выражение (59). Особенностью метода
МЧПДП/3 является то, что орбитальные экспоненты здесь также
параметризуются, и они значительно отличаются от тех, которые
определяются по правилам Слейтера или на основе неэмпирических
расчетов. Кроме того, в выражении для интегралов отталкивания остовов
экспоненциальный множитель в случае пар атомов NH и NO заменяется на
α
АВ
ехр(-R
АВ
). Полная энергия молекулы, энергия связи и теплота
образования вычисляются по формулам (65-75).
Уравнение Рутаана решают методом самосогласованного поля, при этом
быстрота сходимости зависит от выбора базисных функций. В большинстве
полуэмпирических методах используют АО - Слейтера:
χ
nlm
= R
n
СЛ
(r)Y
I
m
(θϕ). (37)
Здесь Y
1
(θϕ)- сферические гармоники атома водорода.
Орбитальная слейтеровская часть имеет вид:

12
R
n
СЛ
=C·n
*
-1
n-1
exp(-
0
a
r
эфф
Z
s
), (38)
где
n
s
- эффективное квантовое число;
Z
эфф
=Z-σ - эффективный заряд ядра ;
σ - константа экранирования, определяемая по правилам Слейтера.
При использовании слейтеровского базиса возникают большие трудности
при расчете обменных интегралов. Эти интегралы в ab initio методах удается
свести к одноцентровым, используя гауссовский базис, где АО имеют вид:
χ=Cχ
a
Y
B
Z
c
exp(-αx
2
-βy
2
-γz
2
) (39)
Число полученных в результате расчета МО равно числу АО
используемого базиса. Каждая МО, согласно принципу Паули, может быть
занята двумя электронами со спаренными спинами; оставшиеся вакантные
(виртуальные) МО основного состояния Малликен предложил использовать
для описания возбужденных состояний молекулы. Известно, что АО
Слейтера удовлетворяют условиям быстрой сходимости, если основное
состояние имеет спин S=0,1… .
В случае, когда основное состояние имеет спин S=1/2 и орбитально не
вырождено, для нахождения энергии основного состояния дублетов или
квартетов применим метод Лонге-Хиггинса-Попла. В приближении ЧПДП, с
введением модификации для P
µν
вида:
P
µν
=2
∑
m
i
C
iµ
C
iµ
+C
µm
C
νm
, (40)
энергия дублетного состояния запишется:
2
E
0
=1/2∑P
µν
(F
µν
+H
µν
)1/4(mm|mm). (41)
Дьюар с сотрудниками вывел формулы метода ЛХП, основываясь на
концепции метода половинок электронов. Эллисон и Матео обобщили этот
метод, включив открытые оболочки с дважды вырожденными МО. Формулы,
позволяющие рассчитывать мультиплеты в линейных молекулах, имеющих
конфигурацию
σ
m
π
m
, где m=1,2; n=1,2,3, можно получить, вводя
дополнительные члены к методу закрытых оболочек. Так же, как и в методе
ЛПХ, изменения и в этом случае будут связаны с матрицей Р
µν
и полной
энергии:
P
µν
=2
∑
ЗАП
i
C
i
µC
i
ν+2f
∑
k
C
µk
C
νk
, (42)
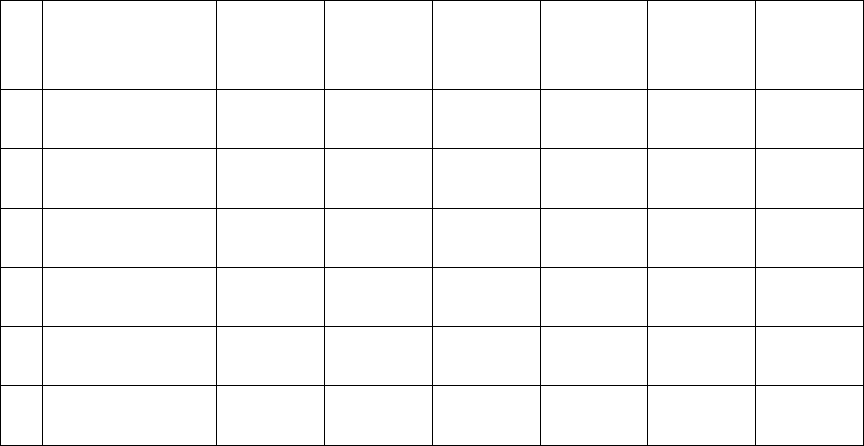
13
E=1/2
∑
µν
P
µν
(H
µν
+F
µν
)+a(kk|kk)+b(ll|ll)+c(kk|ll)+(kl|kl). (43)
Константы a,b,c,d,f, зависящие от спина и от заселения вырожденных МО
φ
K
и
φ
l
, приведены в таблице1.
Таблица 1 Значения параметров a,b,c,d,f в методе полуэлектронов
N Конфигурац
ии
Спин F a b C d
1
ϕ
K
±
||
l
1/2 ¼ -1/16 -1/16 -1/4 1/8
2
ϕ
K
ϕ
l
1 ½ -1/4 -1/4 0 -1/2
3
ϕ
K
2
ϕ
l
2
0 ½ -1/4 -1/4 0 3/2
4
ϕ
K
2
-ϕ
l
2
0 ½ 1/4 1/4 -1 -1/2
5
ϕ
K
2
+ϕ
l
2
0 ½ 1/2 1/4 -1 3/2
6
ϕ
K
2
ϕ
l
±ϕ
K
ϕ
l
2
1/2 ¾ -1/16 -1/16 -1/4 1/8
Если ϕ
К
и ϕ
l
являются π
x
и π
y
орбиталями в линейной молекуле, то
конфигурации 3 и 4 имеют одинаковую энергию и соответствуют
1
∆
g
состоянию, что легко показать, учитывая, что
(xx
|yy)(xx|xx)=-2(xy|xy). (44)
Различные варианты метода МЧДП (MINDO) (модифицированный
метод частичного дифференциального перекрывания) MINDO/1, MINDO/2,
MINDO/3, созданы Дьюаром с сотрудниками на основе метода ЧПДП
(INDO) Попла и ОПДДП и являются более усовершенствованными
методами, которые позволяют более точно вычислять максимальное число
физических свойств.
В каждой последующей модификации улучшалась параметризация,
которая позволяла при умеренных затратах машинного времени в пределах
экспериментальной (химической) точности исследовать большие
органические молекулы, включающие атомы 2, 3 и даже 4-го периодов.
Одноцентровые интегралы в MINDO/3 не вычисляются аналитически, а
задаются как параметры по методу Олеари. Эти параметры, так же как и
параметры, при помощи которых вычисляют резонансные интегралы,
выбирались так, чтобы наиболее точно воспроизвести экспериментальный
результат (например, по теплоте образования и геометрии молекул).
Необходимо помнить, что при расчетах методом КВ, корреляция
электронов учитывается дважды, поскольку непроизвольно заложена в
цифры параметров MINDO/3. Метод MINDO/3 считается одним из лучших
полуэмпирических методов вычислительной химии.

14
Несмотря на то, что параметризация метода МЧПДП/3 (MINDO/3)
позволяет достаточно точно рассчитывать геометрию (на основе
оптимизации энергии), энергии связи, энергии МО и теплоты образования
для молекул 2-4 периодов, в ряде случаев аппроксимация обменных
взаимодействий отталкивания потенциалом отталкивания остовов вида:
V
OCT
AB
= [ λ
AB
R
I
AB
+( I - λ
AB
)
γ
AB
] , где
γ
AB
= exp (-α
AB
R
AB
),
не позволяет верно учесть пренебрежение членами порядка S
2
в фокиане.
Однако результаты расчетов для большинства бимолекулярных реакций
хорошо согласуются с экспериментальными данными.
Как и всякий полуэмпирический метод, MINDO/3 имеет свои
ограничения, достоинства и недостатки, которые неоднократно отмечались
авторами. Параметризация MINDO/3 и ее особенности рассмотрены в книге
Щембелова.
Несмотря на то, что, как указывается Дьюаром, при расчетах
ароматических систем MINDO/3 дает ложные высоколежащие
сигма -
орбитали, метод может успешно применяться для интерпретации
фотоэлектронных спектров.
При рассмотрении качественных результатов и количественных оценок
эффектов СОВ необходимо учитывать, что в методе MINDO/3 энергии
возбужденных
π-состояний всякой химической системы занижены.
Известно, что завышение полной энергии
π
-структур в MINDO/ 3
связано с аппроксимацией интегралов электрон – ядерного взаимодействия
(32)
<X
µ
A
| V
B
| X
µ
A
> = Z
B
γ
AB
. (45)
1.2 Метод КВ
Уравнения Рутаана представляют собой систему линейных уравнений,
для решения которой необходимо приравнять к нулю детерминант системы:
∑
ν
C
iν
(F
µν
-εS
µν
)=0, (46)
|F
µν
-εS
µν
|=0, (47)
F
µν
=H
µν
+G
µν
, (48)
S=
∫χ
µ
A
(1)χ
ν
B
(1) dV(1), (49)

15
H
µν
=∫χ
µ
*(1)[-
2
2
2
i
m
h
∇
-e
A
2
∑
A
r
A
Ze
1
2
]χ
µ
(1) dV
1
, (50)
G
µν
=
∑∑
l
k
P
K,l
[(µν|Kl)-1/2(µl|Kν)], (51)
(
µν|Kl)=e
2
∫χ
µ
(1)χ
ν
(1)|
12
1
r
|χ
K
(2)χ
1
(2)dV
1
dV
2
, (52)
P
K,l
=2∑C
i,K
*C
i,1
. (53)
Поскольку матричный элемент фокиана - F
µν
содержит коэффициенты
ЛКАО разложения (С
ιµ), решение проводят методом итераций, в результате
чего получают минимизированные энергии МО и набор коэффициентов
ЛКАО разложения (С
ιµ) для каждой МО. Базис АО, первоначально
используемых для расчета первых значений орбитальных энергий в
MINDO/3, является Слейтеровским. При промотировании одного или
нескольких электронов с занятых МО на свободные, получим возбужденные
электронные конфигурации. Каждая такая конфигурация может быть
описана одним или суммой детерминантов. При переносе одного электрона с
занятой i-МО на свободную j-МО синглетная и триплетная волновые
функции могут быть записаны:
1′3
Ψ
in
0
=1/2[ϕ
1
ϕ
1
…ϕ
i
ϕ
n
…ϕ
n
ϕ
n
]±[ϕ
1
ϕ
1
…ϕ
i
ϕ
n
…ϕ
n
ϕ
n
]=1/2{|in |±|i n |}, (54)
3
Ψ
i-u
-1
=|iu|,
3
Ψ
i-u
-1
=|ik| (55)
Где i,j- индексы, нумерующие занятые МО; u,
ν-вакантные МО;
i=
ϕ
i
α - молекулярная спин-орбиталь с электроном, имеющим спин α:
ϕ
i
=∑С
iµ
χ
µ
-МО, где χ
µ
- АО. (56)
Здесь
µ-индекс, нумерующий атомные орбитали.
i=
ϕ
i
β - молекулярная спин-орбиталь с электроном, имеющим спин β.
Для основного синглетного состояния невырожденного орбитально
L=0 с полным спином S=0 можно опустить заполненную оболочку,
1
Ψ
0
=|ϕ
1
ϕ
1
ϕ
2
ϕ
2
...ϕ
i
ϕ
i
|≡|ii|
поскольку она не дает вклада в матричные элементы одноэлектронного
оператора и не влияет на симметрию полной волновой функции.
Волновая функция в методе КВ записывается в виде линейной
комбинации слейтеровских определителей, отвечающих различным
электронным возбужденным конфигурациям:

16
Ψ=
∑
m
K
Α
k
Ψ
k
, Ψ=
!
1
N
Ψ
1
…Ψ
n
, (57)
Где
Ψ
i
=ϕ
i
σ
i
; ϕ
i
и σ
i
- пространственная и спиновая части, М-число
учитываемых конфигураций.
Коэффициенты А
k
можно найти, воспользовавшись вариационным
методом. При этом выражение для полной волновой функции (56)
подставляется в формулу (24) и проводится минимизация по коэффициентам
А
k
и С
iµ
в разложении МО ЛКАО. В результате получаются уравнения, из
которых находят A
kl
и полные энергии электронных конфигураций:
Η
kl
-ES
kl
=0, (58)
∑
k
Α
kl
(H
kl
-ES
kl
)=0. (59)
Матричные элементы гамильтониана Н
kl
и матрицы перекрывания S
kl
даются выражениями:
H
kl
=∫Ψ
k
ĤΨ
1
dV, S
kl
=∫Ψ
k
Ψ
1
dV. (60)
Весь расчет КВ выполняется следующим образом: проводят
самосогласованное решение уравнения Рутаана, затем полученные
коэффициенты С
iµ
и энергии Е используются для вычисления матричных
элементов Н
kl
. После этого решают систему (59) и находят коэффициенты А
kl
и энергию возбужденных состояний.
Рассмотрим приближение, в котором учитываются только однократно
возбужденные конфигурации. Оно особенно часто используется в рамках
полуэмпирических методов. Волновую функцию системы, в которой кроме
дважды занятых имеются две однократно занятые МО
Ψ
k
и Ψ
i
, можно
записать в виде четырех различных спин-орбитальных конфигураций:
Ψ
1
=
!2
1
N
Ψ
1
α Ψ
1
β…Ψ
i
αΨ
k
α…Ψ
n
αΨ
n
β, (61)
Ψ
2
=
!2
1
N
Ψ
1
α Ψ
1
β…Ψ
i
βΨ
k
α…Ψ
n
αΨ
n
β,
Ψ
3
=
!2
1
N
Ψ
1
α Ψ
1
β…Ψ
i
αΨ
k
β…Ψ
n
αΨ
n
β,
Ψ
4
=
!2
1
N
Ψ
1
α Ψ
1
β…Ψ
i
βΨ
k
β…Ψ
n
αΨ
n
β, (62)
Синглетному состоянию (S=0) отвечает линейная комбинация:

17
0
Ψ
ik
=
2
1
(Ψ
2
-Ψ
3
). (63)
Триплетному состоянию (S=1) отвечают три вырожденные функции:
Ψ
1
- М
s
=1
Ψ
ik
= (Ψ
2
+Ψ
3
) M
s
=0 (64)
Ψ
4
- M
s
=-1
Для решения секулярной задачи (59) необходимо знать матричные
элементы (60). Матрица S диагональная. В общем случае выражение для
гамильтониана имеет очень сложный вид. Для однократно возбужденных
конфигураций справедлива теорема Бриллюэна, согласно которой матричные
элементы между конфигурациями
Ψ
0
и Ψ
k
равны нулю, если Ψ
k
описывает
однократно возбужденную конфигурацию. Применение этой теоремы
существенно уменьшает вычислительные трудности. Окончательный вид
матричных элементов между различными S-S и T-T состояниями таков:
<
0
Ψ
ik
|Ĥ|
1
Ψ
ik
>=Ε
0
+Ε
k
−Ε
i
−<ii/kk>+2<ik/ik>, (65)
<
1
Ψ
ik
|Ĥ|
1
Ψ
ik
>=Ε
0
+Ε
k
−Ε
i
−<ii/kk>, (66)
<
0
Ψ
ik
|Ĥ|
0
Ψ
ij
>=−<ij/kl>+2<ik/jl>, (67)
<
1
Ψ
ik
|Ĥ|
1
Ψ
jl
>=−<ij/kl>, (68)
где Е
0
– энергия основного состояния, Е
k
и Е
i
- энергии МО Ψ
k
и Ψ
i
.
Интегралы межэлектронного отталкивания вычисляются по формуле
<ij/kl>=∫∫Ψ
i
(1)Ψ
j
(1)
12
2
r
e
Ψ
k
(2)Ψ
l
(2)dV
1
dV
2
, (69)
Метод КВ с учетом только однократно возбужденных конфигураций,
несмотря на свою простоту, достаточно хорошо качественно описывает
свойства возбужденных состояний. Метод КВ удобен тем, что в результате
одного расчета мы получаем информацию с широким спектром электронных
переходов. Но при этом существенным недостатком является то, что при
расчете энергии возбужденных состояний мы используем самосогласованные
орбитали основного состояния, но после процедуры КВ самосогласование
исчезает. Вторым недостатком этого подхода является то, что все расчеты
ведутся при равновесной геометрии основного состояния, то есть не
учитывается возможное изменение молекулярной геометрии при
возбуждении.

18
1.3. Спин-орбитальное взаимодействие (СОВ) в молекулах
1.3.1. Оператор СОВ в молекулах и спиновые функции
Спин-орбитальное взаимодействие (СОВ) является релятивистским
эффектом, учет которого осуществляется введением в полный гамильтониан
Ĥ оператора Ĥ
so
, определяемого формулой (70). Оператор СОВ можно
приближенно представить в виде:
Ĥ
so
=
∑
А
ξ
nl
A
∑
t
l
iA
Ŝ
i
=
∑
i
i
Β
€
Ŝ
i
.
(70)
Перепишем (54, 55) с учетом КВ по формуле (57), разделяя
орбитальные и спиновые переменные:
λΨn(ms)=
∑
ki,
λΑikλΨik(x,y,z)λΩm(σ).
(71)
Здесь заполненная МО опускается, так как она не дает вклады в
матричные элементы одноэлектронного оператора
i
Β
€
Ŝ
i
, который будет
использоваться в дальнейшем.
Ψ
ik=
2
1
[ϕ
i
(1)ϕ
k
(2)±ϕ
i
(2)ϕ
k
(1)], (72)
λΩm=
2
1
[α(1)β(2)±α(2)β(1)],
(73)
3
Ω
1
=α(1)α(2),
3
Ω
1
=β(1)β(2)
(74)
В выражениях (72) и (73) верхний знак соответствует
λ=1, нижний -
λ=3. При отсутствии внешнего магнитного поля учет внутренних магнитных
взаимодействий (ССП-СОВ) приводит к тому, что триплетные спиновые
функции (74), можно представить в виде:
3
Ω
x
=
2
1
(
3
Ω
-1
-
3
Ω
1
),
(75)
3
Ω
y
=
2
1
(
3
Ω
-1
+
3
Ω
1
),
3
Ω
z
=
3
Ω
0
,
(76)
для которых спин квантован по осям x, y, z
1.3.2. Вычисление матричных элементов оператора H
so
и B
ij
Матричные элементы оператора СОВ между синглетными и
триплетными состояниями (72-74) равны:
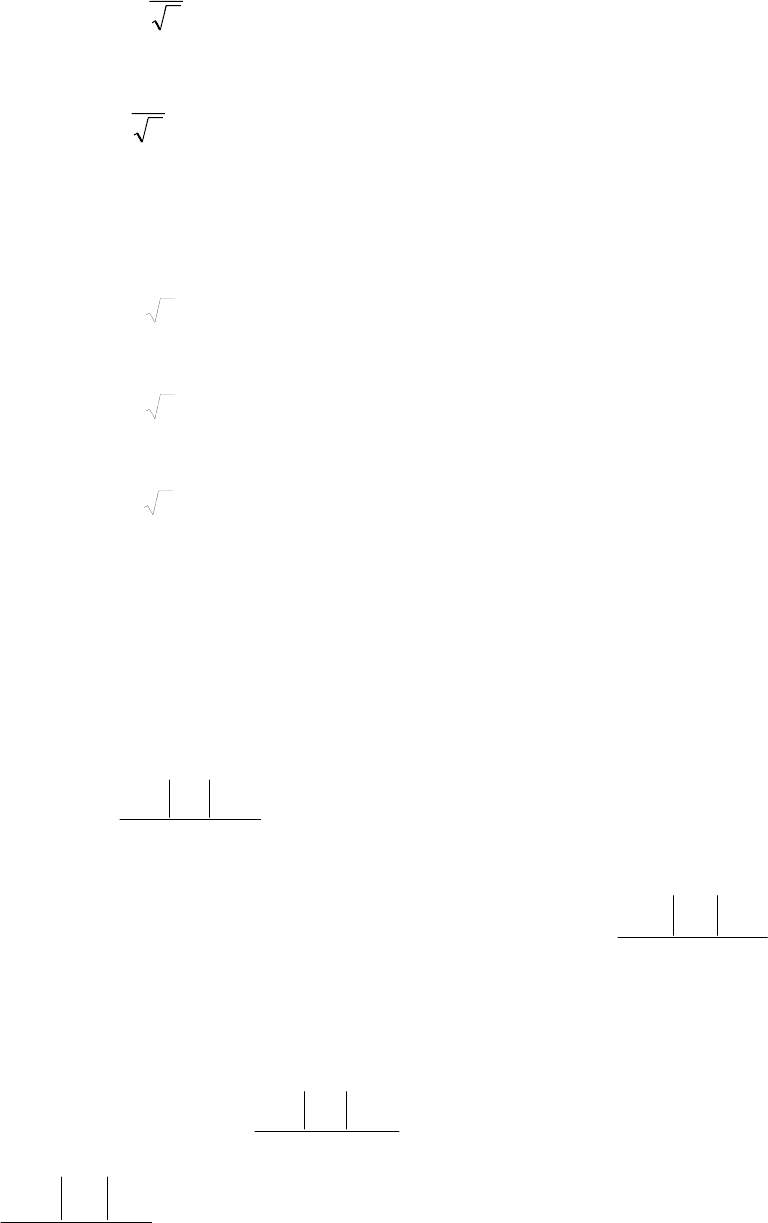
19
<
1
Ψ
0
|Ĥ
so
|
3
Ψ
q
a
>=-
2
1
∑
ki
A
,
ik,q
B
ik
a
,
(77)
<
1
Ψ
ik
|Ĥ|
1
Ψ
jl
>=-
2
1
[
∑
i
k
∑
jk
1
A
ik,p
3
A
jk,1
B
ij
a
-
∑
i
k
∑
il
1
A
ik,p
3
A
jl,1
B
kl
a
],
78)
где а = x, у, z.
Орбитальные интегралы В
ij
для s,p – базиса в одноцентровом
приближении сводятся к виду:
В
ij
x
=<ϕ
i
|Β
€
x
|ϕ
j
>= 2
∑
А
ξ
nl
A
(C
zi
A
C
yj
A
-C
zj
A
C
yi
A
),
(79)
В
ij
y
=<ϕ
i
|Β
€
y
|ϕ
j
>= 2
∑
А
ξ
nl
A
(C
xi
A
C
zj
A
-C
zi
A
C
xj
A
),
(80)
В
ij
z
=<ϕ
i
|Β
€
z
|ϕ
j
>= 2
∑
А
ξ
nl
A
(C
yi
A
C
xj
A
-C
zi
A
C
yj
A
).
(81)
1.3.3. Использование теории возмущений для расчета
характеристик запрещенных S
0
-T
1
переходов
Известно, что оператор (СОВ) смешивает состояния различной
мультиплетности. Используя обозначения
λ
Ψ
m
для волновой функции (72, 73)
при учете СОВ в первом порядке теории возмущения имеем:
3
Ψ
~
i
a
=
1
Ψ
i
+
Ψ
~
∑
Ε−Ε
〉ΨΗΨ〈
p
p
a
sop
13
1
1
3
€
1
1
Ψ
p
,
(82)
1
Ψ
~
0
=
1
Ψ
0
+
∑
Ε−Ε
〉ΨΗΨ〈
q
q
so
a
q
3
0
1
0
1
€
3
3
Ψ
q
a
(83) Дипольный момент перехода T
1
-S
0
при учете СОВ становится отличным
от нуля, поскольку он "заимствует" интенсивность из разрешенных S
n
-S
0
и
T
p
-T
1
переходов:
Q
01
a
=<
1
Ψ
0
|e
∑
k
k
r
r
|
3
Ψ
1
a
>=
∑
Ε−Ε
〉ΨΗΨ〈
n
p
a
son
3
0
1
1
3
€
3
<
1
Ψ
0
|e
∑
k
k
r
r
|
3
Ψ
n
>+
+
∑
Ε−Ε
〉ΨΗΨ〈
p
po
so
a
p
31
0
€
3
<
3
Ψ
p
a
|e
∑
k
k
r
r
|
3
Ψ
1
a
> (84)
Формулу (114) перепишем в виде:
∑
=
=
0
1
n
a
O
Q
r
l
n1
a
∑
+
p
On
Q
r
1
C
Op
a
p
Q
1
3
r
,
(85)

20
C
op
a
=
p
a
pso
Ε−Ε
〉ΨΗΨ〈
3
0
1
3
€
0
1
,
(86)
l
n1
a
=
n
a
son
Ε−Ε
〉ΨΗΨ〈
1
1
3
1
3
€
1
.
(87)
Если молекула имеет электрический дипольный момент в основном
состоянии (
1
Q
00
), то члены при n=0 и p=1 в (84) также дают вклад, и формула
(84) может быть записана в виде:
Q
01
a
=
∑
=1n
1
l
n1
a 1
∑
=
+
2p
on
Q
r
1
C
op
a3
Q
1p
+C
01
(
11
3
00
1
QQ
r
r
+
).
(88)
При температуре Т≤4. 2
°К каждый уровень нулевого поля ведет себя
как независимый осциллятор и интенсивность 0, 0 – вибронной полосы S
0
→T
1
а
перехода определяется силой осциллятора:
f
a
=
2
01
2
3
01
~
8
a
Q
he
cm
r
ν
π
=1.085×10
-5
, (89)
где
01
~
ν
= (
3
Е
1
-
1
Е
0
) – частота перехода в см
-1
. Излучательное время
жизни УНП Т
1
а
(τ
р
а
) определяется формулой:
τ
0
а
=
)
10
(
~
)
10
(
1
5.1
2
01
3
01
~
4
84
3
2
01
~
22
8
TSTSf
q
a
Q
h
a
fe
mc
ν
νπ
νπ
==
r
,
(90)
где g
1
– статистический вес триплета.
Таким образом, задача нахождения вероятности молекулярных
интеркомбинационных переходов сводится к определению доли синглетного
состояния в номинально триплетном состоянии и доли триплетного
состояния в номинально синглетном.
Для синглет-синглетных переходов из основного состояния в Р-тое
возбужденное, проекция момента на ось (r) определяется:
Q
Op
(r)
=
∑
ui,
2
1
A
iup
q
iu
( r)
,
(91)
где q
iu
( r)
=e∫<ϕ
i
|r|ϕ
u
>dr r=x,y,z
(92)
Поставляя в (92) выражение для МО (13), получим, например, для r=х:
