Билеты по общей и неорганической химии
Подождите немного. Документ загружается.

НЕОРГАНИЧЕСКАЯ ХИМИЯ
1. Важнейшие классы неорганических соединений: оксиды, гидроксиды, кислоты,
соли.
Окси́д (о́кисел, о́кись)— соединение химического элемента с кислородом, в котором сам
кислород связан только с менее электроотрицательным элементом. Химический элемент кислород
по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все
соединения химических элементов с кислородом. К исключениям относятся, например, дифторид
кислорода OF
2
.
В зависимости от химических свойств различают:
СОЛЕОБРАЗУЮЩИЕ ОКСИДЫ:
основные оксиды – оксиды, образующие соли и воду при взаимодействии с кислотами или
кислотными оксидами (например, оксид натрия Na
2
O, оксид меди(II) CuO): оксиды металлов,
степень окисления которых I—II;
Химические свойства: Основные оксиды
1. Основный оксид + кислота = соль + вода
CuO + H
2
SO
4
= CuSO
4
+ H
2
O
2. Сильноосновный оксид + вода = щелочь
CaO + H
2
O = Ca(OH)
2
3. Сильноосновный оксид + кислотный оксид = соль
CaO + Mn
2
O
7
= Ca(MnO
4
)
2
Na
2
O + CO
2
= Na
2
CO
3
4. Основный оксид + водород = металл + вода
CuO + H
2
= Cu + H
2
O
кислотные оксиды – оксиды, растворяющиеся только в щелочах, с образованием соли и воды.
Образуются типичными неметаллами и некоторыми переходными элементами (например, оксид
серы(VI) SO
3
, оксид азота(IV) NO
2
): оксиды металлов со степенью окисления V—VII и оксиды
неметаллов;
Химические свойства: Кислотные оксиды
1. Кислотный оксид + вода = кислота
SO
3
+ H
2
O = H
2
SO
4
Некоторые оксиды, например SiO
2
, с водой не реагируют, поэтому их кислоты получают
косвенным путём.
2. Кислотный оксид + основный оксид = соль
CO
2
+ CaO = CaCO
3
3. Кислотный оксид + основание = соль + вода
SO
2
+ 2NaOH = Na
2
SO
3
+ H
2
O
Если кислотный оксид является ангидридом многоосновной кислоты, возможно образование
кислых или средних солей:
Ca(OH)
2
+ CO
2
= CaCO
3
↓ + H
2
O
CaCO
3
+ CO
2
+ H
2
O = Ca(HCO
3
)
2
4. Нелетучий оксид + соль1 = соль2 + летучий оксид
SiO
2
+ Na
2
CO
3
= Na
2
SiO
3
+ CO
2
↑
амфотерные оксиды — солеобразующие оксиды, проявляющие в зависимости от условий либо
осно́вные, либо кислотные свойства (то есть проявляющие амфотерность). Образуются
переходными металлами (например, оксид цинка ZnO, оксид алюминия Al
2
О
3
): оксиды металлов со
степенью окисления III—IV и исключения II (ZnO, BeO, SnO, PbO);
Химические свойства: Амфотерные оксиды
При взаимодействии с сильной кислотой или кислотным оксидом проявляют основные свойства:
ZnO + 2HCl = ZnCl
2
+ H
2
O
При взаимодействии с сильным основанием или основным оксидом проявляют кислотные
свойства:
ZnO + 2KOH + H
2
O = K
2
[Zn(OH)
4
)](в водном растворе)
ZnO + CaO = CaZnO
2
(при сплавлении)
НЕСОЛЕОБРАЗУЮЩИЕ ОКСИДЫ: оксид углерода(II) СО, оксид азота(I) N
2
O, оксид азота(II) NO,
оксид кремния(II) SiO.
ПОЛУЧЕНИЕ ОКСИДОВ
1. Взаимодействие простых веществ (за исключением инертных газов, золота и платины) с
кислородом:
2Cu + O
2
= 2CuO
1

2. При горении в кислороде щелочных металлов (кроме лития), а также стронция и бария
образуются пероксиды и надпероксиды:
2Na + O
2
= Na
2
O
2
2. Обжиг или горение бинарных соединений в кислороде:
4FeS
2
+ 11O
2
= 2Fe
2
O
3
+ 8SO
2
↑
3. Термическое разложение солей
CaCO
3
= CaO + CO
2
↑
4. Термическое разложение оснований или кислот:
2Al(OH)
3
= Al
2
O
3
+ 3H
2
O↑
4HNO
3
= 4NO
2
↑ + O
2
↑ + 2H
2
O
5. Окисление низших оксидов в высшие и восстановление высших в низшие
4FeO + O
2
= 2Fe
2
O
3
Fe
2
O
3
+ CO = 2FeO + CO
2
↑
6. Взаимодействие некоторых металлов с водой при высокой температуре:
Zn + H
2
O = ZnO + H
2
↑
7. Взаимодействие солей с кислотными оксидами при нагревании с выделением летучего
оксида:
Ca
3
(PO
4
)
2
+ 3SiO
2
= 3CaSiO
3
+ P
2
O
5
↑
8. Взаимодействие металлов с кислотами-оксилителями:
Zn + 4HNO
3(конц.)
= Zn(NO
3
)
2
+ 2NO
2
↑ + 2H
2
O
9. При действии водоотнимающих веществ на кислоты и соли:
2KClO
4
+ H
2
SO
4(конц)
= K
2
SO
4
+ Cl
2
O
7
+ H
2
O
10. Взаимодействие солей слабых неустойчивых кислот с более сильными кислотами:
NaHCO
3
+ HCl = NaCl + H
2
O + CO
2
↑
Гидроксиды (гидроокиси) — соединения оксидов химических элементов с водой. Гидроксиды
могут образовать только оксиды металлов.
В зависимости от того, является ли соответствующий оксид основным, кислотным или
амфотерным, соответственно различают:
основные гидроксиды (основания ) — гидроксиды, образованные элементами с металлическими
свойствами (например, гидроксид кальция Ca(ОН)
2
, гидроксид калия KOH, гидроксид натрия NaOH и
др.)
СПОСОБЫ ПОЛУЧЕНИЯ ОСНОВАНИЙ:
1. Получение щелочи при реакции сильноосновного оксида с водой
Так как только сильноосновные оксиды способны реагировать с водой, этот способ можно
использовать исключительно для получения сильных оснований или щелочей.
CaO(т) + H
2
O(ж) → Ca(OH)
2
(p)
Слабоосновные и амфотерные оксиды с водой не реагируют, и поэтому соответствующие им
гидроксиды таким способом получить нельзя.
2. Косвенное получение основания (гидроксида) при реакции соли со щелочью
Гидроксиды малоактивных металлов получают при добавлении щелочи к растворам
соответствующих солей. Так как растворимость слабоосновных гидроксидов в воде очень мала,
гидроксид выпадает из раствора в виде студнеобразной массы.
CuSO
4
(p) + 2NaOH(p) → Cu(OH)
2
(т)↓ + Na
2
SO
4
(p)
3. Получение щелочи при реакции замещения типичного металла с водой.
Ca+2H
2
O=Ca(OH)
2
+H
2
КЛАССИФИКАЦИЯ ОСНОВАНИЙ:
- Растворимые в воде основания (щёлочи)
LiOH, NaOH, KOH, Ca(OH)
2
, Ba(OH)
2
, Sr(OH)
2
, Ra(OH)
2
, CsOH, RbOH, FrOH
- Практически нерастворимые в воде гидроксиды
Mg(OH)
2
, Zn(OH)
2
, Cu(OH)
2
, Al(OH)
3
, Fe(OH)
3
, Be(OH)
2
- Другие основания
NH
3
× H
2
O
Деление на растворимые и нерастворимые основания практически полностью совпадает с
делением на сильные и слабые основания, или гидроксиды типичных и не типичных металлов
Химические свойства:
1. Действие на индикаторы: лакмус - синий, метилоранж - жёлтый, фенолфталеин -
малиновый,
2. Основание + кислота = Соли + вода. П р и м е ч а н и е : р е а к ц и я н е и д ё т , е с л и и
к и с л о т а , и щ ё л о ч ь с л а б ы е .
2

NaOH + HCl = NaCl + H
2
O
3. Щёлочь + кислотный или амфотерный оксид = соли + вода
2NaOH + SiO
2
= Na
2
SiO
3
+ H
2
O
4. Щёлочь + соли = (новое)основание + (новая) соль. П р и м е ч а н и е : и с х о д н ы е
в е щ е с т в а д о л ж н ы б ы т ь в р а с т в о р е , а х о т я б ы о д и н и з п р о д у к т о в р е а к ц и и
в ы п а с т ь в о с а д о к и л и м а л о р а с т в о р я т ь с я .
Ba(OH)
2
+ Na
2
SO
4
= BaSO
4
+ 2NaOH
5.Слабые основания при нагреве разлагаются:
Cu(OH)
2
+Q=CuO + H
2
O
6.При нормальных условиях невозможно получить гидроксиды серебра и ртути, вместо них в
реакции появляются вода и соответствующий оксид:
AgNO
3
+ 2NaOH(p) → NaNO
3
+Ag
2
O+H
2
O
кислотные гидроксиды (кислородосодержащие кислоты) — гидроксиды, проявляющие
кислотные свойства (например, азотная кислота HNO
3
, серная кислота H
2
SO
4
, сернистая кислота
H
2
SO
3
и др.)
амфотерные гидроксиды, проявляющие в зависимости от условий либо основные, либо
кислотные свойства (например, гидроксид алюминия Al(ОН)
3
, гидроксид цинка Zn(ОН)
2
).
Термин «гидроксиды» часто применяют только по отношению к основным и амфотерным
гидроксидам.
Кислота – это сложное вещество, в молекуле которого имеется один или несколько атомов
водорода и кислотный остаток.
КЛАССФИКАЦИЯ КИСЛОТ:
1. По содержанию кислорода
- бескислородные (HCl, H
2
S);
- кислородосодержащие (HNO
3
).
2. По основности— количество кислых атомов водорода
- Одноосновные (HPO
3
);
- Двухосновные (H
2
SO
4
);
- Трёхосновные (H
3
PO
4
).
- Четырёхосновные (H
4
СO
4
).
3. По силе
- Сильные— диссоциируют практически полностью, константы диссоциации больше 1·10
−3
(HI, HBr, HCl, H
2
SO
4
,
HNO
3
);
- Слабые— константа диссоциации меньше 1·10
−3
(HF, H
3
PO
4
, H
2
SO
3
, H
2
S, H
2
CO
3
, H
2
SiO
3
,).
ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ:
1. Взаимодействие с оксидами металлов с образованием соли и воды:
CaO +2HCl →CaCl
2
+H
2
O
2. Взаимодействие с амфотерными оксидами с образованием соли и воды:
ZnO + 2HNO
3
→Zn(NO
3
)
2
+H
2
O
3. Взаимодействие со щелочами с образованием соли и воды (реакция нейтрализации):
NaOH +HCl →NaCl
+ H
2
O
4. Взаимодействие с нерастворимыми основаниями с образованием соли и воды, если
полученная соль растворима:
Cu(OH)
2
↓ + 2H
2
SO
4
→CuSO
4
+ 2H
2
O
5. Взаимодействие с солями, если выпадает осадок или выделяется газ:
BaCl
2
+H
2
SO
4
→BaSO
4
↓ + 2HCl↑
6. Сильные кислоты вытесняют более слабые из их солей:
K
3
PO
4
+ 3HCl → 3KCl + H
3
PO
4
7. Металлы, стоящие в ряду активности до водорода, вытесняют его из раствора кислоты (кроме
азотной кислоты любой концентрации и концентрированной серной кислоты), если образующаяся
соль растворима:
Mg + 2HCl →MgCl
2
+ H
2
↑
С азотной кислотой и концентрированной серной кислотами реакция идёт иначе:
Mg + 2H
2
SO
4
→MgSO
4
+ SO
2
↑ +2H
2
O
СПОСОБЫ ПОЛУЧЕНИЕ КИСЛОТ:
Кислоты можно получить по реакциям соответствующих кислотных оксидов с водой:
CO
2
+ H
2
O → H
2
CO
3
Соли - вещества, состоящие из катионов металла (или катиона аммония NH
4
+
) и анионов
кислотного остатка.
КЛАССИФИКАЦИЯ СОЛЕЙ:
3

- Средние (нормальные) соли— все атомы водорода в молекулах кислоты замещены на атомы
металла Na
2
CO
3
- Кислые соли— атомы водорода в кислоте замещены атомами металла частично. Они
получаются при нейтрализации основания избытком кислоты K
2
HPO
4
- Осно́вные соли— гидроксогруппы основания (OH
-
) частично замещены кислотными остатками
(CuOH)
2
CO
3
- Двойные соли— в их составе присутствует два различных катиона, получаются
кристаллизацией из смешанного раствора солей с разными катионами, но одинаковыми
анионами. KAl(SO
4
)
2
∙ 12H
2
O
- Смешанные соли— в их составе присутствует два различных аниона Ca(OCl)Cl
- Гидратные соли (кристаллогидраты)— в их состав входят молекулы кристаллизационной воды
Na
2
SO
4
∙ 10H
2
O.
- Комплексные соли— в их состав входит комплексный катион или комплексный анион
K
3
[Fe(CN)
6
], [Cu(NH
3
)
4
](OH)
2
.
СПОСОБЫ ПОЛУЧЕНИЯ СОЛИ:
1. Взаимодействие кислот с металлами, основными и амфотерными оксидами / гидроксидами:
H
2
SO
4
+ Mg → MgSO
4
+ H
2
↑
2. Взаимодействие кислотных оксидов c щелочами, основными и амфотерными оксидами /
гидроксидами:
CaO +SiO
2
→ CaSiO
3
3. Взаимодействие солей c кислотами, другими солями (если образуется выходящий из сферы
реакции продукт):
CuCl
2
+ Na
2
S → 2NaCl + CuS↓
4. Взаимодействие простых веществ:
Fe + S → FeS
5. Взаимодействие оснований с неметаллами, например с галогенами:
Ca(OH)
2
+ Cl
2
→ Ca(OCl)Cl + H
2
O
ХИМИЧЕСКИЕ СВОЙСТВА СОЛИ:
1. Соли взаимодействуют с кислотами и основаниями, если в результате реакции получается
продукт, который выходит из сферы реакции (осадок, газ, мало диссоциирующие вещества,
например, вода):
BaCl
2
+ H
2
SO
4
→ BaSO
4
↓ + 2HCl
2. Соли взаимодействуют с металлами, если свободный металл находится левее металла в
составе соли в электрохимическом ряде активности металлов:
Cu + HgCl
2
→ CuCl
2
+ Hg
3. Соли взаимодействуют между собой, если продукт реакции выходит из сферы реакции; в том
числе эти реакции могут проходить с изменением степеней окисления атомов реагентов:
AgNO
3
+ NaCl → AgCl↓ + NaNO
3
4. Некоторые соли разлагаются при нагревании:
NH
4
NO
3
→ N
2
O↑ + 2H
2
O
2. Закон сохранения материи.
Закон сохранения материи (М.В. Ломоносов; А. Лавуазье)
Общая масса веществ, вступивших в химическую реакцию (реагентов), равна общей массе
продуктов реакции (продуктов).
Например, если 4 г водорода сгорают в кислороде с образованием 36 г воды, то следует
заключить, что в этой реакции принимают участие 32 г кислорода:
ггг
OHOH
36
2
32
2
4
2
22
3. Основные типы комплексных соединений (к.с.). Поведение к.с. в водных растворах.
Константа нестойкости.
Классификация комплексных соединений.
По принадлежности к определенному классу соединений различают:
- комплексные кислоты – H[AuCl
4
];
- комплексные основания – [Ag(NH
3
)
2
]OH;
- комплексные соли – K
2
[HgI
4
].
По природе лигандов различают:
- аквакомплекс – [Co(H
2
O)
6
]SO
4
;
4
- аммиакаты – [Ag(NH
3
)
2
]Cl;
- ацидокомплексы – K
4
[Fe(CN)
6
];
- комплексы смешанного типа – [Co(NH
3
)
3
(H
2
O)
3
]
- бикомплексы (катион и анион – комплексы)
- гироксокомплексы – K
3
[Al(OH)
6
].
По знаку заряда комплекса различают:
- катионные – [Al(H
2
O)
6
]Cl
3
- анионные – K[AuCl
4
]
- нейтральные – [Co(NH
3
)
3
Cl
3
]
По внутренней силе различают:
- циклические
- хелактные (клешневидные)
Комплексные соединения катионного и анионного типа чаще всего растворимы в воде; в их
водных растворах устанавливаются химические равновесия, иногда довольно сложные. Комплексы-
неэлектролиты, как правило, малорастворимы в воде; растворившаяся часть комплексов ведет
себя как слабый электролит.
При первичной диссоциации комплекса, имеющего ионы внешней сферы, соединение ведет
себя как сильный электролит - полностью отделяет ионы внешней сферы. Затем происходит
вторичная диссоциация комплекса уже по типу слабого электролита - отделяются лиганды
внутренней сферы.
Так, в случае аммиачного комплекса серебра наблюдается последовательное замещение
молекул аммиака молекулами воды:
[Ag(NH
3
)
2
] + H
2
O
[Ag(H
2
O)
2
] +NH
3
Мерой прочности комплексного иона служит константа нестойкости К
н
, соответствующая
процессу полной диссоциации комплексного иона на комплексообразователь и лиганды:
[Fe(CN)
6
]
3-
=Fe
3+
+6CN
-
3
6
63
])([
]][[
CNFe
CNFe
K
н
Чем меньше значение К
н
, тем более устойчив комплекс.
4. Номенклатура комплексных соединений. Координационное число.
Номенклатура комплексных соединений утверждена комиссией ИЮПАК с учетом особенностей,
принятых в русском языке: первым называют анион, затем катион;
Название числовых приставок:
1 – моно- 5 – пента- 9 – нона-
2 – ди- 6 – гекса- 10 – дека-
3 – три- 7 – гепта- 11 – ундека-
4 – тетра- 8 – окта- 12 – додека-
Название а н и о н н ы х лигандов получают соединительную о, например:
F
-
- фторо OH
-
- гидроксо NCS
-
- тиоцианато
Cl
-
- хлоро CN
-
- циано NO
2
-
- нитро
O
-
- оксо H
-
- гидродо SO
3
2
-
- сульфито
Название н е й т р а л ь н ы х лигандов:
H
2
O – аква
NH
3
– аммин
CO – карбонил
NO – нитрозил
Названия комплексов строятся по схеме n+L+M (т.е. справа налево по формуле).
Нейтральные комплексы:
[Co(NH
3
)
3
Cl
3
] – трихлоротриамминкобальт
Катионные комплексы:
[Al(H
2
O)
6
]Cl
3
– хлорид гексаакваалюминия(III)
Анионные комплексы:
K[AuCl
4
] – тетрахлороаурат(III) калия
Число химических связей, которые комплексообразователь образует с лигандами, называют
координационным числом. если комплексообразователь связан с монодентантными лигандами,
то координационное число равно числу лигандов. Значение координационного числа
комплексообразователя зависит от его природы, степени окисления, природы лигандов и условий
протекания реакции комплексообразования. Между значением координационного числа и
степенью окисления комплексообразования существует определенная связь. Часто
5

координационное число равно удвоенному значению степени окисления комплексообразователя.
Нейтральные лиганды могут присоединятся к комплексообразователю в большем количестве.
5. Амфотерные гидроксиды
Амфоте́рные гидрокси́ды — химические вещества, которые могут проявлять как основные,
так и кислотные свойства (в зависимости от условий реакции).
Амфотерные гидроксиды в кислой среде ведут себя как основания, а в щелочной — как
кислоты. К амфотерным гидроксидам относятся основания, образованные переходными
металлами: Al(3+), Be(2+), Fe(3+), Cr(3+), Zn(2+), Sn(2+), Pb(2+) и другие…
Практически все они нерастворимы в воде, являются слабыми электролитами.
При нагревании соединения разлагаются.
6. Комплексные соединения. Комплексообразователь, лиганды.
Комплексные соединения – соединения, в узлах кристаллической решетки которых
содержаться ионы (комплексы), способные к самостоятельному существованию в растворе или
расплаве.
Комплексные соединения представляют собой сложные вещества, молекулы которых содержат
центральный атом или ион (комплексообразователь), связанный с несколькими способными к
самостоятельному существованию молекулами или ионами, называемыми лигандами. Различают
внутреннюю и внешнюю сферы комплексного соединения. Более прочно связанные частицы
внутренней сферы называют комплексным ионом или комплексом. При написании
координационной формулы эту часть комплексного соединения заключают в квадратные скобки.
Комплекс выступает как самостоятельная единица в химических реакциях, процессах растворения,
структуре кристалла. Частицы внешней сферы, связанные в соединении менее прочно, при
диссоциации в растворе отделяются.
В качестве комплексообразователя может выступать любой элемент, но наиболее характерна
эта роль для d- и f-металлов. Лигандами могут быть простые и сложные ионы, а также
электронейтральные молекулы, как вода, аммиак и др.
7. Гидролиз солей, образованных слабым основанием и сильным кислотой. Степень и
константа гидролиза.
В случае соли, образованной слабым основанием и сильной кислотой, гидролизу
подвергается катион соли и реакция сопровождается образованием ионов H
+
, например:
HClOHNHOHClNH
424
или
HOHNHOHNH
424
Накопление ионов H
+
к уменьшению концентрации ионов OH
-
. Таким образом, р а с т в о р ы
с о л е й о б р а зо в а н н ы е с л а б ы м о с н о в а н и е м и с и л ь н о й к и с л о т о й , и м е ю т к и с л у ю р еа к ц и ю
(pH<7).
Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу,
к общей концентрации её ионов в растворе.
C
C
г
г
,
где С
г
– концентрация гидролизной соли, С – концентрация растворенной соли. Степень
гидролиза определяется тремя факторами: ее значение тем больше, чем ниже концентрация
раствора, больше константа гидролиза и выше температура (гидролиз — эндотермический
процесс).
Величина К
г
называется константой гидролиза соли. ее значение характеризует способность
данной соли подвергаться гидролизу; чем больше К
г
, тем в большей степени (при одинаковых
температуре и концентрации соли) протекает гидролиз.
Для случая соли, образованных слабой кислотой и сильным основанием, константа гидролиза
связана с константой диссоциации кислоты К
кисл
зависимостью:
кисл
OH
г
K
K
K
2
Ч е м с л а б е е к и с ло т а , т ем в бо л ь ш ей с т е пе н и п о д в е р г а ю т с я ги д р о л и з у е е с о л и .
Для солей, образованных слабым основанием и сильной кислотой, аналогичное соотношения
связывает константу гидролиза с константой основания К
осн
:
6

осн
OH
г
K
K
K
2
Поэтому, ч е м с л а б ее о с но в а н и е , т е м в б о ль ш е й с т е п е н и п о д в е р г а е т с я г и др о л и з у
о б р а з о в а н н ые и м с о л и .
Для солей, образованных слабой кислотой и слабым основание, константа гидролиза связана с
константами диссоциации кислоты и основания следующими соотношением:
оснкисл
OH
г
KK
K
K
2
8. Растворение твердых веществ. Из каких слагаемых состоит теплота растворения
твердого вещества в жидкости?
Большинство веществ, находящихся в кристаллическом состоянии, растворяются в жидкостях с
поглощением теплоты. Однако при растворении в воде гидроксида натрия, карбоната калия и
многих других веществ происходит заметное повышение температуры.
К о л и че с т в о т е п л о т ы , п о г л о щ а ю щ е й с я ( и л и в ы д е л я ю щ е й с я ) п р и р а с т в о р е н и и
о д н о г о м о л я в е щ е с т в а , н а з ы в а е т с я т е п л о то й р а с т в о р е н и я э т о г о ве щ е с т в а .
Теплота растворения имеет отрицательное значение, если при растворении теплота
поглощается, и положительное – при выделении теплоты.
Процесс растворения сопровождается значительным возрастанием энтропии системы, так как в
результате равномерного распределения частиц одного вещества в другом резко увеличивается
число микросостояний системы.
При растворении кристаллов происходит их разрушение, что требует затраты энергии. Поэтому
растворение должно было бы сопровождаться поглощением теплоты. Если же наблюдается
обратный эффект, то это показывает, что одновременно с растворением происходит какое-то
взаимодействие между растворителем и растворенным веществом, при котором выделяется в виде
теплоты больше энергии, чем ее расходуется на разрушение кристаллической решетки.
Энтольпия (теплота) растворения:
TmcH
pS
,
где m – масса раствора; c
p
– удельная изобарная теплоемкость раствора; ∆Т – изменение
температуры.
9. Типы окислительно-восстановительных реакций.
Р е а к ц и и , в р е з у л ь т а т е к о т о ры х и зме н я ю т с я с т е п е н и о к и с л е н и я э л е м е н то в ,
н а з ы в а ю т с я о к и с л и т е л ь н о - в о с с т а н о в и т е л ь н ы м и .
Окисление – процесс отдачи электронов, сопровождающийся повышением степени
окисленности элемента.
Восстановление – процесс присоединения электронов, сопровождающийся понижением
степени окисленности элемента.
Вещество, в состав которого входит окисляющийся элемент, называется восстановителем, а
вещество, содержащее восстанавливающийся элемент, окислителем.
Межмолекулярные - реакции, в которых окисляющиеся и восстанавливающиеся атомы
находятся в молекулах разных веществ, например:
Н
2
S + Cl
2
S + 2HCl
Внутримолекулярные - реакции, в которых окисляющиеся и восстанавливающиеся атомы
находятся в молекулах одного и того же вещества, например:
NH
4
NO
3
N
2
O + 2 H
2
O
Диспропорционирование (самоокисление-самовосстановление) - реакции, в которых атомы
с промежуточной степенью окисления превращаются в эквимолярную смесь атомов с более
высокой и более низкой степенями окисления:
Cl
2
+ H
2
O
HClO + HCl
Реакции контрпропорционирования (коммутации) — это процессы взаимодействия
окислителя и восстановителя, в состав которых входит один и тот же элемент с разными
степенями окисления. В результате продуктом окисления и восстановления является
вещество с промежуточной степенью окисления атомов данного элемента:
HBr
+5
O
3(конц)
+5HBr
(конц)
=3Br
2
0
+3H
2
O
10. Закон постоянства состава. Дальтониды, бертоллиды.
Закон постоянства состава веществ (Ж.Л. Пруст)
7

Состав молекулярного соединения остается постоянным независимо от способа его получения.
В отсутствии молекулярной структуры его состав зависит от условий получения и предыдущей
обработки.
Дальтониды —вещества постоянного качественного и количественного состава, который не
зависит от способа получения. К дальтонидам относятся низкокислящие жидкости, твердые
вещества с молекулярной структурой.
Бертоллиды — соединения переменного состава, не подчиняющиеся законам постоянных и
кратных отношений. Это нестехиометрические бинарные соединения переменного состава,
зависящего от способа получения. Многочисленные случаи образования бертоллидов открыты в
металлических системах, а также среди оксидов, сульфидов, карбидов, гидридов и др.
11. Кристаллизация разбавленных и концентрированных растворов. Кристаллогидраты.
Раствор, в отличие от чистой жидкости не отвердевает целиком при одной температуре.
Кристаллы начинают выделяться при какой-то одной температуре. По мере понижения
температуры количество их растет, пока весь раствор не отвердеет. Температурой начала
кристаллизации называют температуру, при которой при охлаждении раствора начинается
образование кристаллов. Не рассматривая здесь систем, в которых происходит образование
твердых растворов, можно сказать, что температурой начала кристаллизации называется
температура, при которой кристаллы растворителя находятся в равновесии с раствором данного
вещества. Опыт показывает, что разбавленный раствор замерзает при температуре более низкой,
чем чистый растворитель. Такое изменение температуры можно рассматривать как общее правило.
Для характеристики температуры замерзания раствора введена величина “понижение
температуры замерзания” DT
3
.
Кристаллогидраты — кристаллы, включающие молекулы воды. Многие соли, а также кислоты
и основания выпадают из водных растворов в виде кристаллогидратов Типичными
кристаллогидратами являются многие природные минералы, например гипс CaSO
4
·2H
2
O,
карналлит MgCl
2
·KCl·6H
2
O. Кристаллизационная вода обычно может быть удалена нагреванием,
при этом разложение кристаллогидрата часто идёт ступенчато; так, медный купорос CuSO
4
·5H
2
O
(синий) выше 105 °С переходит в тригидрат CuSO
4
·3H
2
O (голубой), при 150 °С в моногидрат
CuSO
4
·H
2
O (белый); полное обезвоживание происходит выше 250°С. Однако некоторые соединения
(например, BeC
2
O
4
·H
2
O) устойчивы только в форме кристаллогидрата и не могут быть обезвожены
без разложения.
12. Ионообменные реакции. Произведение растворимости.
Ионный обмен — обмен ионов между двумя электролитами. Ионный обмен может происходить
как в гомогенной среде (истинный раствор нескольких электролитов), так и в гетерогенной, в
которой один из электролитов является твёрдым (при контакте раствора электролита с осадком,
ионитом и др.).
В н а с ы щ е н но м р а с т в о р е э л е к т р о л и та п р о и зв е д е н ие к о н ц е н т р а ц и и е г о и он о в е с т ь
в е л и чи н а по с т о я н н а я п р и д а н н о й т е м п е р а т у р е . Эта величина количественно характеризует
способность электролита растворяться; ее называют произведением растворимости электролита
и обозначают буквами ПР.
]][[
AKПР
KA
13. Закон кратных отношений.
Закон кратных отношений: «Е с л и д в а э л е м е н т а о б р а з у ю т д р у г с д р у г о м н е с к о л ь к о
х и м и че с к и х с о е д и н е н и й , т о м а с с ы о д н о г о и з э л е м е н т о в , п р и х о д я щ и е с я в э т и х
с о е д и н е н и я х н а о д н у и т у ж е м а с с у д р у г о г о , о т н о с я т с я м е ж д у с о б о й к а к н е б о л ь ш и е
ц е л ы е ч и с л а ».
14. Электрохимическая диссоциация воды. Ионное произведение воды. Водородный
показатель.
Чистая вода очень плохо проводит электрический ток, но все же обладает измеримой
электрической проводимостью, которая объясняется небольшой диссоциацией воды на ионы
водорода и гидроксид-иона:
OHHOH
2
По величине электрической проводимости чистой воды можно вычислить концентрацию ионов
водорода и гидроксид-ионов в воде. при 25
о
С она равна 10
−7
моль/л.
8

Д л я в о д ы и р а з б а в л е н н ы х в о д н ы х р а с т в о р о в п р и н е и зме н н о й т е м п е р а т у р е
п р о и зв е д е н ие к о н ц е н т р а ц и и и он о в во д о р о да и гид р о к с и д - и о н о в е с ть в е л и ч и н а
п о с т о я н н а я и н а зы в а е т с я и о н н ы м п р о и з в е д е н и е м в о д ы .
Растворы, в которых концентрации ионов водорода и гидроксид-ионов одинаковы, называются
нейтральными растворами. В кислых растворах больше концентрация ионов водорода, в щелочных
– концентрация гидроксид-ионов.
чтобы не писать числа с показателем степени, кислотность раствора часто выражают через
отрицательный логарифм концентрации ионов водорода, называя эту величину водородным
показателем и обозначая ее pH:
]lg[
HpH
Практически реакцию среды удобно определит при помощи индикаторов – веществ, меняющих
свой цвет в зависимости от относительной концентрации ионов H
+
и OH
−
.
Название
Окраска индикатора в среде
Кислая
[H
+
]>[OH
−
]
pH<7
Нейтральная
[H
+
]=[OH
−
]
pH=7
Щелочная
[H
+
]<[OH
−
]
pH>7
Лакмус красный фиолетовый синий
Фенолфталеин бесцветный бесцветный малиновый
Метилоранж розовый оранжевый желтый
15. Отношение металлов к соляной и серной кислотам (разбавленной и
концентрированной).
Серная кислота проявляет окислительные свойства в концентрированном растворе за счет серы
в степени окисления +6. Состав продуктов восстановления определяется главным образом
активностью восстановителя и концентрацией кислоты:
Так, взаимодействие концентрированной H
2
SO
4
с малоактивными металлами, некоторыми
неметаллами и их соединениями приводит к образованию оксида серы (IV):
OHSOCuSOSOHCu
конц 224)(42
22
Активные металлы восстанавливают концентрированную серную кислоту до серы или
сероводорода:
OHSZnSOSOHZn
конц 24)(42
4343
16. Факторы, влияющие на окислительно-восстановительные процессы. Расстановка
коэффициентов в окислительно-восстановительных реакциях.
Природа, концентрация, температура, катализаторы
Метод электронного баланса, основанный на учете изменения степеней окисления и принципе
электронейтральности молекулы, является универсальным. Его обычно используют для
составления уравнений окислительно-восстановительных реакций, протекающих между газами,
твердыми веществами и в расплавах.
Последовательность операций, согласно этому методу, такая:
1) Записывают формулы реагентов и продуктов реакции в молекулярном виде:
HClSFeClSHFeCl
223
2) Определяют степени окисления атомов, меняющих ее в процессе реакции:
HClSClFeSHClFe
0
2
22
23
3
3) По изменению степеней окисления устанавливают число электронов, отдаваемых
восстановителем, и число электронов, принимаемых окислителем, и составляют электронный
баланс с учетом принципа равенства числа отдаваемых и принимаемых электронов:
9
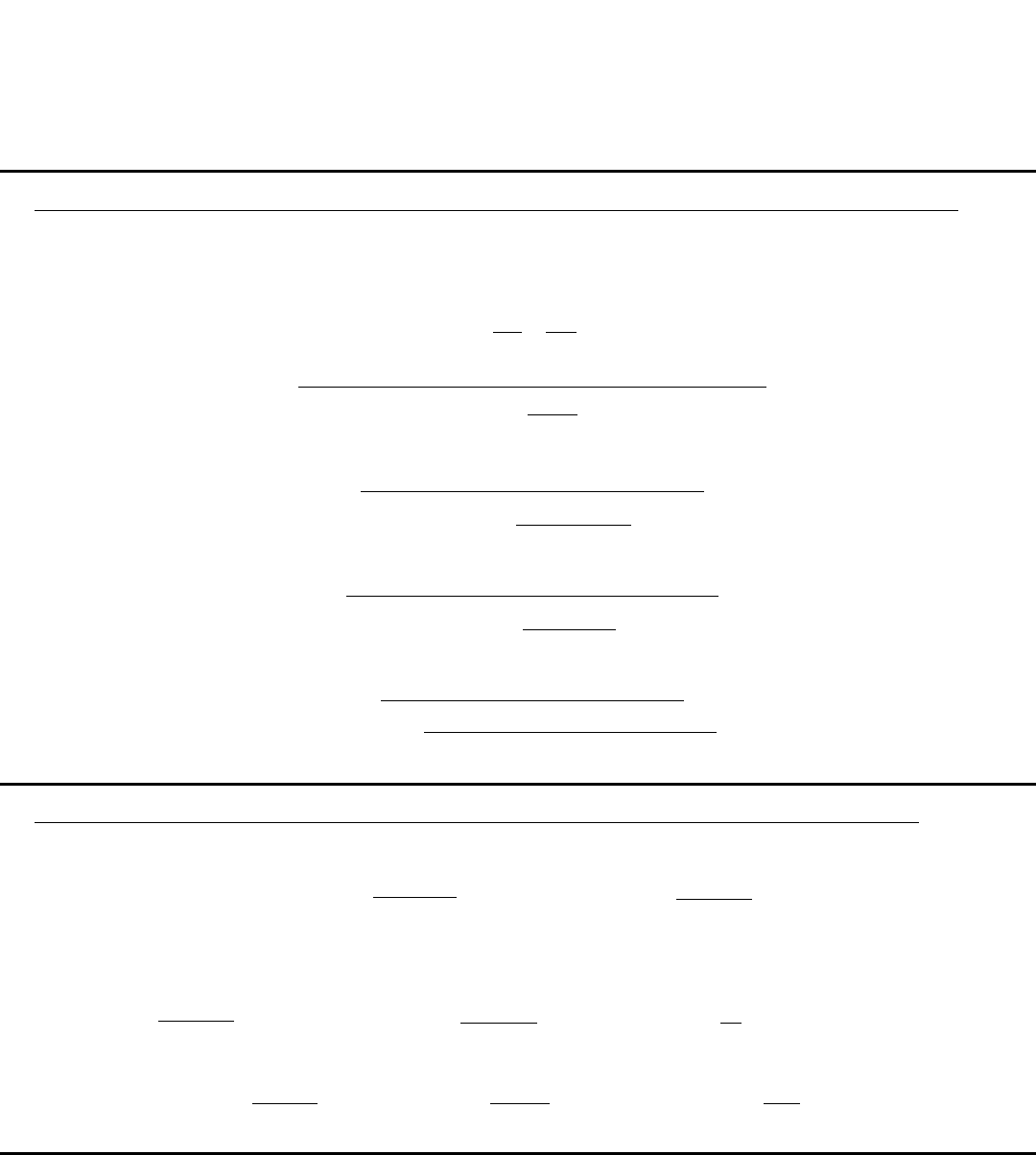
4) Множители электронного баланса записывают в уравнение окислительно-восстановительной
реакции как основные стехиометрические коэффициенты:
HClSFeClSHFeCl
223
22
5) подбирают стехиометрические коэффициенты остальных участников реакции:
HClSFeClSHFeCl
223
22
При составлении уравнений следует учитывать, что окислитель (или восстановитель) может
расходоваться не только в основной окислительно-восстановительной реакции, но и при
связывании образующихся продуктов реакции, т.е. выступать в роли среды и солеобразователя.
17. Закон эквивалентов. Определение эквивалентов простых и сложных веществ.
Закон эквивалентов: «Д л я м о лек у л я р н ы х с о е д и н е н и й м а с с о в ы е к о л и ч е с т в а
с о с т а в л я ю щ и х э л е м е н т о в п р о по р ц и о н а л ь н ы и х х и м и ч е с ки м э кв и в а ле н т а м ; п р и
о т с у тс т в и и м о л е ку л я р н о й с т р у к т у р ы м а с с о в ы е ко л и ч е с т в а с о с т а в л я ющ и х
э л е м е н т о в м о г у т о т к л о н я т ь с я о т з н а ч е н и й и х х и м и ч е с к и х э к в и в а л е н т о в ».
2
2
1
1
Э
m
Э
m
ЭКВИВАЛЕНТНАЯ МАССА ПРОСТОГО ВЕЩЕСТВА:
n
rA
Э
)(
,
где n – заряд элемента.
ЭКВИВАЛЕНТНАЯ МАССА КИСЛОТЫ:
Hатчисл
M
Э
кисл
кисл
..
.
.
В химической реакции делим на число замещенных атомов водорода.
ЭКВИВАЛЕНТНАЯ МАССА ОСНОВАНИЯ:
OHчисл
M
Э
осн
осн
.
.
.
В химической реакции делим на число гидроксогрупп.
ЭКВИВАЛЕНТНАЯ МАССА СОЛИ:
.... катионзарядкатиончисл
M
Э
соли
соли
18. Способы выражения концентрации раствора: молярная, нормальная, титр.
М о л я р н а я к о н ц е н т р а ц и я – отношение количества растворенного вещества к объему
раствора; показывает количество моль вещества, приходящегося на 1 л раствора.
лмоль
лVM
m
C
M
/
)(
M
C
M
10
Н о р м а л ь н о с т ь ( Э к в и в а л е н т н а я к о н ц е н т р а ц и я ) – отношение количества
эквивалентов растворенного вещества к объему раствора; показывает количество эквивалентов
вещества, приходящихся на 1 л раствора.
лмоль
лVЭ
m
C
H
/
)(
Э
p
C
H
10
Э
m
p
- кол-во эквивалентов
Т и т р – показывает граммовое содержание вещества 1 мл раствора.
млг
MC
T
m
/
1000
млг
ЭC
T
Н
/
1000
млгT /
100
19. Квантово-механическая теория строения атома. Уравнение Луи де Бройля. Принцип
неопределенности Гейзенберга.
Электроны могут находиться в атоме только в дискретных состояниях с определенной
энергией; при переходе электрона из одного состояния в другое испускается (или поглощается)
фотон. Согласно квантовой механике, не существует определенных круговых орбит электронов,
как в теории Бора. В силу волновой природы электрон «размазан» в пространстве, подобно
«облаку» отрицательного заряда.
Электронное облако можно интерпретировать как с корпускулярной, так и с волновой точки
зрения. Следовательно, размытое в пространстве облако является результатом волновой природы
электронов. Электронное облако можно также интерпретировать как распределение вероятностей
для данной частицы. Мы не можем предсказать траектории, по которой будет двигаться электрон.
10
