Туяхов И.А. Практическая метрология
Подождите немного. Документ загружается.

ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
240
водности раствора и усиленная электронным блоком, дает информа-
цию на показывающем и регистрирующем устройстве о концентрации
растворенного вещества в воде. В резонансных схемах для измерения
величины индукции L
x
безэлектродного индуктивного преобразовате-
ля используется резонансный контур, частота собственных колебаний
которого зависит от индуктивности L
x
первичного безэлектродного
преобразователя.
Разновидностью безэлектродного индуктивного преобразователя
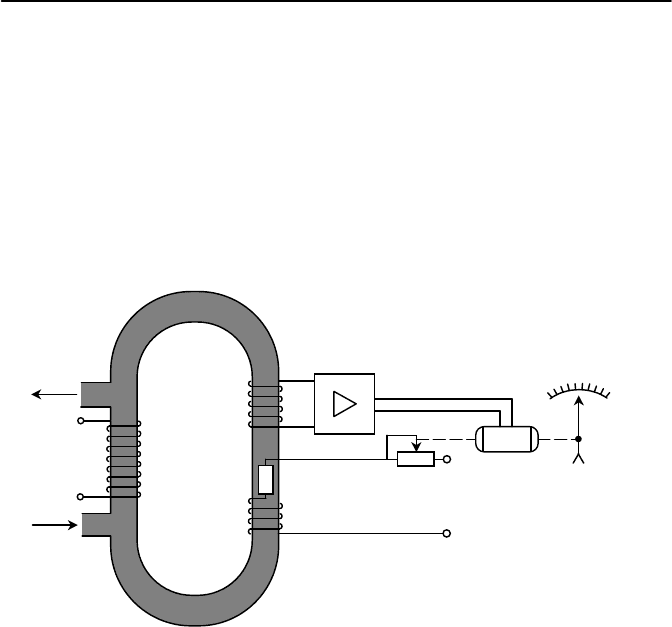
является трансформаторный преобразователь (рисунок 8.4), в котором
анализируемый раствор протекает по кольцевой пластмассовой трубе,
образующей замкнутый контур.
Трансформаторный преобразователь состоит из первичной об-
мотки, на которую подается переменное напряжение U
вх
частотой 50
Гц, вторичной измерительной обмотки, с которой снимается напряже-
ние U
вых
и компенсационной обмотки, на которую подается компенса-
ционное напряжение U
к
частотой 50 Гц. Перечисленные обмотки объ-
единены кольцевым жидким контуром, выполняющим роль сердечни-
ка трансформатора.
При изменении концентрации солей (щелочей, кислот и др.) в
анализируемой жидкости изменяется переменный магнитный поток в
жидком контуре, и выходное напряжение U
вых
будет однозначно опре-
делять содержание солей в жидкости. Для уменьшения влияния коле-
баний напряжения и частоты питающей сети предусмотрен компенса-
ционный контур, который создает переменный магнитный поток в
∼
U
вх
%NaCl
∼
U
к
R
к
R
t
U
вых
Рисунок 8.4 – Безэлектродный трансформаторный кондуктометр

ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
241
жидком контуре, направленный навстречу основному потоку, созда-
ваемому первичной обмоткой. Возрастание компенсационного маг-
нитного потока, управляемого выходным напряжением U
вых
через
усилитель, исполнительный механизм и компенсационное сопротив-
ление , происходит до полной компенсации основного магнитного по-
тока. Величина компенсационного магнитного потока, таким образом,
будет определяться положением движка реохорда R
k
, которое зависит
от значения U
вых
. Стрелка измерительного прибора, кинематически
связанная с валом исполнительного механизма, укажет на концентра-
цию растворенных в воде веществ.
Для автоматической коррекции влияния температуры анализи-
руемой жидкости на показание измерительного прибора кондуктомет-
ра используется полупроводниковый компенсационный терморези-
стор R
t
. При увеличении температуры анализируемой жидкости уве-
личивается степень диссоциации молекул растворенных веществ и
увеличивается магнитный поток. Одновременно уменьшается сопро-
тивление терморезистора и возрастает ток в компенсационной цепи,
увеличивая компенсационный магнитный поток.
Безэлектродные трансформаторные кондуктометры рассчитаны
на диапазон измерения удельной электропроводности 0,01 – 1,0 См/см
при допускаемой основной погрешности 2,5 %.
8.4 Потенциометрический метод анализа воды
Потенциометрический метод анализа качества воды и различных
растворов основывается на законе Нерста. В отличие от кондуктомет-
ров, в которых определяется общая концентрация солей (щелочей ки-
слот и др.), потенциометрические анализаторы определяют концен-
трацию конкретного иона (конкретного растворенного в воде вещест-
ва), а также величину pH раствора. Сущность данного явления состоит
в том, что при погружении любого металлического стержня (электро-
да) в раствор, происходит переход ионов этого металла в раствор из-за
значительного (в 81 раз) ослабления связей между атомами. Переход
ионов будет происходить до тех пор, пока количество ионов, пере-
шедших в раствор, не будет равно количеству ионов, возвратившихся
из раствора на поверхность металла. В результате этого явления на
поверхности металла возникает электрический потенциал, зависящий
от активной концентрации ионов этого металла в растворе. Измерение
поверхностного потенциала электрода позволяет судить о концентра-
ции соответствующих ионов в растворе.
ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
242
Величина потенциала на поверхности электрода в зависимости от
концентрации ионов определяется по уравнению Нерста:
Е=E
0
+RT
F
n
aln
⋅
, (8.2)
где Е
0
– нормальный потенциал;
R – газовая постоянная, (8,314 кДж/(кмоль⋅К));
Т – абсолютная температура;
n – заряд ионов;
F – число Фарадея (9,65⋅10
4
моль
Кл
).
Для измерения поверхностного потенциала Е необходимо замк-
нуть электрическую цепь, вводя в раствор второй электрод, называе-
мый электродом сравнения. Потенциал этого электрода должен оста-
ваться постоянным в процессе измерения. В качестве электрода срав-
нения используется пластина из платины, погруженная в раствор с
активной концентрацией ионов водорода, равной единице при нор-
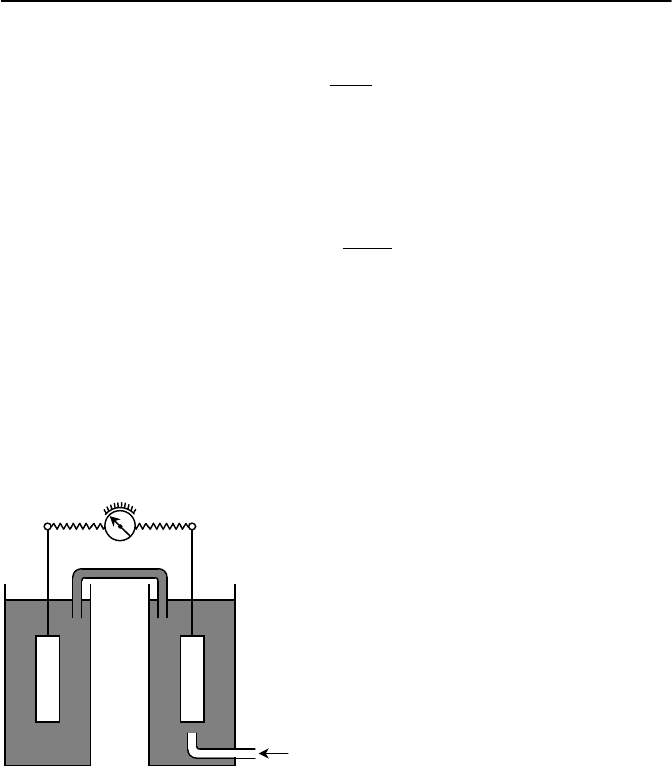
мальном давлении и температуре. На рисунке 8.5 представлена схема
измерения концентрации конкретного иона в растворе с использова-
нием ячейки сравнения. В измери-
тельной ячейке 1 с анализируемым
раствором расположен специальный
(селективный) электрод 3, который
предназначен для определения кон-
центрации определенного компонен-
та. В ячейке сравнения 2 платиновый
электрод помещен в раствор, через
который пропускается водород под
давлением. Две ячейки электрически
связаны между собой перемычкой с
жидким электролитом 5.
Разность потенциалов между
двумя электродами ∆Е=Е – Е
0
соглас-
но закона Нернста однозначно опре-
деляется концентрацией анализируе-
мого компонента, растворенного в
воде. Область применения потенцио-
метрических методов измерения кон-
центрации определенных ионов в
многокомпонентных растворах значи-
ЕЕ
о
6
5
5
1
2
4
Н
2
1 – измерительная ячейка;
2 – ячейка сравнения; 3 – се
-
лективный электрод; 4 – пла
-
тиновый электрод; 5 – пере
-
мычка; 6 – измерительный
прибор
Рисунок 8.5 – Схема потен
-
циометрического анализатора
раствора

ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
243
тельно расширилась благодаря созданию новых ионоселективных
электродов, обладающих выборным характером действия по отноше-
нию к таким катионам и анионам как Na
+
, K
+
, Ca
2+
, Mg
2+
, Pb
2+
,
Cl
-
, Br
-
, I
-
и др.
Созданные лабораторные потенциометрические преобразователи,
называемые ионометрами, являются универсальными приборами, ко-
торые снабжаются комплектом ионоселективных электродов, позво-
ляющими производить измерение концентрации перечисленных выше
ионов.
Наиболее широко потенциометрические приборы применяются
для измерения активной концентрации ионов водорода в растворах,
т.е. для определения рН растворов. При растворении в воде кислот
повышается концентрация ионов водорода и величина рН снижается,
а при растворении щелочи концентрации ионов водорода снижается и
рН растет. Чистая вода, как нейтральное вещество, имеет значение
рН=7. Таким образом, отклонение числа рН в водных растворах от 7 в
ту или другую сторону характеризует меру их кислотных или щелоч-
ных свойств. При эксплуатации паровых котлов тепловых электро-
станций постоянно контролируется величина рН питательной воды,
значение которой должно быть на уровне 9,1±0,1. В качестве коррек-
тирующих добавок в питательную воду вводится аммиак, количество
которого можно определить по показаниям рН – метров.
Для измерения рН в лабораторных и промышленных условиях
используются стеклянные рабочие электроды, которые отличаются
широким диапазоном анализируемых сред, высокими метрологиче-
скими характеристиками и простотой конструкции. В стеклянных
электродах водородными функциями обладает чувствительная тонко-
стенная мембрана, выполненная из литиевого или натриевого стекла.
Водородные функции мембраны объясняются тем, что происходит
замещение ионов щелочных металлов (Na, Li), находящихся внутри
силикатной решетки стекла, более подвижными ионами водорода.
Один из вариантов стеклянного рабочего электрода, применяемо-
го для определения рН растворов в промышленных условиях (в част-
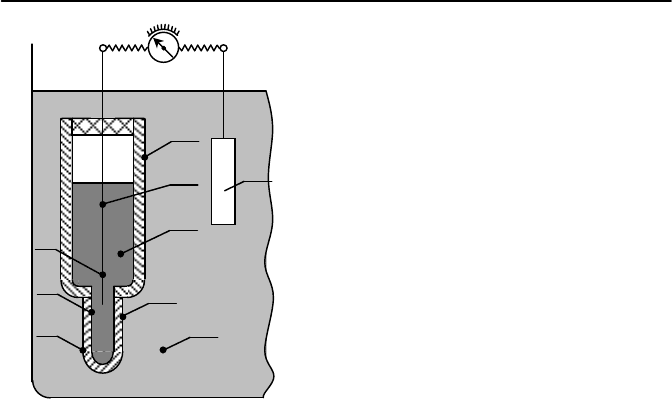
ности на тепловых электростанциях), представлен на рисунке 8.6.
Электрод выполнен из толстостенной стеклянной трубки 1, к концу
которой припаяна чувствительная мембрана из литиевого стекла 4. На
внешней поверхности мембраны при погружении ее в анализируемый
раствор 5 развивается потенциал Е
3
, зависящий от активной концен-
трации ионов водорода. Внутри стеклянного электрода находится рас-
твор кислоты 3 постоянной концентрации, который замыкает электри-
ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
244
ческую цепь между мембраной 4 и
контактным электродом 2. Потенциа-
лы Е
1
(на контактном электроде) и Е
2
(на внутренней поверхности мембра-
ны) остаются постоянными при по-
стоянной температуре раствора.
В качестве вспомогательных
(сравнительных) электродов чаще
всего используют погружной хлорсе-
ребрянный электрод, внутри которо-
го находится серебрянная проволока
(электрод), погруженный в 3,5 нор-
мальный раствор КСl, содержащий
кристаллы хлористого серебра. Элек-
трический потенциал Е
0
, развивае-
мый вспомогательным электродом,
составляет 12 мВ. Выводные контак-
ты с потенциалами Е и Е
0
рабочего и
вспомогательного электродов (ячеек)
подключаются к вторичному измери-
тельному прибору, имеющему гра-
дуировку в единицах рН.
Эксплуатируемые в промыш-
ленности рН – метры работают в
комплекте с автоматическими потенциометрами и имеют пять диапа-
зонов измерения числа рН: 1; 2,5; 10; 15. Предельная допустимая по-
грешность рН – метров составляет ±1,0% диапазона измерения.
Широкое распространение рН – метры получили на тепловых
электростанциях для контроля кислотно-щелочных характеристик пи-
тательной воды паровых котлов.
8.5 Измерение концентрации газов, содержащихся в воде и паре
Растворенные в воде газы и присутствующие в паре, такие как ки-
слород, углекислый газ, водород и другие оказывают вредное влияние
на работу технологического оборудования, которое контактирует с во-
дой и паром. Наибольшую опасность представляет кислород, который
вызывает коррозию металла внутренних поверхностей водяных и паро-
вых трактов различных промышленных и лабораторных установок.
Полное удаление всех газов из воды и пара требует больших за-
Е
Е
о
рН
1
2
3
Е
1
5
Е
2
Е
3
4
6
1 – контактный электрод;
2 – стеклянная трубка; 3 – рас
-
твор кислоты; 4 – мембрана;
5 – анализируемый раствор;
6 – вспомогательный электрод
Рисунок 8.6 – Схема рабочего
стеклянного электрода

ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
245
трат, как энергетических так и материальных в виде химических реа-
гентов, что экономически нецелесообразно. Поэтому, для каждого типа
технологического агрегата устанавливаются регламентные нормы кон-
центрации отдельных компонентов газовой среды в воде и паре Так,
например, для энергетических паровых котлов содержание растворен-
ного кислорода в питательной воде должно составлять 7 – 10 мкг/кг.
Повышение надежности эксплуатации технологического обору-
дования может быть обеспечено непрерывным или периодическим
контролем и автоматическим регулированием содержания растворен-
ного в воде кислорода. В зависимости от концентрации кислорода в
воде используются фотоколориметрические, электрохимические и
кондуктометрические методы.
Фотоколориметрические методы основаны на измерении про-
зрачности (оптической плотности) анализируемой воды, интенсив-
ность окраски которой зависит от концентрации в воде кислорода.
Окрашивание воды производится специальными химическими реак-
тивами, которые изменяют свой цвет при взаимодействии с раство-
ренным кислородом. Измерение интенсивности окрашивания воды
производится специальными химическими реактивами, которые изме-
няют свой цвет при взаимодействии с растворенным кислородом.
Измерение интенсивности окрашивания воды производится в фо-
токолориметрических анализаторах, в которых осуществляется преоб-
разование измеряемой величины (кислородосодержания) в изменение
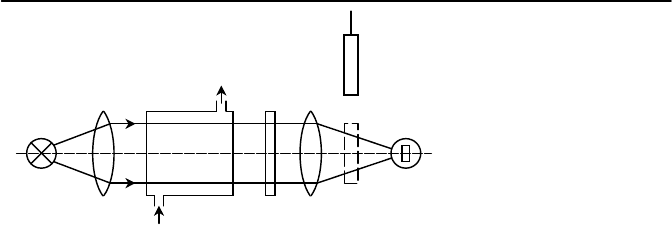
электрического сопротивления фоторезистора (рисунок 8.7). Анализи-
руемая вода набирается в специальную кювету 5, в которую автомати-
чески вводится определенный объем реактива. Степень ослабления све-
тового потока, проходящего через кювету от источника 1, зависит от
интенсивности окраски воды, которая определяется концентрацией рас-
творенного кислорода. Световой поток, падающий на фоторезистор 7, а
следовательно, и электрическое сопротивление его находится в одно-
значной зависимости от измеряемой величины – содержания раство-
ренного кислорода в воде. Фоторезистор включен в мостовую схему
автоматического моста, шкала измерительного прибора которого отгра-
дуирована в единицах массовой концентрации, мг/кг, мкг/кг.
Фотоколориметрические анализаторы кислорода являются при-
борами дискретного действия, что является основным недостатком
приборов этого типа. Однако перевод приборов на непрерывный ре-
жим усложняет их конструкцию и резко увеличивает расход реагентов
для окрашивания воды.
Наибольшее распространение на тепловых электростанциях
ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
246
получили кондукто-
метрические кислоро-
домеры для определе-
ния микроконцентра-
ций растворенного в
воде кислорода. Дей-
ствие кондуктометри-
ческих анализаторов
основано на исполь-
зовании химических
реакций с каким – ли-
бо реагентом, сопро-
вождающихся изме-
нением электропро-
водности анализируемой воды. Основное требование к реагенту – он
должен быстро и полно реагировать с растворенным в воде кислоро-
дом с образованием сильного электролита и не вступать в реакции с
водой и ее примесями.
Из многих опробованных реагентов в наибольшей степени приве-
денным выше условиям удовлетворяет металлический талий (Tl). Од-
нако, следует отметить основной недостаток таллия – токсичность как
самого металла, так и его соединений.
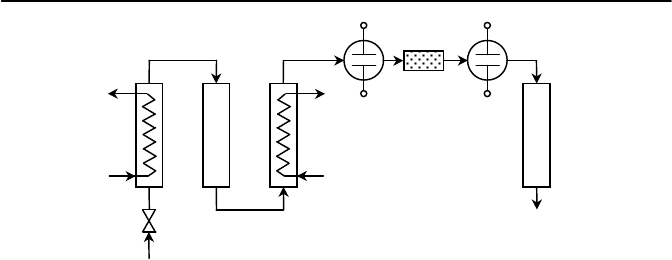
Принципиальная схема кондуметрического анализатора для из-
мерения микроконцентраций растворенного в воде кислорода приве-
дена на рисунке 8.8. Проба анализируемой воды пропускается через
термостат – холодильник 1 и поступает на фильтр 2 для обессолива-
ния воды, заполненный ионообменными смолами. Обессоленная про-
ба пропускается через дополнительный холодильник 3 и кондукто-
метрический преобразователь 4 для измерения начальной электропро-
водности воды и далее в патрон 5 из полиэтилена, заполненный мел-
кодисперсным металлическим таллием. В патроне происходит хими-
ческая реакция взаимодействия таллия с кислородом.
Н
2
О+2Тl+0,5⋅О
2
=2TlOH
Образовавшаяся гидроокись таллия ТlOH хорошо растворяется в
воде и является сильным электролитом, при этом электропроводность
раствора повышается пропорционально содержанию растворенного в
воде кислорода. Изменение электропроводности воды после таллиево-
го патрона фиксируется кондуктометрическим преобразователем 6.
Для очистки воды от токсичных продуктов реакции на выходе прибо-
ра установлен фильтр 7.
1
2
3
4
5
6
7
вода
1 – источник света; 2, 5 – линзы; 3 – рабочая каме-
ра; 4 – светофильтр; 6 – контрольный светофильтр;
7 – фоторезистор
Рисунок 8.7 – Схема фотоколориметрического
анализатора кислорода в воде
ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
247
Измерительная схема кислородомера представляет собой мост, в
котором сопротивления R
1
и R
2
кондуктометрических преобразовате-
лей 4 и 6 включены в противоположные плечи моста. При таком со-
единении изменение электропроводности исходной воды, влияя на
сопротивление обоих преобразователей 4 и 6, не вызывает изменение
небаланса моста. Изменение концентрации кислорода в анализируе-
мой воде приводит к изменению сопротивления R
2
преобразователя 6.
Возникший разбаланс моста, пропорциональный концентрации ки-
слорода, усиливается усилителем, затем преобразуется в выходной
сигнал постоянного тока 0 – 5 мА и измеряется автоматическим мил-
лиамперметром.
Кондуктометрический анализатор выпускается класса точности 6
с диапазоном измерения 0-30 мкг/л О
2
.
Кондуктометрический метод используется также для определе-
ния содержания водорода в питательной воде и пара паровых котлов
на тепловых электростанциях. Появление водорода в пароводяном
тракте котла и величина его концентрации характеризует интенсив-
ность протекания процесса коррозии металла внутренних поверхно-
стей труб. Скорость коррозии металла зависит от водного и темпера-
турного режима эксплуатации парового котла. Непрерывный автома-
тический контроль за водородом в воде и паре позволяет оперативно
вмешиваться в работу котельной установки и устанавливать опти-
мальные режимы работы котла.
Используемые на тепловых электростанциях водородомеры осно-
вода
1
2
3
4
R
1
5
6
R
2
7
1, 3 – холодильники; 2 – фильтр для обессоливания воды; 4, 6 – элек
-
тродные преобразователи; 5 – патрон с таллием; 7 - фильтр
Рисунок 8.8 – Схема кондуктометрического преобразователя для из
-
мерения кислорода в воде
ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
248
ваны на измерении теплопроводности газовой смеси, в которой нахо-
дится водород. В отличии от многих газов, таких как N
2
, CО
2
, CО,
CН
4
, О
2
и других, теплопроводность водорода в 5 – 7 раз выше, что
позволяет с достаточной точностью определять концентрацию водо-
рода в газовой смеси. Для выделения водорода из анализируемой сме-
си (конденсата) ее пропускают через кислородную атмосферу. При
этом, чем больше водорода содержится в воде, тем большее количест-
во его будет выделяться в окружающую кислородную среду. Таким
образом, по концентрации водорода в кислородной среде можно су-
дить о содержании водорода, растворенного в воде (конденсате пара).
Приборы, основанные на измерении теплопроводности газовой смеси,
получили название термокондуктометрическими анализаторами.
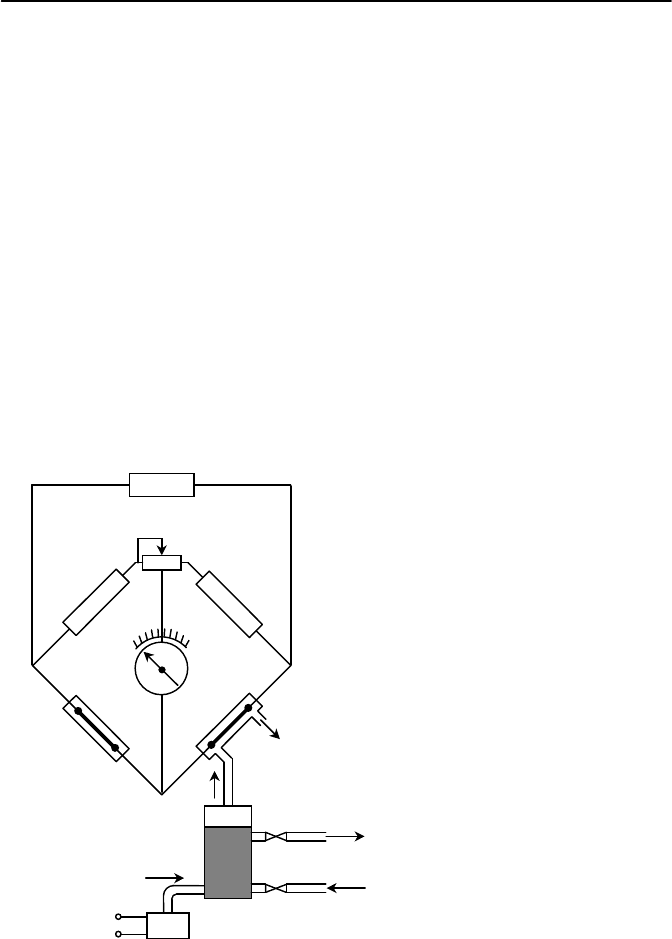
Анализатор состоит из следующих устройств и элементов (рису-
нок 8.9): неуравновешенного моста с манганиновыми резисторами R
1
,
R
0
, R
2
и платиновыми резисторами R
3
, R
4
; стабилизированного источ-
ника питания ИПС; измерительного прибора ИП; электролизера Эл,
заполненного водным раствором едкого калия, для получения чистого
кислорода; приемной колонки ПК, в которую поступает контролируе-
мая проба воды или кон-
денсата пара. Чувстви-
тельный элемент (рези-
стор) R
3
помещен в герме-
тически закрытую камеру,
заполненную чистым ки-
слородом (сравнительным
газом). Чувствительный
элемент (резистор) R
4
по-
мещен в рабочую камеру,
которая соединена с верх-
ней частью приемной ко-
лонки.
Кислород из электро-
лизера непрерывно пода-
ется в приемную колонку
ПК. Одновременно в эту
колонку поступает анали-
зируемая проба конденса-
та или воды, при этом
конденсат (вода) соприка-
сается с газообразным ки-
Рисунок 8.9 – Схема термокондуктомет-
рического анализатора для измерения
водорода в воде или паре
R
2
R
3
R
4
О
2
б
а
R
o
ИПС
R
1
ИП
ПК
О
2
+
–
Эл
вода
О
2
+Н
2

ПРАКТИЧЕСКАЯ
МЕТРОЛОГИЯ
И
ИЗМЕРЕНИЯ
249
слородом и выделяет растворенный водород. Газовая смесь, состоя-
щая из кислорода и водорода, поступает в рабочую камеру с чувстви-
тельным элементом (резистором) R
4
. Наличие водорода в рабочей ка-
мере резко увеличивает теплоотдачу от нагретой до 100 °С платино-
вой проволоки к стенкам камеры за счет увеличения теплопроводно-
сти газового слоя. Температура чувствительного элемента R
4
понижа-
ется, а следовательно, уменьшается его сопротивление. При этом, на
вершинах измерительной диагонали моста из-за нарушения его рав-
новесия появится напряжение, величина которого будет определяться
концентрацией водорода в газовой смеси. Измерительный прибор, ус-
тановленный в газовой диагонали моста, укажет содержание водорода
в питательной воде (конденсате).
Для снижения влияния температуры стенок камеры на показания
измерительного прибора служит плечо сравнения R
3
, аналогичное R
4
и
находящееся в камере, заполненной кислородом, а переменный рези-
стор R
0
служит для начальной балансировки моста (для установки
стрелки измерительного прибора в нулевое положение).
Шкалу вторичного прибора анализаторов, применяемых для оп-
ределения растворенного в воде и паре водорода, градуируют в мик-
рограммах на литр (мкг/л) или в микрограммах на кг (мкг/кг). Диапа-
зон измерения водородомера составляет 0 – 20 и 0 – 200 мкг/кг Н
2
,
предельная погрешность не превышает ±6%.
