Расчёт абсорбционной установки
Подождите немного. Документ загружается.

Уравнение 1.13 показывает, что изменение в абсорбционном аппарате
происходит прямолинейно и, следовательно, в координатах Y-X рабочая линия
процесса абсорбции представляет собой прямую с углом наклона, тангенс которого
равен l = L/G.
Между удельным расходом абсорбента и размерами аппарата, например
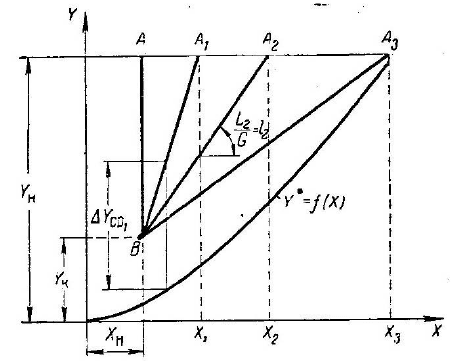
показанного на рис. 11.2, существует определенная связь. Через точку В с
координатами Y
н
и Y
к
(рис 1.2) проведем, согласно уравнению 1.6, рабочие линии
ВА, ВА
1
, ВА
2
, ВА
3
, отвечающие различным концентрациям абсорбента или разным
удельным его расходам. При этом точки А, А
1,
А
2
, А
3
будут лежать на одной
горизонтальной прямой в соответствии с заданной начальной концентрацией Y
н
газа в смеси.
К определению удельного расхода абсорбента
Рис.1.2
В случае растворов небольшой концентрации для любого значения Х и
выбранной величины l движущая сила процесса выражается разностью ординат Y-
Y
*
, изображенных вертикальными отрезками, соединяющими соответствующие
точки рабочей линии и линии равновесия Y
*
=f(X). Для всего аппарата можно
принять среднее значение ∆Y
ср.
, величина которого, например для рабочей линии
ВА
1
, изображена на рисунке отрезком ∆Y
ср.
Величина ∆Y
ср
будет тем больше, чем
круче наклон рабочих линий и, следовательно, чем больше удельный расход
абсорбента. Если рабочая линия ВА совпадает с вертикалью, то движущая сила
процесса имеет максимальное значение, однако удельный расход абсорбента l при
этом будет бесконечно большим (так как X
к
=X
н
). Если же линия рабочих
концентраций ВА
3
касается линии равновесия, то удельный расход абсорбента
минимален (l=l
min
), а движущая сила в точке касания равна нулю, поскольку в этой
точке рабочая концентрация равна равновесной. В первом случае размеры

абсорбционного аппарата будут наименьшими при бесконечно большом расходе
абсорбента, во втором – расход абсорбента наименьший при бесконечно больших
размерах аппарата. Таким образом, оба случая являются предельными и
практически неосуществимыми.
В реальном абсорбционном аппарате равновесие между фазами не
достигается и всегда X
к
<X
*
к
, где X
*
к
– концентрация поглощаемого газа в жидкости,
находящейся в равновесии с поступающим газом. Отсюда следует, что величина l
всегда должна быть больше минимального значения l
min
, отвечающего предельному
положению рабочей линии (линия ВА
3
на рис. 1.2). Значение l
min
можно определить
по уравнению 1.12 при замене X
к
на X
*
к
:
l
min
=
(
L
G
)
min
=
(
Y
н
−Y
к
)
(
X
к
−Х
н
)
(1.14)
Необходимо отметить, что увеличение удельного расхода l абсорбента
одновременно со снижением высоты аппарата приводит к определенному
увеличению его диаметра. Это объясняется тем, что с увеличением l возрастает
также расход поглотителя L, а при этом, снижаются допустимые скорости газа в
аппарате, по которым находят его диаметр. Вот почему в тех случаях, когда
удельный расход абсорбента не задан технологическими условиями, т.е. когда не
задана конечная концентрация X
к
абсорбента, следует выбирать такое соотношение
между размерами абсорбционного аппарата и удельным расходом l абсорбента, при
котором величина l и размеры аппарата будут оптимальными.
Оптимальный удельный расход поглотителя l
опт
может быть найден только с
помощью технико-экономического расчета /1/.
1.1.3. Скорость процесса.
Скорость физической абсорбции.
Скорость процесса абсорбции характеризуется уравнением, если движущую
силу выражают в концентрациях газовой смеси:
M = K
y
.
F
.
∆Y
ср
(1.15)
и уравнением, если движущая сила выражается в концентрациях жидкой
фазы

M = K
x
.
F
.
.∆х
ср
(1.16)
В этих уравнениях коэффициенты массопередачи K
y
и K
x
определяются,
согласно уравнений:
K
y
=
1
1
β
г
+
m
β
ж
и
K
х
=
1
1
β
г
⋅m
+
1
β
ж
,
(1.17)
где β
г
– коэффициент массоотдачи от потока газа к поверхности контакта фаз;
β
ж
- коэффициент массоотдачи от поверхности контакта фаз к потоку.
Как уже отмечалось, для хорошо растворимых газов величина m
незначительна и мало также диффузионное сопротивление в жидкой фазе. Тогда
1
β
г
¿¿
m
β
ж
¿
и можно принять, что K
y
≈ β
г.
Для плохо растворимых газов можно
пренебречь диффузионным сопротивлением в газовой фазе (в этом случае значения
m и β
г.
велики). Отсюда
1
β
ж
¿¿
1
β
г
⋅m
¿
и можно полагать, что K
ж
≈ β
ж.
В уравнении мольные концентрации газовой фазы могут быть заменены
парциальными давлениями газа, выраженными в долях общего давления. Тогда
M
/
= K
p
.
F
.
∆p
ср
, (1.18)
где p
ср
– средняя
движущая сила процесса, выраженная в единицах давления;
K
p
– коэффициент массопередачи, отнесенный к единице движущей силы,
выражаемой через парциальные давления поглощаемого газа.
Если линия равновесия является прямой, то средняя движущая сила процесса
выражается уравнением:
Δр
ср
=
Δр
б
−Δр
м
2, 3⋅lg
Δр
б
Δр
м
,
(1.19)
где ∆p= p
н
– p
*
к
и ∆p
м
= p
к
– pº
н
– движущая сила на концах абсорбционного
аппарата;
p
н
и p
к
– парциальные давления газа на входе в аппарат и выходе из него;
p
к
и pº
н
– равновесные парциальные давления газа на входе в аппарат и
выходе из него.
Если парциальное давление выражено в долях общего давления Р, то
коэффициенты массопередачи K
p
и
K
y
численно равны друг другу. Если же
парциальные давления выражены в единицах давлениях, то
K
p
= Р
.
K
y
(1.20)
Скорость абсорбции, сопровождаемой химической реакцией.
Во многих практически важных процессах абсорбции поглощение газа
жидкостью сопровождается химическим взаимодействием фаз. Если реакция
протекает в жидкой фазе, то часть газообразного компонента переходит в
связанное состояние. При этом концентрация свободного (т.е. не связанного с
поглощаемым газом) компонента в жидкости уменьшается, что приводит к
ускорению процесса абсорбции по сравнению с абсорбцией без химического
взаимодействия фаз, так как увеличивается движущая сила процесса. В общем
случае скорость хемосорбции зависит как от скорости реакции, так и от скорости
массопередачи между фазами. В зависимости от того, какая скорость определяет
общую скорость процесса переноса массы, различают кинетическую и
диффузионную области протекания хемосорбционных процессов.
В кинетической области скорость собственно химического взаимодействия
меньше скорости массопередачи и поэтому лимитирует скорость всего процесса. В
диффузионной области лимитирующей является скорость диффузии компонентов в
зоне реакции, которая зависит от гидродинамики и физических свойств фаз и
определяется по общему уравнению массопередачи.
В тех случаях, когда скорости реакции и массопередачи соизмеримы по
величине, процессы абсорбции протекают в смешанной, или диффузионно-
кинетической, области.
При расчете требуемой поверхности контакта фаз в условиях хемосорбции
ускорение процесса можно учесть увеличением коэффициента массоотдачи β
ж
,
если считать движущую силу процесса такой же, как при физической абсорбции.
Тогда коэффициент массоотдачи в жидкой фазе β
/
ж
при протекании химической
реакции
β
/
ж
= β
ж
.
Φ, (1.21)
где Φ – фактор ускорения массообмена, показывающий, во сколько раз
увеличивается скорость абсорбции за счет протекания химической реакции /1/.
1.2. Основные технологические схемы для проведения процесса
Промышленные схемы абсорбционных установок бывают противоточные,
прямоточные, одноступенчатые с рециркуляцией и многоступенчатые с
рециркуляцией.
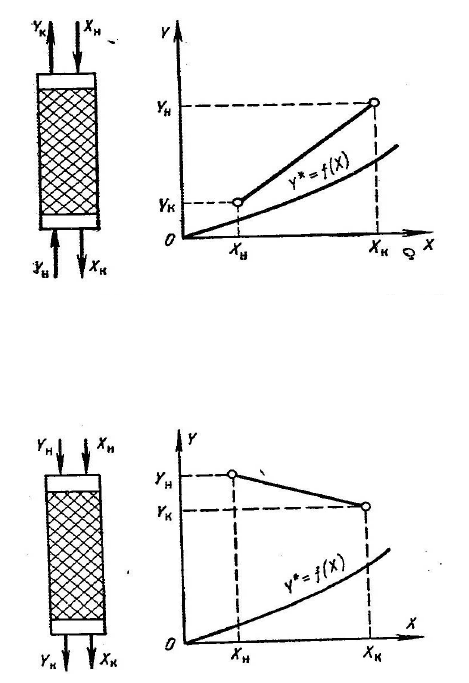
При противоточной схеме абсорбции (рис.1.3) газ проходит через абсорбер
снизу вверх, а жидкость стекает сверху вниз. Так как при противотоке уходящий
газ соприкасается со свежим абсорбентом, над которым парциальное давление
поглощаемого компонента равно нулю (или очень мало), то можно достичь более
полного извлечения компонента из газовой смеси, чем при прямоточной схеме
(рис. 1.4), где уходящий газ соприкасается с концентрированным раствором
поглощаемого газа. Кроме того, при противотоке можно достигнуть более высокой
степени насыщения поглотителя извлекаемым компонентом, что, в свою очередь,
приводит к уменьшению расхода абсорбента.
Схема противоточной абсорбции
Рис.1.3
Схема прямоточной абсорбции
Рис.1.4
Для отвода тепла, выделяющегося при абсорбции, а также для повышения
плотности орошения часто применяют схемы с рециркуляцией части абсорбента.
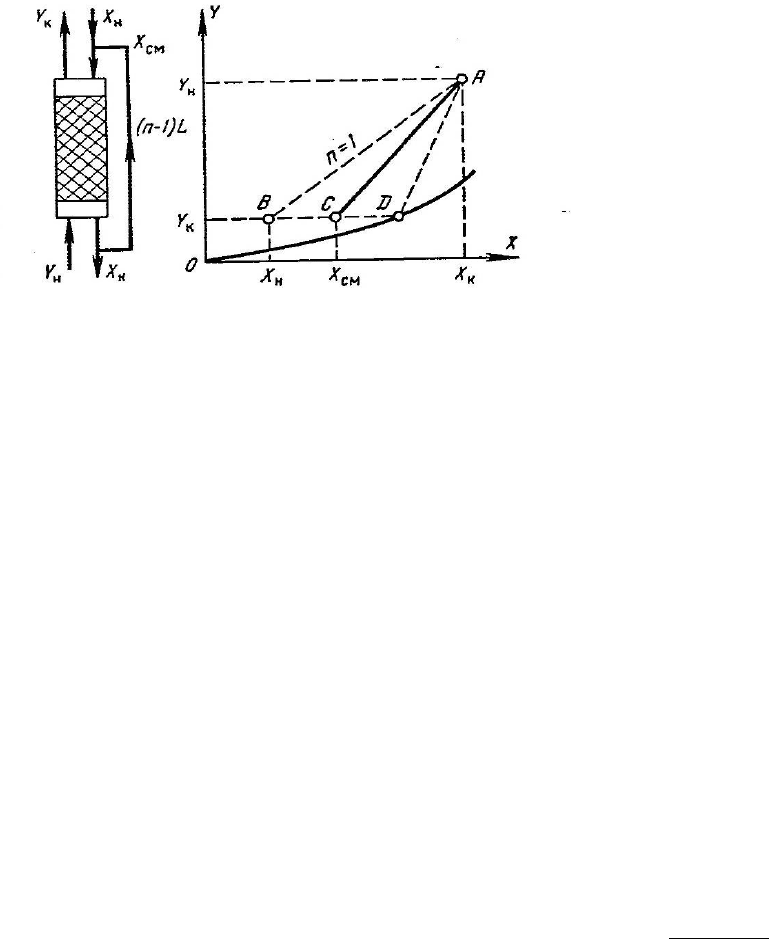
На рис.1.5 представлена схема одноступенчатой абсорбции с частичной
рециркуляцией абсорбента. Часть жидкости концентрацией Х
к
отбирается из
нижней части колонны в качестве конечного продукта, а другая ее часть
возвращается насосом на верх колонны, где жидкость присоединяется к
поглотителю, имеющему начальную концентрацию Х
н
. В результате образуется
смесь, концентрация которой равна Х
см
, причем Х
см>
Х
н
.
Схема одноступенчатой абсорбции с рециркуляцией жидкости
Рис.1.5
Жидкость, возвращается в колонну, может быть попутно охлаждена, что
приведет к понижению температуры жидкости, орошающей колонну и
соответственно – к понижению температуры процесса.
Обозначим через n кратность циркуляции, или отношение числа киломолей
жидкости, протекающей через абсорбер, к числу киломолей исходной жидкости.
Тогда через абсорбер будет проходить nL кмоль и рециркулировать (n-1)L кмоль
поглотителя, где L – расход поглотителя. Соответственно материальный баланс
процесса выразится уравнением
G
.
(Y
н
-Y
к
) = L
.
(X
к
-X
н
) = n
.
L
.
(Х
к
-Х
см
) (1.22)
откуда кратность циркуляции равна
n=
X
к
−Х
н
Х
к
−Х
см

(1.23)
Концентрация абсорбента в смеси на входе в колонну:
Х
см
=
Х
н
−
(
1−n
)
⋅Х
к
n
(1.24)
Линия АВ на диаграмме Y-X (рис.1.5) отвечает абсорбции без рециркуляции
(т.е. при n=1), причем наклон этой линии равен отношению расходов фаз L/G. При
наличии рециркуляции рабочая линия имеет большой наклон (nL/G) и выражается
отрезком АС. Наклон рабочей линии возрастает с увеличением n, однако
предельное положение рабочей линии соответствует прямой AD, точка D которой
находится на линии равновесия. Это положение рабочей линии отвечает
максимальной величине n, когда поступающая в колонну смесь находится в
равновесии с уходящим газом.
Схема многоступенчатой абсорбции с рециркуляцией части жидкости
приведена на рис.1.6. При этом газ проходит последовательно через все колонны
навстречу жидкости. На диаграмме Y-X рабочая линия для всей системы
изображается прямой АВ. Эта прямая состоит из отрезков АС, СD и DВ,
соответствующих рабочим линиям для отдельных колонн. При отсутствии
рециркуляции данную систему можно было бы рассматривать как один абсорбер,
разделенный на части. Если каждая отдельная колонна работает с рециркуляцией
жидкости, то рабочие линии для каждой из этих колонн выразятся отрезками А
/
С,
С
/
D и D
/
В. Рассмотренная схема широко распространена в промышленности.
Схема многоступенчатой противоточной абсорбции с рециркуляцией
жидкости в каждом абсорбере
Рис.1.6
Количество жидкости, проходящей через абсорберы, работающие по схеме с
рециркуляцией поглотителя, при одном и том же расходе свежего абсорбента
значительно больше, чем в схемах без рециркуляции. В результате увеличивается
коэффициент массоотдачи в жидкой фазе при некотором снижении движущей
силы процесса.
Применение схем с рециркуляцией поглотителя целесообразно в следующих
случаях:
1) когда основное сопротивление массопередаче сосредоточено в жидкой
фазе;
2) при необходимости охлаждать поглотитель в процессе абсорбции;
3) для улучшения смачивания насадки (при малых плотностях орошения).
Вместе с тем рециркуляция жидкости приводит к усложнению абсорбционных
установок и дополнительным расходам энергии на перекачивание
рециркулирующей фазы.
Схемы установок, приведенные на рис.1.5-1.7, относятся к насадочным
абсорберам, в которых затруднительна организация внутреннего отвода тепла в
процессе абсорбции. В тарельчатых абсорберах охлаждающие устройства
(например змеевики) устанавливают непосредственно на тарелках, что является
существенным преимуществом этих аппаратов при проведении в них процессов
абсорбции, протекающих со значительным выделением тепла.
На рис.1.7 представлена схема абсорбционной установки с рециркуляцией
жидкости и десорбцией. Насыщенный поглощенным компонентом абсорбент из
последнего (по ходу жидкости) абсорбера 1 сливается в сборник 2, откуда насосом
5 через теплообменник 8 подается в десорбционную колонну 9, где освобождается
от растворенного газа. Регенерированный поглотитель из колонны 9 поступает в
теплообменник 8, где отдает тепло жидкости, направляемой на десорбцию, и далее
через холодильник 10 возвращается в цикл орошения первого (по ходу жидкости)
абсорбера /1/.
Схема абсорбционной установки с рециркуляцией жидкости и
десорбцией

1 – абсорбер, 2-4 – сборники, 5-7 – насосы, 8 – теплообменник,
9 - десорбционная колонна, 10 – холодильники
Рис.1.7
1.3. Типовое оборудование для проектируемой установки.
Аппараты, в которых осуществляются абсорбционные процессы, называется
абсорберами. Как и другие процессы массопередачи, абсорбция протекает на
поверхности соприкосновения между жидкостью и газом. По способу образования
этой поверхности абсорберы можно условно разделить на следующие группы:
1) поверхностные и пленочные;
2) насадочные;
3) барботажные (тарельчатые);
4) распыливающие.
Следует отметить, что аппараты большинства конструкций, приводимых
ниже, весьма широко применяются и для проведения других массообменных
процессов /1/.
1.3.1. Поверхностные и пленочные абсорберы.
В абсорберах этого типах поверхностью соприкосновения фаз является
зеркало неподвижной или медленно движущей жидкости, или же поверхность
текущей жидкой пленки.
Поверхностные абсорберы.
Эти абсорберы используют для поглощения хорошо растворимых газов
(например, для поглощения хлористого водорода водой). В указанных аппаратах
газ проходит над поверхностью неподвижной или медленно движущейся жидкости

(рис.1.8). Так как поверхность соприкосновения в таких абсорберах мала, то
устанавливают несколько последовательно соединенных аппаратов, в которых газ
и жидкость движутся противотоком друг к другу. Для того чтобы жидкость
перемещалась по абсорберам самотеком, каждый последующий по ходу жидкости
аппарат располагают несколько ниже предыдущего. Для отвода тепла,
выделяющегося при абсорбции, в аппаратах устанавливают змеевики,
охлаждаемые водой или другим охлаждающим агентом, либо помещают абсорберы
в сосуды с проточной водой.
Поверхностный абсорбер
Рис.1.8
Более совершенным аппаратом такого типа является абсорбер (рис.1.9),
состоящий из ряда горизонтальных труб, орошаемых снаружи водой.
Необходимый уровень жидкости в каждом элементе 1 такого аппарата
поддерживается с помощью порога 2.
Оросительный абсорбер
1 – элемент абсорбера, 2 – сливные пороги
Рис.1.9
Пластинчатый абсорбер (рис.1.10) состоит из двух систем каналов: по
каналам 1 большого сечения движутся противотоком газ и абсорбент, по каналам 2
меньшего сечения – охлаждающий агент (как правило вода). Пластинчатые
