Получение формальдегида
Подождите немного. Документ загружается.

№1
Изложите товарные и определяющие технологию свойства
формальдегида, область применения.
Формальдегид (муравьиный альдегид) НСНО – бесцветный газ с
резким раздражающим специфическим запахом (т.конд. -19 ºС; т. кип. -21ºС;
т. пл. 92ºС). Хорошо растворим в воде. В водных растворах находится почти
исключительно в гидратированной форме – в виде метиленгликоля СН
2
(ОН)
2
и продуктов его полимеризации – полиоксиметиленгликолей НО(СН
2
О)
n
Н (n
колеблется от 8 до 100). Чем концентрированнее водный раствор
формальдегида, тем больше в нем полиоксиметиленгликолей.
Водный раствор формальдегида (33-40% об. НСНО) выпускается под
названием формалина. При хранении может полимеризоваться. Для
предотвращения полимеризации формальдегида в растворе формалина
обычно стабилизируют метиловым спиртом, содержание которого
колеблется от 6 до 13% вес.
Формальдегид является протоплазматическим ядом. В очень малых
концентрациях он раздражает слизистые оболочки глаз, а в несколько
большей концентрации действует раздражающе на слизистые оболочки
дыхательных путей; вдыхание формальдегида высокой концентрации может
привести к гнойному воспалению легких. Формальдегид вызывает также
раздражение кожи, переходящее в воспалительный процесс. Предельно
допустимая концентрация паров формальдегида в воздухе производственных
помещений 1 мг/м
3
. [1]
Формальдегид обладает высокой реакционной способностью.
Восстанавливается Н
2
в присутствии многих металлов или их оксидов
(например, Ni, Pt, Cu) до метанола; окисляется HNO
3
, KMnO
4
до муравьиной
кислоты или CO
2
и H
2
O; осаждает многие металлы (Ag, Pt, Bi и др.) из
растворов и солей, окисляясь при этом в муравьиную кислоту.
С альдегидами в присутствии сильных щелочей формальдегид вступает
в так называемую перекрестную реакцию Канниццаро (C
6
H
5
CHO + HCHO
NaOH
C
6
H
5
CH
2
OH + НCOONa); с ацетальдегидом в присутствии Ca(OH)
2
образует пентаэритрит, в паровой фазе при 285ºС – акролеин: под действие
алкоголятов AL или Mg формальдегид подвергается
диспропорционированию с образованием метилфомиата.
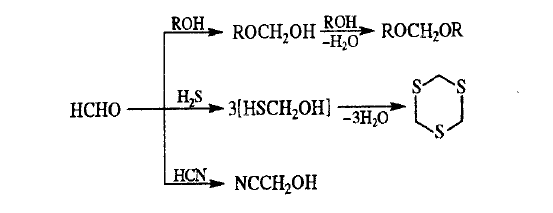
Реакция формальдегида со спиртами в присутствии сильных кислот
приводов к ацеталям (формалям), с H
2
S – к циклич. тритиану, с HCN в
присутствии щелочей – к циангидриду:
Формальдегид присоединяется к олефинам в присутствии кислых
катализаторов с образованием 1,3-дигликолей и 1,3-диоксанов, реакция
формальдегида с изобутиленом дает изопрен, жидкофазная конденсация с
пропиленом в присутствии BF
3
или H
2
SO
4
– бутадиен. Из формальдегида и
кетена в промышленности получают β-пропиолактон.
Ароматические соединения (бензол, анилин, толуол) образуют с
формальдегидом соответствующие диарилметаны: в присутствии HCI бензол
хлорметилируется формальдегидом по Блана реакции, образуя бензилхлорид;
с фенолами в присутствии кислот или оснований формальдегид
конденсируется с образованием орто- и пара-метилольных производных,
которые далее превращаются в феноло-формальдегидные смолы. Продукты
конденсации формальдегида с фенол- и нафталинсульфокислотами
используют как дубильные вещества. [2]
Формальдегид, открытый Гофманом в 1867 г., применяется сейчас как
исходный продукт в многочисленных органических синтезах, а также как
дезинфицирующее и дезинсекционное средство.
2
В наибольших количествах формальдегид потребляется для
производства полимеризационных и поликонденсационных полимеров
(полиформальдегида, феноло-формальдегидных, карбамидных, меламиновых
и др. смол), являющихся основой пластических масс, пленкообразующих и
пропитывающих материалов, клеев и т. д. Применяется для производства
антиокислительных, антикоррозионных, противозадирных, моющих
присадок. За последние годы формальдегид начали использовать для
получения изопрена и бутадиена – важных мономеров промышленности
синтетических каучуков. На основе формальдегида можно получать
синтетические смолы для химических волокон (нейлон, капрон),
этиленгликоль, глицерин, пентаэритрит, красители, взрывчатые вещества,
фармацевтические препараты и т. п. [1]
ПДК в атмосферном воздухе 0,003 мг/м
3
, в воздухе рабочей зоны 0,5
мг/м
3
, в воде водоемов хозяйственно-бытового пользования 0,05мг/л.
Температура самовоспламенения 430ºС, КПВ при 20ºС 7-72%об. [2]
3
№2
Укажите сырьевые источники для получения формальдегида.
В промышленности формальдегид получают, окислит.
дегидрированием метанола в паровой фазе О
2
воздуха в присутствии Ag или
серебряной сетки при 600-650ºС (конверсия 77-87%) с возвращением
непрореагировавшего метанола в рецикл. Процесс можно проводить в
присутствии оксидов металлов (Fe-Mo-V) при 250-400ºС (конверсия 98-
99%). Формальдегид может быть получен окислением метана, пропана,
бутана, этилена, гидрированием оксида углерода(II), однако эти методы не
имеют промышленного значения по экономическим причинам.
Получение формальдегида неполным окислением концентрированного
метана кислородом воздуха с использованием в качестве катализатора
окислов азота (гомогенный катализ). Окисление проводят в реакторе
трубчатого типа при температуре около 600ºС. Трубки изготовлены из
жароупорного сплава сихромаля и футерованы изнутри керамической массой
(80% SiO
2
, 20% AL
2
O
3
). Выход формальдегида составляет 38% от
прореагировавшего метана. При окислении метана образуются помимо
формальдегида и другие продукты реакции, например, муравьиная кислота,
оксид углерода(II), оксид углерода(I), водород, поэтому из реакционной
смеси формальдегид выделяют конденсаций или поглощением водой с
последующим его выделением.
Другим способом получения формальдегида является окислительное
дегидрирование метилового спирта в присутствии катализаторов. Последние
можно разделить на две группы:
a) окисные катализаторы, например окисные железо-молибденовые,
в некоторых случаях с присадками окислов других металлов
(магния, марганца, кадмия);
б) металлическая медь или серебро в виде металлической сетки или
осажденные на инертном высокопористом носителе (например, на
пемзе).
4
№3
Кратко охарактеризуйте современные промышленные способы
получения формальдегида.
Существует множество вариантов технологического оформления
процесса окислительного дегидрирования метанола в формальдегид. Однако
принципиально все методы основаны на пропускании смеси паров
метилового спирта с воздухом над катализатором при повышенных
температурах.
Окисление проводят в реакторе трубчатого типа при температуре около
600ºС. Трубки изготовлены из жароупорного сплава сихромаля и футерованы
изнутри керамической массой (80% SiO
2
, 20% AL
2
O
3
). Схема производства
формальдегида представлена на рис.1. [2]
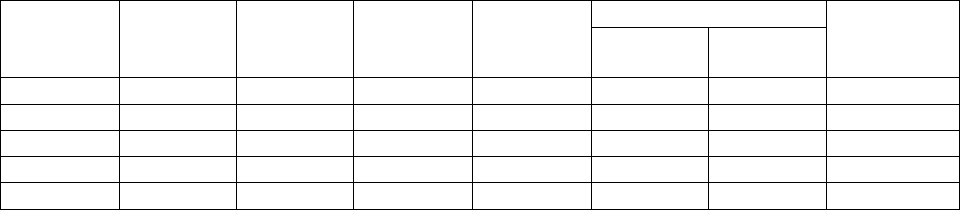
1 – горелка; 2 – теплообменник; 3 – реактор; 4 – газодувка; 5 – водяной холодильник; 6 –
водяной скруббер; 7 – емкость для нейтрализации раствора формальдегида; 8 – выносной
кипятильник; 9 – ректификационная колонна; 10 – дефлегматор; 11 – сборник формалина.
Рис. 1. Технологическая схема производства формальдегида окислением
метана кислородом воздуха в присутствии гомогенных катализаторов
(окислов азота):
5
На рис. 1 показана схема получения формальдегида неполным
окислением концентрированного метана кислородом воздуха с
использованием в качестве катализатора окислов азота (гомогенный катализ).
Метан и воздух в объемном отношении 3,7 : 1, предварительно
подогретые до 400ºС в теплообменнике 2, поступают в реактор 3. Перед
входом реактор к газам добавляют 0,08% об. паров азотной кислоты,
образуемой в результате окисления аммиака кислородом воздуха в горелке 1.
Продукты реакции охлаждаются в теплообменнике 2, а затем в водяном
холодильнике 5 и поступают в скруббер 6, где формальдегид отмывают
водой. Из верхней части скруббера 6 выходит газ, содержащий 12% СН
4
, 5%
СО, 2% СО
2
, 6% О
2
и 75% N
2
. Часть этого газа возвращают в реактор, так
чтобы на один объем исходной смеси приходилось девять объемов
рециркулирующего газа.
Вытекающий из скруббера 6 водный раствор формальдегида с
содержанием до 10% НСНО нейтрализуют в аппарате 7 щелочью для
связывания муравьиной кислоты. Далее раствор подвергают ректификации
под давлением 4 ат в колонне 9, где получают 34%-ный раствор
формальдегида, содержащий 3% вес. метилового спирта. Выход
формальдегида составляет 38% от прореагировавшего метана.
Процесс на серебряном катализаторе протекает при более высокой
температуре – в пределах 600-650ºС. Формалин, получаемый на серебряном
катализаторе, содержит до 10% метанола. Для отделения метанола
получаемый формалин подвергают ректификации. При окислительном
дегидрировании метанол на серебряном катализаторе выход формальдегида
зависит от способа приготовления катализатора, и колеблются от 82 до 92%.
При использовании окисных катализаторов температуру процесса
поддерживают в пределах 300-400ºС; образующийся при этом формалин
содержит небольшое количество метилового спирта (~1%). Выход
формальдегида на окисных катализаторах высокий – достигает 90% и более.
[1]
6
№4
Опишите физико-химические закономерности процесса получения
формальдегида путем каталитического окисления метанола кислородом
воздуха. Определите тип процесса.
Принципиально все методы получения формальдегида основаны на
пропускании смеси паров метилового спирта с воздухом над катализатором
при повышенных температурах.
В качестве катализаторов применяют побочные процессы окисления,
дегидрирования и гидрирования до образования окиси и двуокиси углерода и
других продуктов.
При использовании окисных катализаторов температуру процесса
поддерживают в пределах 300-400ºС; образующийся при этом формалин
содержит небольшое количество метилового спирта (~1%). Выход
формальдегида на окисных катализаторах высокий – достигает 90% и более.
[1]
При испытании в качестве активной основы Na
3
PV
7
W
5
O
40
(2,3%)
показано, что выход формальдегида резко возрастает с переходом от AL
2
O
3
и
угля к носителям, в структуре которых в значительных количествах
присутствует звено Si-O.
Существенное влияние на выход продуктов парциального окисления
метана оказывает содержание гетерополикислот (ГПК) на носителе. Так, в
присутствии кремниймолибденовой кислоты, нанесенной на алюмосиликат,
выход формальдегида растет с уменьшением содержания ГПК на носителе с
10 до 2% масс.; дальнейшее понижение концентрации до 1% заметно
ухудшает достигнутые результаты. Так, выход формальдегида в последнем
случае снижается с 12 до 5%.
На катализаторе 2,3% Y
2
SiMo
12
O
40
/AL
2
O
3
-SiO
2
при 500ºС выход
формальдегида составляет 0,5 % в отсутствии паров и 3,4% после обработки
ею. Последующая повторная обработка катализатора паро-воздушной
7
смесью позволяет во времени увеличить выход целевого продукта до 7 % и
выше. Аналогичная закономерность наблюдается и на катализаторах типа
Na
4
PFeMo
11
O
39
, Na
3
PV
7
W
5
O
40
. В таблице 1 приведены более подробные
данные по влиянию паров воды и соответственно реагентов в разбавленных
по метану реакционных смесях.
Таблица 1. Влияние соотношения СН
4
:О
2
и водяного пара на окисление
метана в формальдегид:
Соотно-
шение
СН
4
:О
2
Нали-
чие
Н
2
О
Темпе-
ратура,
ºС
Конвер-
сия,
%
Селектив-
ность,
%
Выход формальдегида Производи-
тельность
г/л
кт
ч
% г/нм
3
1:20 - 600 30 20 6,0 90
1:20 + 600 32,3 21,4 6,9 109 3,6
1:20 + 650 53,6 23,1 12,2 188 6,3
1:10 + 600 31,1 19,8 6,2 95 3,2
1:0,5 + 600 44,1 36,6 16,1 258 52,0
(Na
3
PMo
12
O
40
/AL
2
O
3
-SiO
2
, CH
4
- <5% об., линейная скорость 11,8 л/ч).
Из данных таблицы 1 видно, что при обработке катализатора парами
воды и при варьировании соотношения метан-кислород можно заметно
увеличить конверсию метана и, соответственно, выход формальдегида; к
тому же существенно возрастает производительность процесса.
Следует отметить, что в смесях с содержанием метана выше верхнего
предела взрываемости наблюдается преимущественное образование
формальдегида, а в разбавленных по метану средах – также продуктов его
окислительной конденсации.
Для некоторых низкопроцентных катализаторов из ГПС 12-го ряда
молибдена в разбавленных смесях (СН
4
:О
2
=1:20) наблюдается выраженное
влияние соотношения метан-пара на направление окислительного
превращения метана. При действии избытка паров воды создаются
оптимальные условия для образования формальдегида, так и сопутствующих
продуктов, однако, появляются значительные количества пропана. 10-15-
кратное снижение паров воды в реакционной смеси снижают выход
формальдегида, ингибирует образование С
2
Н
6
и С
3
Н
8
; наблюдается в
продуктах реакции только этилен. Следовательно, в данном случае вода
выступает в качестве окислителя, что характерно для других процессов. [3]
8
№5
Изобразите и опишите аппаратурно-технологическую схему.
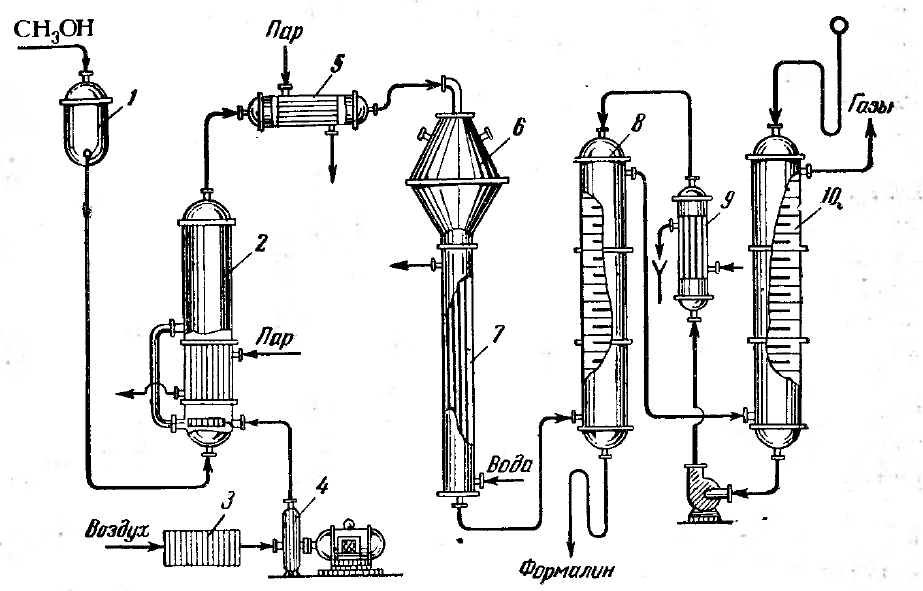
На рис. 2 показана схема получения формалина окислительным
дегидрированием метилового спирта на серебряном катализаторе
1 - мерник; 2 – испаритель; 3 – фильтр; 4 – воздуходувка; 5 – подогреватель;
6 – контактный аппарат; 7 – холодильник; 8,10 – абсорберы; 9 –
промежуточный холодильник.
Рис. 2. Схема производства формалина окислением метилового спирта:
Метиловый спирт через мерник 1 подают в испаритель 2,
обогреваемый глухим паром или горячей водой. Одновременно через
испаритель пропускают очищенный от пыли и других примесей воздух,
нагнетаемый воздуходувкой 4. Барботируя через слой спирта, нагретого до
45-50ºС, воздух насыщается его парами до содержания примерно 0,5 г
СН
3
ОН в 1 л паро-воздушной смеси, что значительно превышает верхний
придел взрываемости смеси паров метилового спирта с воздухом.
Весьма важно поддерживать постоянный состав паро-воздушной
смеси, так как при повышенном содержании паров спирта побочные реакции
9
протекают более интенсивно, а при пониженном содержании спирта может
образоваться взрывоопасная смесь.
Даже при незначительных колебаниях состава паро-воздушной смеси
нарушается нормальный ход процесса, потому систему снабжают
автоматическими регуляторами уровня спирта в испарителе, температуры
воздуха и спирта, давления в системе.
Во избежание конденсации паров спирта из паро-воздушной смеси ее
подогревают в аппарате 5 глухим паром до 110ºС и при этой температуре
подают в контактный аппарат 6. При установившемся процессе окисление
протекает аутотермически. Температурный режим в контактном аппарате
регулируют, изменяя температуру и количество подаваемой парогазовой
смеси. В период пуска системы для инициирования реакции используют
платино-асбестовый контактный запал (предложен Е.И. Орловым),
устанавливаемый на входе газа в слой катализатора, либо электрозапал.
Продукты реакции, выходящие из контактного аппарата, охлаждают в
холодильнике 7 до 100-130ºС. Охлаждение до более низкой температуры
нежелательно, так как при этом возможны полимеризация формальдегида и
забивание трубопровода полимерами.
Далее в абсорберах 8 и 10 из контактных газов поглощается
формальдегид. Абсорбер 10 орошается водой, абсорбер 8 – разбавленным
раствором формальдегида, поступающим из абсорбера 10. Для отвода тепла
абсорбции устанавливают промежуточные холодильники (на схеме показан
один). Из абсорбера 8 вытекает формалин – водный раствор формальдегида,
содержащий 37,6% НСНО и около 10% СН
3
ОН; последний стабилизирует
формальдегид, предотвращая его полимеризацию. Выход формальдегида
около 90%. [1]
10
