Лабораторная работа №1
Подождите немного. Документ загружается.


ГОЧ ВПО Ижевский Государственный Технический Университет Кафедра химии и химической технологии
Лабораторная работа
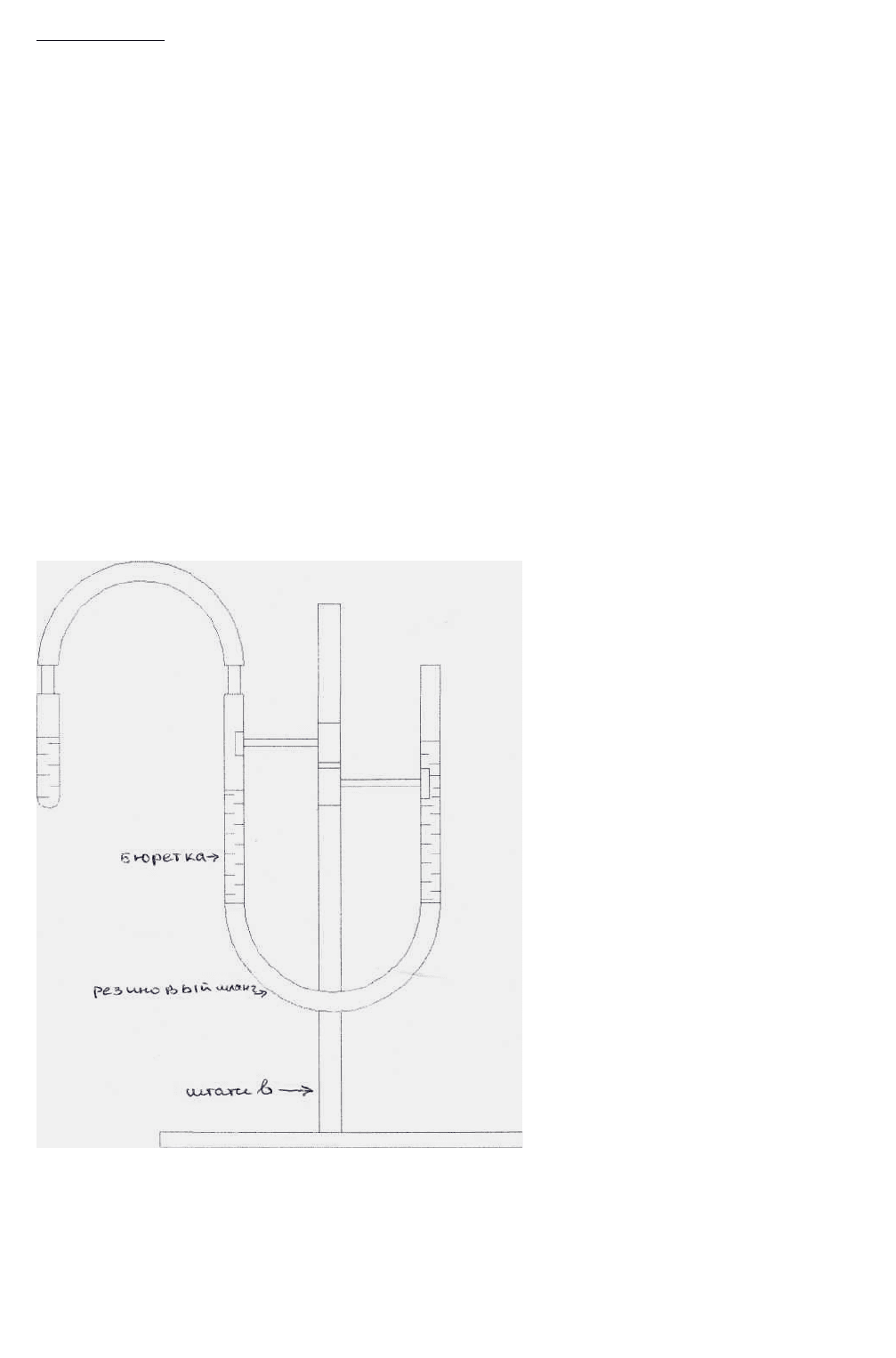
Определение эквивалента металла объемным методом
Выполнил:
Ст. гр. 3-75-2
Шустов М. С.
Проверил:
К.т.н, доц.
Бондарь А. Ю.
Ижевск 2008
Цель работы : определить эквивалент неизвестного металла, его эквивалентную массу и
относительную ошибку опыта.
Теоретическая часть:
Эквивалент.
Эквивалент - Реальная или условная частиц в-ва которая может заменять, присоединять, высвобождать ,
а также быть каким- либо др образом – равнозначной одному атому или иону водорода, ионы обменов
кислотных остатков, либо одному электрону в окислительно-восстановительных реакциях.
Молярная масса эквивалента.
Молярная масса эквивалента M[(1/z)X] есть отношение молярной массы M(X) вещества к числу
эквивалентности. Например, M(1/1HCl) = 36,46/1=36,46 г/моль; M[1/6Fe2(SO4)3] = 399,88/6 = 66,65 г/моль.
Закон эквивалентов.
Закон эквивалентов: массы реагирующих и образующихся веществ относятся друг к другу, как их эквивалентные
массы.
Экспериментальная часть:

Экспериментальные данные:
Р
атм
=758 мм.рт.ст t° -20°Г
t
0
ком
=20
0
С
h=17,535 мм.рт.ст.
Т
О
=273 К
Р
о
=760 мм.рт.ст.
Т
1
=273+20=293 К
Р
1
=758-17.535=740,465 мм.рт.ст.
т(Ме)=0,0152 г.
n=3 кол-во в-ва
V(Н
2
)=20мл.
М(Н
2
)
=
2г/моль=22,4г/моль
Э(Н
2
)=1г/моль=11200 мл.
Расчетная часть:
1) По объединенному закону газовому закону, приводящему V(H
2
) к нормальным условиям
2)по закону
эквивалентов определить эквивалент
металла
3)определяем эквивалентную массу
М(Ме) = Э(Ме) * n = 28,14 г/моль
4) Аr(Ме)=М(Ме)=28 а.е.м.
из таблицы Менделеева наиболее близко подходящее к атомной массе - алюминий
5)относительная ошибка опыта
P
o
V
o
T
o
=
P
1
V
1
T
1
V
o
( H
2
)=
T
o
P
1
V
1
( H
2
)
P
o
T
1
=
273 K∗740 . 465 мм. рт. ст.∗20 мл
760 мм. рт.ст .∗293 К
=
4042938 , 9
222680
=18 ,1558241
Э( Me )=
m( Me )Э( H
2
)
V
o
( H
2
)
=9 .3766≈9. 38
V (H
2
)
m( Me)
=
Э( H
2
)
Э( Me)
|
Ar ( Me)теор− Ar (Me )эксп
Ar ( Me)теор
|∗100 %= 0 ,03333 %

Вывод:
2Аl
0
+6НСl=2АlСl
3
+ЗН
2
Аl°-Зе ->Аl
+3
окислитель восстанавливается
2Н
+
+2е ->Н
2
° восстановитель окисляется
Рассчитали эквивалент металла, он равен 9,3766, эквивалентную массу равную 28г/моль,
относительная ошибка 0,03333%
Относительная ошибка опыта получилась в следствии неточностей в экспериментах, и не точных
расчетов (мы брали приблизительные числа при расчетах), но эта относительная ошибка не так
велика, по этому мы можем ей пренебречь.
