Газы, изопроцессы, газовые формулы
Подождите немного. Документ загружается.

ГАЗЫ
Условные обозначения:
p Давление
V Объем
T Температура
n Концентрация
N
А
Постоянная Авогадро
m Масса газа
M Молярная масса
R Универсальная газовая постоянная
Формулы:
n=
V
N
=
M
m
V
1
N
A
Концентрация газа
pV=
M
m
kN
A
T
[Подставить kN
A
]
pV=
M
m
RT
Уравнение состояния для произвольной массы идеального газа
(уравнение Менделеева – Клапейрона)
1
11
T
Vp
=
M
m
R
Уравнение для газа данной массы
Газовые законы:
Изотермический процесс. Процесс изменения состояния термодинамической
системы макроскопических тел при постоянной температуре называдт
изотермическим.
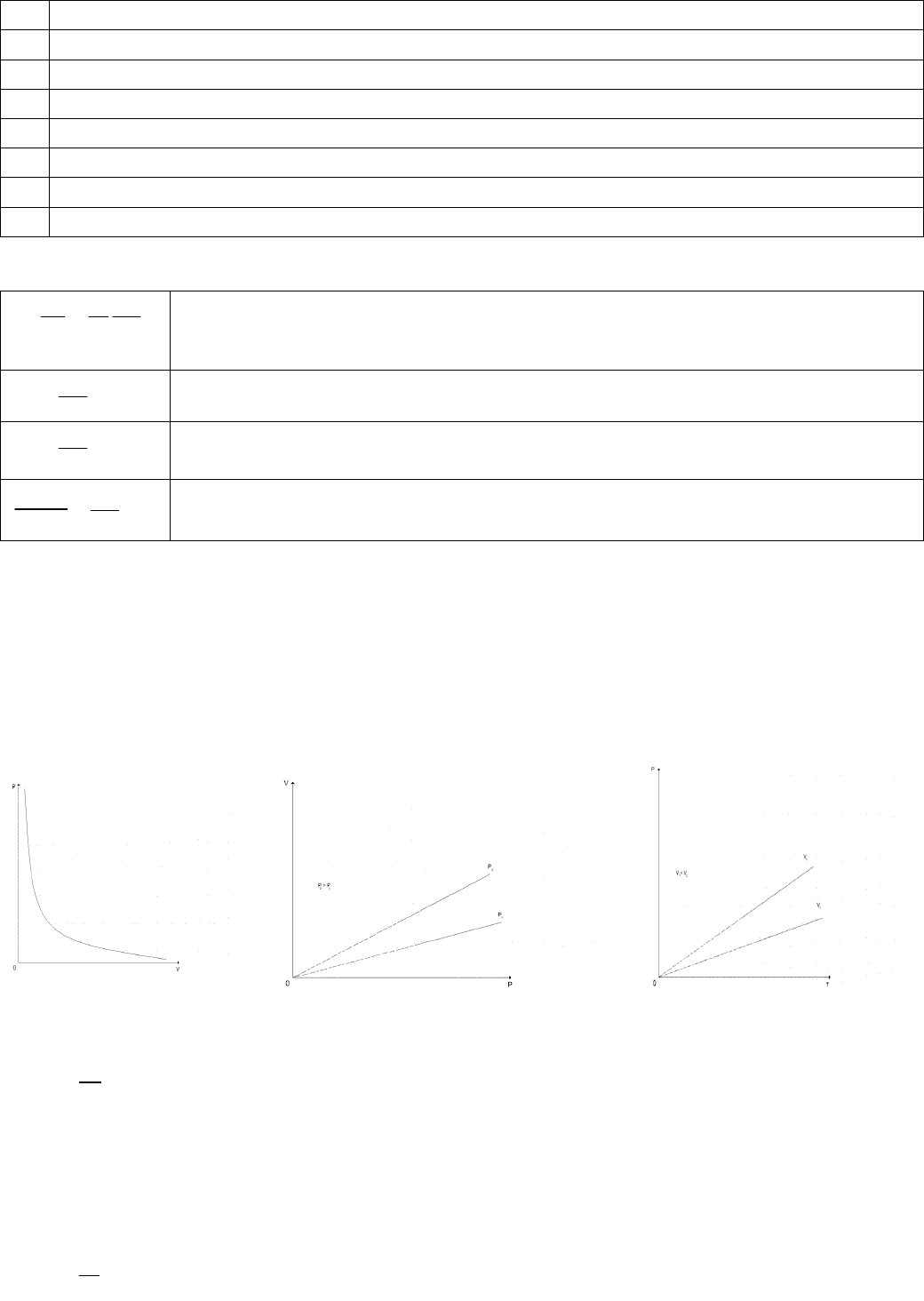
pV=const при Т=const (закон Бойля – Мариотта)
Для газа данной массы произведение давления газа на его объем постоянно,
если температура газа не меняется.
Изобарный
процесс. Процесс изменения отношения состояния термодинамической системы
при постоянном давлении называют изобарным.
T
V
=const при p=const (закон Гей-Люссака)
Для данной массы отношение объема к температуре постоянно, если
давление газа не меняется.
Изохорный процесс. Процесс изменения состояния термодинамической
системы при постоянном объеме называют изохорным.
T
p
=const при V=const (закон Шарля)
Для газа данной массы отношение давления к температуре постоянно, если
объем не меняется.
