Ефимов А.И. и др. Свойства неорганических соединений. Справочник
Подождите немного. Документ загружается.

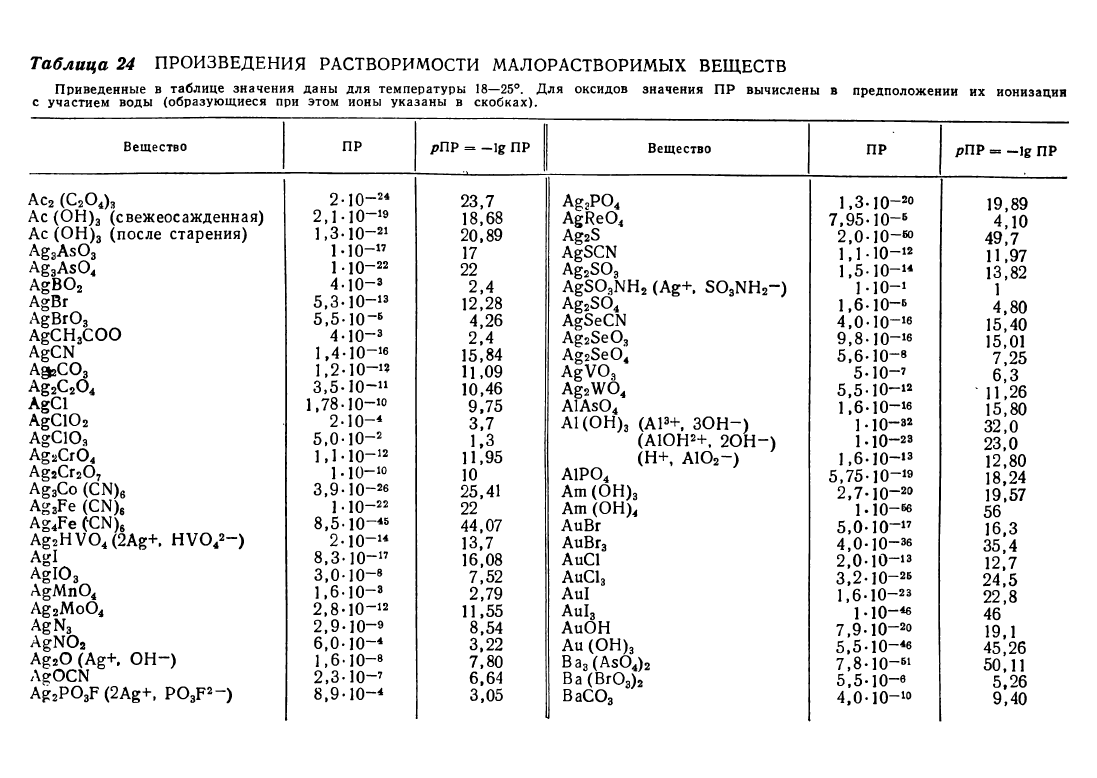
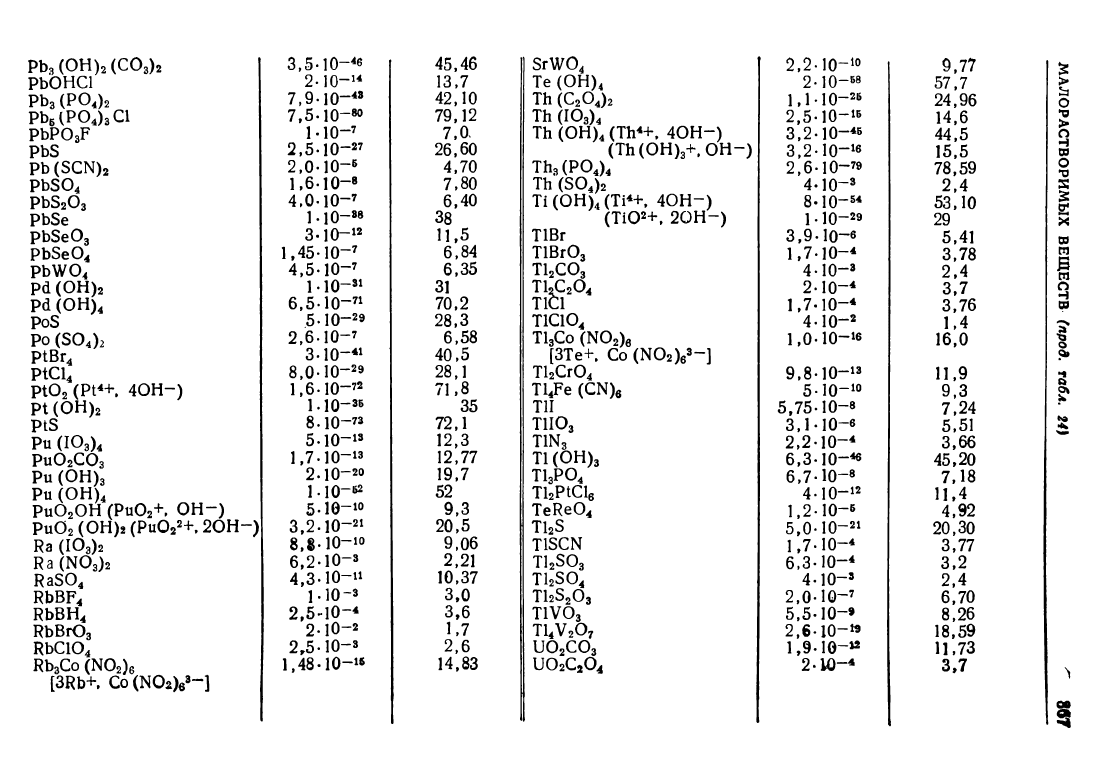
Таблица
24
ПРОИЗВЕДЕНИЯ
РАСТВОРYJМОСТИ
МАЛОРАСТВОРИМЫХ
ВЕЩЕСТВ
Приведеиные
в
таблице
значения
даны
для
температуры
18-25°.
Для
оксидов
значения
ПР
вычислены
в
предположении
их
иониаацнв
с
участием
воды
(образующиеся
при
этом
ионы
указаны
в
скобках).
I
РПР=-lgПР
ПР
Вещество
I
рПР
=
-lg
ПР
11
ПР
Вещество
АС2
(С
2О
4
)
з
2·10-24
23,7
Ag~P04
1
,3·10-20
19,89
Ас
(ОН)з
(свежвосажденная)
2,1·10-19
18,68
AgRe0
4
7,95·10-6
4,10
Ас
(ОН)з
(после
старения)
1,3·10-21
20,89 Ag2S
2,0·10-60
49,7
АgзАsО
з
1·10-17
17
AgSCN
1,1·10-12
11,97
Аg
зАsО
4
1·10-22
22
Аg
2SО
з
1,5·10-14
13,82
AgB0
2
4·10-3
2,4
АgSО
зNН
2
(Ag+.
SОзNН2-)
1·10-1
1
AgBr
5,3·10-
1
З
12,28
Ag
2S0
4
1,6·10-6
4,80
АgВrО
з
5,5·10-6
4,26
AgSeCN
4,0·10-16
15,40
АgСНзСОО
4·10-
З
2,4
Аg
2SеО
з
9,8·10-16
15,01
AgCN
1,4·10-16
15,84
Ag2Se0
4
5,6·10-8
7,25
А~СОз
1,2·10-1~
11,09
АgVО
з
5·10-7
6,3
Ag
2C
2
0
4
3,5·10-11
10,46
Ag
2W0
4
5,5·10-12
' 11,26
AgCl
1,78·10-10
9,75
A1As0
4
1,6·10-16
15,80
AgCI02
2·10-4
3,7
Аl
(ОН)з
(АР+,
30Н-)
1·10-32
32,0
АgСI0
з
5,0·10-2
1,3
(АI0Н2+,
20Н-)
1·10-23
23,0
Ag
2Cr0
4
1,]
·10-12
11,95
(Н+,
AI0
2-)
1,6·]0-IЗ
12,80
Ag2Cr207
1·10-10
10
мю,
5,75.
]0-19
]8,24
АgзСо
(CN)6
3,9·10-26
25,41
Ат
(ОН)з
2,7·10-20
19,57
АgзFе
(CN)s
1·10-22
22
Ат
(ОН)4
1·10-56
56
Ag
4F
е
(·CN)6
8,5·10-45
44,07
AuBr
5,0·10-17
]6,3
Ag2H
V0
4
(2Ag+.
HV0
4
2-)
2·10-14
13,7
АuВrз
4,0·10-
З
6
35,4
AU'I
8,3·]0-17
16,08
AuCl
2,0·10-
1
З
12,7
АgIО
з
3,0·
]0-8
7,52
АuСl
з
3,2·10-26
24,5
AgMn0
4
1,6·10-3
2,79 AuI
1,6·10-23
22,8
Ag
2Mo0
4
2,8·10-12
11,55
АuI
з
1·10-46
46
АgN
з
2,9·10-9
8,54 AuOH
7,9·10-20
19,1
AgN0
2
6,0·10-4
3,22
Au
(ОН)з
5,5·10-46
45,26
Ag
20
(Ag+.
ОН-)
1,6·10-8
7,80
Ваз
(AS0
4)2
7,8·10-61
50,11
AgOCN
2,3·10-7
6,64
Ба (ВrО
З)2
5,5·
]0-6
5,26
А~2РОзF
(2Ag+,
РО
зF2-)
8,9·10-4
3,05
ВаСО
з
4,0·10-10
9,40

в
в
в
в
с
с
Вещество
ПР
I
рПР
~
-12
ПР
~
Вещество
I.
ПР
I
рПР
--lgПР
1, 1·10-7
6,96
Се2
(SеОз)з
3,75·10-26
24',43
1,2·10-10
9,93
СОз
(As0
4
)2
7,6·10-29
28,12
1,1·10-6
5,98
Со
(802)2
3,2·10-9
8,5
3·10-8
7,5
СоСО
з
1,05·10-10
9,98
1
,5·10-9
8,82
СоС
20"
6,3·10-8
7,2
2,5·10-10
9,60
Со
2Ре
(CN)r,
4,8·10-38
37,32
4·10-8
7,40
CoHg (SCN)4
1,5·10-6
5,82
5,0·10-3
2,3
[С
о2+,
Hg (SCN)4
2-]
4·10-7
6,4
Со
(IО
З
)
2
1,0·10-4
4,0
6·10-
З
9
38,22
Со
(NН
Э
)
6
(ВР
4
) 2
4.
]0-6
5,4
3·10-11
10,5
Со
(NН
З)6
(Rе0
4)з
1,7·10-12
11,77
4·10-3
2,4
Со
(ОН)2
(голубая)
6,3·10-16
14,20
5,25·10-2
1,28
Со
(О
Н)2
(розовая
свежео-
1
,6·
]0-16
14,80
8.
]0-7
6,1
сажденная)
1,1·10-10
9,97
Со
(ОН)2
(розовая
после
2,0·10-16
15,70
1,6.
]0-6
4,79
старения)
5·10-8
7,30
Со
(ОН)з
4·10-46
44,4
6,3·10-22
21,2
CoS
(а)
4,0·10-21
20,40
2·]0-14
13,7 CoS
(~)
2,0·10-25
24,70
2,8
·10-10
9,36
сеэ-о,
1,6·10-7
6,8
4·10-36
35,4
CrAsO"
7,8·10-21
20,11
8,]
·10-19
]8,09
Cr
(NН
З)6
(ВF
4)з
6,2·10-6
4,21
7· 10-9
8,85
Cr
(~НЗ)6
(Мn0
4)З
4,0·10-8
7,40
],8·10-31
30,75 Cr
(NН
З
)
6
(Rе04)З
7,7.
]0-12
11
,
11
Cr
(NНз)е
(SОзF)з
4,3·10-4
3,9
Cr
(ОН)2
1,0.
]0-17
17,0
4·]0-10
9,4
Cr
(ОН)З
(Сr
З
+
,
30Н-)
6,3.
]0-31
30,20
1,3.
]0-2З
22,90
(CrOH2+,20H-)
7,9·10-21
20, ]0
1·10-97
97
(Н+,
Н2СrО
з-)
4,0.
]0-16
14,4
6,8.
]0-19
18,17
CrP0
4
(фиолетовый)
1,0.
]0-17
17,00
7,7 ·10-7
6, ]1
CrP0
4
(зеленый)
2,4·10-23
22,62
3,8·
]0-9
8,42
CsAuC1
4
(Cs+,
AuC1
4-)
1·10-3
3
2,3·10-9
8,64
CsBF" (Cs+,
ВР
4-)
2·10-6
4,7
7,1·10-4
3,15
CsBH
4
(Cs+,
ВН
4
-
)
2,5·
10-7
6,6
~
~
::J
."
О
:s:
t.IJ
Qj
tt1
~
tt1
:I:
:s:
~
."
>
о
-1
Qj
О
."
:s:
э:
о
о
-1
~
СаР2
4,0.)
0-11
10,40
с-в-о,
2·10-2
1,7
~
СаНРО4
(Са
2+,
НРО42-)
2,7·10-7
6,57
CsCIO~
4·10-2
1,4
>
~
Са
(Н2Р04)2
1·10-
З
3
с-сю.
4·10-
З
2,4
о
(Са
2+,
2Н
2
Р
04-)
СsзСо
(\;02)~
5,8.
]0-16
]5,24
~
>
Са
(103)2
7,0·10-7
6,]5'
[3Cs+,
Со
(NО
2
)
в
Э
-
]
о
-i
С
а
(N
Н
4)2
Ре
(CN)6
4·10-8
7,4
СsНgСl
з
(Cs+.
НgСl
з-)
2·10-3
2,7
trI
Са
(ОН)2
(Са
2+,
20Н-)
5,5.10-6
5,26
сяо,
]
,0·10-2
2,0
О
~
(СаОН+.
ан-)
1,4·10-4
3,86
сяо,
4,4·10-3
2,36
:s:
с»,
(РО.)2
2,0·10-29
28,70
с-мьо,
9,1·10-5
4,08
~
е:
СаРОзF
(Са
2+.
РОзF2-)
4·10-
З
2,4
Cs
2PtCl
s
3·10-8
7,5
><
Са6
(
Р
0
4
)
З
О
Н
1,6·10-58
57,8
Cs
2PtF
e
2,".
]0-6
5,62
trI
с-зо,
3,2·10-7
6,5
CSR
e0
4
4,0.
]0-4
3,40
rr1
сьзо,
2,5.
]0-5
4,6
Cs
2SiF
s
]
,3.
]0-5
.(,89
S
tt1
СаSеОз
4,7.
]0-6
5,53
Cs
2SnCl&
(2Cs+.
SпСl
s2-)
3,6·10-8
7,4~
о
-i
CaSiF&
8,1·10-4
3,09
Сц,
(ASO.)2
7,6·10-36
35, ]2
trI
CaW0
4
9,0·10-9
8,06
CuBr
5,25·10-9
8,28
"""
са,
(AS0
4
)2
2,2·10-
3 З
32,66
CuCN
3,2·10-20
]9,49
~
с)
са
(802)2
2,3·10-9
8,64
сьсо,
2,5·10-10
9,6
!'-ь
са
(CN)2
1,0·10-8
8,0
СПС
2О
4
3·]0-8
7,5
"'t
~
сасо,
1,0·10-12
12,0
CuCl
]
,2·10-6
5,92
о-
:::.
CdG
20
4
1,5·10-8
7,8
CuCrO..
3,6·10-6
5,44
~
Cd2Fe (CN)s
4,2·10-18
17,38
СП2Ре
(CN)~
1,3·10-16
]5,89
...
......
Cd
(NН
з
) ,
(ВР
4
) 2
2·10-6
5,7
Си!
] ,1·10-12
1],96
Cd
(ОН)2
(Са
2+,
20Н-)
2,2·10-14
]3,66
Сп
по,ь
7,4·10-8
7, ]3
(с
вежеос
ажденн
ая)
сем,
5,0
·10-9
8,3
Cd
(ОН)2
(Cd
2+,
20Н-)
5,9·10-15
]4,23
сь.о
(2Cu+.
ОН-)
1·10-14
]4,0
(после
старения)
Сп
(ОН)2
(Cu
2+,
20Н-)
2,2
·10-20
19,66
Cd
(ОН)2
(Н+,
HCd0
2-)
2·10-19
18,7
(СпОН+,
ОН-)
2,2·10-
1
З
12,66
CdS
] ,6·10-28
27,8
(Н+,
HCU02-)
1·10-19
19,0
сав-о,
5,0·10-9
8,30
Си2
(ОН)2
СО
з
(малахит)
1,7·10-
З
4
33,76
CdW0
4
2·10-6
5,7
с«,
(ОН)2
(СО
З
)
2
(азурит)
],1·10-46
45,96
Се2
(С
2О
4)з
2,5·10-29
28,60
Си
2Р2
0
7
8,3·10-16
15,08
Се
(IО
з)з
3,2·10-10
9,50
CuS
6,3·10-36
35,20
Се
(IOi!)4
5·10-17
16,3
Cu
2
S
2,5·10-48
47,60
Се
(ОН)а
4·10-25
24,40
CuSCN
4,8·10-10
14,32
Се02
(СеО
2+,
2'JH-)
1·10-24
24,0
CuSe
1·10-49
49
Се02
(Се
4+.
40Н-)
1,6·10-15
54,8
сьз-о,
1,7·]0-8
7,78
u)
ф
~
Вещество
I
ПР
I
рПР
-
-lr
ПР
~
Веществ.
I
ПР
I
рПР
-
-lg
П--;-
(~
CuW0
4
]
·10-6
5 K2PtF
8
2,9·10-1.
4,54
FeAs0
4
5,8·10-21
20,24
кн-о,
1
,9.)0-3
2.72
гесо,
3,5·JO-11
10,46
K2S~Fe
8,7
·10-7
6,06
РеС
2О
4
2.JO-7
6,7
K
2TiF
s
5·10-4
3,3
Fe
4
[Fe
(СN)еlз
3,0·10-41
40,52
K2
ZrF
e
5·10-4
3,3
Fe
(ОН)2
(Fe
2+,
20Н-)
8·10-16
15,1
La
(ВrО
з)з
3·10-3
2,5
(FeOH+,
ОН-)
3·1-0-10
9,5
La2
(СО~)з
4·10-34
33,4
(Н+,
HFe02-)
8·10-20
19,1
La2
(С
2О
4
) з
1·10-25
25,0
Fe
(ОН)з
(Fе
З+,
30Н-)
6,3·10-38
37,2
La
(10з)з
6,2.
]0-12
11,2]
(свежеос
ажденн
ая)
La2
(Мо0
4)з
2,2·10-21
20,66
Fe
(ОН)З
(Fе
З
+
,
зан-)
6,3·10-39
38,2
La
(ОН)з
(свежеосажден-
6,5·10-20
19,19
(после
старения)
пая)
Fe
(ОН)з
[Fe
(ОН)2+'
ОН-]
1·10-17
17,0
La
(ОН)З
(после
старения)
1,3·10-21
20,89
[Fe
(ОН)2+,
20Н-]
5·10-27
26,3
Lа2SЭ
2,0.
JO-13
12,70
РеР0
4
1,3·10-22
21,89
La2
(SО,)з
3·10-6
4,5
FeS '
5·10-18
17,3
ььсо,
4,0·10-3
2,40
FeS2 (Fe
2+,
S22-)
6,3.
]0-31
30,2
LiF
1
,7·
]o-~
2.77
FeSe
1. ]0-26
26
цон
4.
]0-2
1,4
Ре2
(SеО
з
)
з
2·10-31
30,7
LiзРО
..
3,2·10-9
8,5
::2
"
Оа
..[Fe
(СN)slз
1,5·10-34
33,82
Мg
з
(AS0
4)2
2,1·10-20
19,68
0-
Оа
(ОН)З
(Оа
З
+
,
30Н-)
]
,6.
]0-37
36,8
MgCO!i
2,1·10-6
4,67
:s:
с.&1
(Н+.
Н2GаОз-)
2,5·10-11
10,6 MgC
20
4
8,5·10-6
4,07
t:J'
t11
ОеО2
(Ое
4+.
40Н-)
}·10-
57
57
MgF
2
6,5·10-9
8,19
~
GeS
3·10-35
34,5
Mg (103)2
3·10-3
2,5
t11
::с
HfO
(ОН)2
(Hf0
2+,
20Н-)
4·10-26
25,4
MgK
2Fe
(CN)s
5·10-9
8,3
:s:
Hg
2
B
r2
(Htt
22+,
2Br-)
5,8·1.()-23
22,24 Mg (NH
4)2Fe
(CN)o
4·10-8
7,4
~
Hg
2CO;j
( ;t22+.
СО
я2-)
8,9·10-17
]6,05
MgNH
4P0
4
2,5.
]0-13
12,6
"о
>
Hg2C204( i
22
+,
С
2О
42-)
1·10-13
]3
Mg
(ОН)2
(свежеосажден-
6,0·10-10
9,22
о
-i
Hg
2C12
(H~
+,
2Сl-)
1,3·10-18
17,88
ная)(М
g2+,
20Н-)
t:J'
Hg
2Cr0
4
(
g22+, CrO.
2-)
5,0.
]0-9
8,70
Mg
(ОН)2
(после
старения)
о
"о
Hg
21
2
(Hg
22+,
21-)
4,5·10-29
28,35
(M
g
2+,
20Н-)
7,1·10-12
11,15
:s:
Hg
2
(103)2(Hg
22+.
210
з-)
2,45·10-14
13,71
(MgOH+,
ОН-)
2,7
·10-9
8,57
э:
о
Hg2HP04 (Hg
22+.
НР04-)
4,0·10-13
12,40
Мg
з
(
Р
04)2
1·10-13
13,0
о
-i
Hg
2
0 (Hg
22+,
20Н-)
1,6·]0-23
22,8
МgSО
з
3·]И-3
2,5
:s;

HgO
(Hg2~.
20Н-)
З,О·10-!8
25,52
МgSеО
з
4,4·10-8
5,36
~
Hg5
(черный)
1.6.
]0-62
51.8
Мп
э
(AS0
4)2
1.9·10-29
28,72
>
:::.
Hg5
(красный)
4,0-10-63
52.40
МпСО
з
1,8-10-11
10,74
О
Hg
2S
(H~22+.
52-)
1-10-47
47
МПС
2О
4
5·]0-6
5.3
~
>
Hg
2
(5С
)2
3,0-10-20
19,52
Мп
2Ре
(CN)6
7,9·10-18
12,10
о
-1'
Нg
250
з
(Hg
22+,
50
з
2-)
1·10-27
27 MnNH
4
P04
1·10-12
12
со
Hg
250
4
(Hg
22+.
5042-)
6,8·10-1
6,17
Мп
(ОН)2
(Мп
2+,
20Н-)
1,9·10-18
12,72
О
"а
Hg5e
1·10-69
59
(МпОН+,
ОН-)
1
.5·10-9
8.82
:s:
~
Нg
25еО
з
(Hg
22+,
5еОз2-)
6,3-10-16
14.2
(Н+,
НМп02-)
1·10-19
19.0
sz:
Hg
2
W0
4
(Hg
22+,
W0
4
2
- )
1,1·10-17
16,96
Мп
(ОН)з
'1·10-16
36
>с
IП
4
[Ре
(СN)s]з
1,9·10-"
43,72
Мп
(ОН)4
1·10-156
56
tD
In
(IО
з)з
3·10-3
2,5
Мп5
(телесного
цвета)
2,5·10-10
9,60
t"I2
!3
In
(ОН)з
(Iп
Э
+
,
ЗОН-)
5·10-Э~
33.3
Мп5
(зеленый)
2.5·10-18
12,60
t"I2
[lп(ОН)2+,20Н-)]
4·10-2~
23.4
МпSеО
з
5.4·10-8
7.27
о
-1
(Н+,
Н
2IпО
8-)
1·10-16
16
Мп
(ОН)4
1·10-50
50
~
IП2SЗ
5.75
·10-74
73,24
(NH4)8A1F6
гзнн,«
АIР
в
8
-
)
1.6·10-3
2,80
~
ьо,
(Ir~+,
40
Н-)
1.6·10-72
71,8
(NН
4
)
з
Со
(N0
2)6
7,6·10-6
5.12
о
ь,о,
2·10-48
47.7
[3NH
4
+,
Со
(N02)e
3
- ]
~
Ir5
2
1·10-7&
75
(NH4)2IrCls
3·10-&
4,5
...
s:.
К
зАIF
е
(3К+,
АIF
6
Э
-
)
1,6·10-9
8,80
(NH.~,>2PtCls
9·10-6
5,05
е
КВР
4
(К+.
BF
4
- )
2·10-8
2,7
Nа
зАIF
в
4.1-10-10
9.39
КВН
4
(К+,
ВН
4
-
)
1,3·10-3
2,7
Nai
BeF
4
7
·10-
З
2.15
~
"
'-
К
(С
6Н
6
) 4
В
[К+,
(С
в
Н
а)4
В
-
]
2,25·10-8
7,65
ныо,
3·10-3
2.5
ксю,
1,1·10-2
1,97
Na5b
(ОН)в
4·10-8
7.4
КзСо
(N0
2)6
4,3·10-10
9,37
[Na+,
5Ь
(ОН)6-]
[3К+.
Со
(N0
2)в
З
-
]
Na
2SiF
g
2.8·10-4
3,56
~
K2Cu2Fe(CN)s
2,2·10-27
26,66
Ni
э
(AS0
4)2
3,1·10-26
25,51
К2
О
е
Р
&
3,0·10-6
4.52
Ni (802)2
2·]0-9
8,7
K
2
HfF
s
2·10-8
2,7
Ni (C
4H
70
2N
2)2
(днметил-
2,3·10-2&
24,64
K
2
IrC1
8
6,8·10-6
4,17
глиоксимат)
кю,
8,3·10-~
3,08
Ni (CN)2 3·10-23
22,5
~NaCo
(N0
2)c
2,2·10-11
10,66
мсо,
1,.3.
]0-7
6.87
[2К+.
Na+,
Со
(N0
2
) 6
З
-
]
мс.о,
4·]0-10
9.4
K
2
PdC1
4
1,6·10-6
4,9
Ni
(СI0
З)2
1.
]0-4
4
K
2
PdCla
6.0·10-6
5,2
Ni
2Fe
(CN)s
1~·10-11
14.89
к.ио,
8·10-8
2,1
Ni
(10з)2
1,4-10-8
7,85
K2PtCle
1,1·10-1
4,96
Ni
(NНз)s
(BF
4
) 2
1-10-6
6
I
~
Ф
tn
Вещество
I
ПР
I
рПР
=-I&,
ПР
~
I
ПР
ГРПР=-I&,ПР
Ig
Вещество
Ni (NH?)s (Re04)2
5,1·]0-4.
3,29
кыо,
5,5·10-~
3,26
Ni
(ОН)2
(свежеооажден-
2,0·]0-16
]4,89
ньмьо,
2,~.
]0-3
2,54
н
ая)
Rb
2PtCls
9·10-8
7,2
Ni
(ОН)2
(после
старения)
6,3.
]0-18
]7,20
Rb
2PtF
s
7,6.
]0-7
6,12
Ni
2P2
0
7
]
,7.
]0-13
]2,77
вьн-о,
9,6·
]o-~
3,02
NiS
«(1)
3,2.
]0-19
]8,50
Rb
2SiF
6
5·]0-7
6,3
NiS
(~)
].
]0-24
24,0
Rb
2TiF
6
5,5.
]0-6
4,26
NiS(g
2,0·]0-26
25,70
Rh
2О
з-(Rh
3+,30Н-)
2·10-4.8
47,7
NiSe
з
]
,0·]0-6
5,0
RU20з
(Ru
3+.
30Н-)
1·10-38
38
Np~2(OH)2
(Np02
2+.
20Н-)
2,5.
]0-22
21,6
Ru
(ОН)4
1. ]0-49
49
РЬ
З
(AS0
4)2
4,].
]0-З6
35,39
SЬ
2О
З
(sь
з
+
,
30Н-)
4·10-4.2
4] ,4
РЬ
(802)2
]
,7.
]0-11
]0,78
(SbO+.
ОН-)
7,9·]0-18
17,1
Pb
Br
2
9,1·]0-6
5.04
(Н+,
Н
2SЬО
з-)
]
,3·]0-12
11,9
РЬ
(ВrО
З
)
2
8,0·10-6
5,]0
Sc
(ОН)з
2.
]о-зо
29,7
РЬСО
з
7,5.
]0-14
]3,13
SnI
2
8,3·
]0-6
5,08
РЬС
2О
4
4,8.
]0-10
9.32
Sn
(ОН)2
(Sn
2
+,
20Н-)
6,3.
]0-27
26,20
РЬС1
2
1,6.
]0-6
4,79
(SnOH+,
ОН-)
4,6.
]0-16
14,34
РЬСIР
2,8.
]0-9
8,55
(Н+,
НSпО2-)
],3.]0-16
]4,9
PbCr0
4
]
,8·]0-14
]3,75
Sn
(ОН)4
1. ]0-67
57
::2
."
РЬР
2
2,7.
]0-8
7,57
SnS
2,5·10-27
26,6
О
Pb
2
Fe (CN)s
9,55.
]0-19
]8,02
Srз
(AS0
4
)2
]
,3.
]0-18
17,1
::s::
~
РЫ
2
]
,1·]0-9
8,98
з-со,
]
,1.
]0-10
9,96
tD
r'I1
РЬ
(lO?)2
2,6.
]0-1З
]2,58
SrC
2
0
4
1,6.10-7
6,80
~
РЬМоО
4
4,0·10-6
5,4
э-с-о,
3,6.
]0-5
4,44
t!1
::r:
РЬ
(N
З)2
2,6.10-9
8,59
SrF
2
2,5·10-9
8,6]
:s::
РЬО
2
(РЬ
4+,
40Н-)
3,0.
]0-66
65,5
Sr
(IО
З
)
2
3,3.
]0-7
6,48
}Q
РЬ
з0
4
(2РЬ
2
+
,
РЬО
4
4
-
)
5,3·10-51
50,28
э-мео,
2·]0-7
6,7
."
>
РЬ
(ОН)2
Sr
(ОН)2
3,2·10-4
3,50
о
--1
(красный)
(РЬ
2+,
20Н-)
5·]0-16
]5,3
Sr;l
(РО
4)2
]·10-31
31
tD
РЬ
(ОН)2
SгРОзF
3·10-3
2,5
е
'tf
(желтый)
(РЬ
2+.
20Н-)
7,9·
10-16
15,1
в-зо,
4·]0-8
7,4
:s::
(РЬОН+,ОН-)
6,3·
]0-9
8.2
э-зо,
3,2·10-7
6.49
~
о
(Н+,
НРЬО
2
-
)
3,2.
]0-16
15,5
SгSеО
з
4.4·
]0-6
5,36
о
~
PbOHBr
2·10-~5
14,7
SrSiF
6
1,5·10-2
1,82
:s;
РЬ
э
(ОН)2
(СО
З)2
3,5·10-46
45,46
SrW0
4
2,2·10-10
9,77
з:
РЬОНСl
2·10-14
13,7
Те
(ОН).
2·10-58
57,7
>
РЬ
З
(РО.)2
7,9·10-48
42,10
ТЬ
(С
2О
4
)
2
1,1·10-20
24,96
~
о
РЬ
6
{Р04)З
Cl
7,5·10-80
79,12
ТЬ
(lОЗ)4
2,5·10-16
14,6
~
>
РЬРОз
F
1·10-7
7,0,
ТЬ
(ОН)4
(ТЬ
4+,
40Н-)
3,2·10-46
44,5
о
PbS
2,5·10-27
26,60
(ТЬ
(ОН)з+,
ОН-)
3,2·10-16
15,5
-t
=
РЬ
сзсхь
2,0·10-6
4,70
ть,
(Р0
4
)
4
2,6·10-79
78,59
О
"
гьзо,
1,6·10-8
7,80
ТЬ
(S04)2
4·10-3
2,4
:s:
РЬS
2О
з
4,0·10-7
6,40 Ti
(ОН)4
(Ti
4+,
40Н-)
8·10-54
53,10
~
е:
PbSe
1·10-88
38
(Ti0
2+,
20Н-)
1·10-29
29
~
РЬSеОз
3·10-12
11,5 TIBr
3,9.10-6
5,41
=
гьзео,
1,45·10-7
6,84
пв-о,
1
,7·10-4
3,78
r!1
PbW0
4
4,5·10-7
6,35
Т1
2СО
з
4·10-3
2,4
.8
r!1
Pd
(ОН)2
1·10-31
31
Tl
cC
20
4
2·10-4
3,7
о
-t
Pd
(ОН)4
6,5·10-71
70,2
Тl
1
1,7·10-4
3,76
~
poS
5·10-29
28,3
TICI0
4
4·10-2
1,4
""
Ро
(S04)2
2,'6.10-7
6,58
тьсе
(N0
2
)
в
1,0·10-16
16,0
~
о
ив-,
3·10-41
40,5
[3Те+,
Со
(N0
2)6
3-]
~
PtC1
4
8,0·10-29
28,1
T1
2Cr0
4
9,8·10-13
11,9
'1
Pt0
2
(Pt
4
+,
40Н-)
1,6.10-72
71,8
Тl.Ре
(CN)s
5·10-10
9,3
Q
Pt
(ОН)2
1·10-36
35
ТlI
5,75·10-8
7,24
~
PtS
8.10-73
72,1
тпо,
3,]
·10-6
5,51
t-a
е
Pu
(IО
З)4
5·10-13
12,3
ТIN
з
2,2·10-4
3,66
и.о.со,
1,7.
]О-IЗ
12,77
Tl
(ОН)з
6,3·10-46
45,20
Pu
(ОН)з
2·10-20
19,7
ты-о,
6,7·10-8
7,18
Pu
(ОН)4
1·10-02
52
тьись
4·10-12
11,4
и.о.он
(PU02+'
ОН-)
5·16-10
9,3
TeR
e0
4
1,2·10-6
4,92
PU02
(ОН)!
(PU02
2+,
20Н-)
3,2·10-21
20,5
тьэ
5,0·10-21
20,30
Ra
(IО
З)2
8,1.
]0-10
9,06
TlSCN
1,7·10-4
3,77
Ra
(NО
з)2
6,2·10-3
2,21
Т1
2SО
з
6,3·10-4
3,2
RaS0
4
4,3·10-11
10,37
T1
2S0
4
4·]0-3
2,4
кьвг;
1·10-3
3,0
Т12S20з
2,0·10-7
6,70
ньвн,
2,5
..
10-4
3,6
пуо,
5,5·10-'
8,26
ньв-о,
2·10-2
1,7
тъу,о,
2,6·10-19
18,59
RbCI0
4
2~5·10-3
2,6
U0
2СО
з
1
,9.
](~-i2
11,73
RЬзСо
(N02)6
1,48·10-16
14,83
U02C
2
0
4
2·Ю-~
3,7
[3Rb+,
Со
(N02)e
3-]
I
08
~

I
рПР
=
-lg
ПР
11
--,-
I
рПР=-lgПР
I~
Вещество
I
ПР
Вещество
ПР
i::J
I
I~
о
:s:
CIJ
(U0
2)2
Ре
(CN)6
7,1·10-1.
13,15
Zп
з
(AS0
4)2
1,3·10-27
27,89
tJj
t't1
U(J2
HAs0
4
3,2·]0-11
10,50
Zn (CN)2
2,6·10-13
12,59
~
t't1
(U0
2
2+,
HAs0
42-)
::r:
ZпСО
з
1,45·10-11
10,84
:s:
U02HP04
(U0
22+,
НРО42-)
2,14·10-11
]0,67
~
ZnC
20
4
2,75·10-8
7,56
~
>
U0
2
(103)2
3·10-8
7,5
Zn2Fe (CN)6
2,1·10-16
15,58
о
-t
цо.кмо,
2,5·10-23
22,60
tJj
ZnHg (SCN)4
2,2·10-7
6,66
О
~
U0
2K
P04
7,8·10-2.
23,11
[Zn
2+.
Hg (SCN)4
2-]
:s:
~
цо.ни.х,о,
1,7·10-24
23,77
Zn (103)2
2,0·10-8
7,7
О
о
U0
2
NH
4
P0
4
4,4·10-27
26,36
Zn
(ОН)2
(Zn
2+,
20Н-)
1,2·10-17
16,92
-t
:s:
U0
2NaAs0
4
1,3·10-22
21,87
(ZnOH+.
ОН-)
3,0·10-13
12,52
~
>
U
(ОН~з
1·]0-19
19,0
Zn
3
(Р0
4)2
9,
]·]0-33
32,04
~
о
~
U
(ОН)4
]·10-45
45,0 ZtiS
(сфалерит)
]
,6·]0-2.
23,80
>
о
ИО
2
(ОН)2
(U0
22+.
20Н-)
1·10-22
22,0
ZnS
(вюртцит)
2,5·]0-22
21,60
-t
tJj
О
VO
(ОН)2
7,4·10-23
22,13
ZnSe
1·10-31
31
~
:s:
V
20
5
(V0
2+,
ОН-)
1,6·10-15
14,8
ZnSeOJ
]
,9·]0-8
7.72
з
!2:
(VО)з
(Р0
4)2
8·10-25
24, ]
Zr
(ОН)4
(Zr
4+.
40Н-)
].
]0-62
52,0
:><
tJj
W
(ОН)4
1·10-50
50,0
[Zr
(ОН)2
2+.
20Н-]
3,2·10-26
25,5
~
Е
у
(ОН)з
3,2·10-26
24.5
Zrз
(Р0
4)2
1·]0-132
132
t't1
о
-t
Ф
~
't3
с)
~
"i
~
0\
:о.
~
~
"-
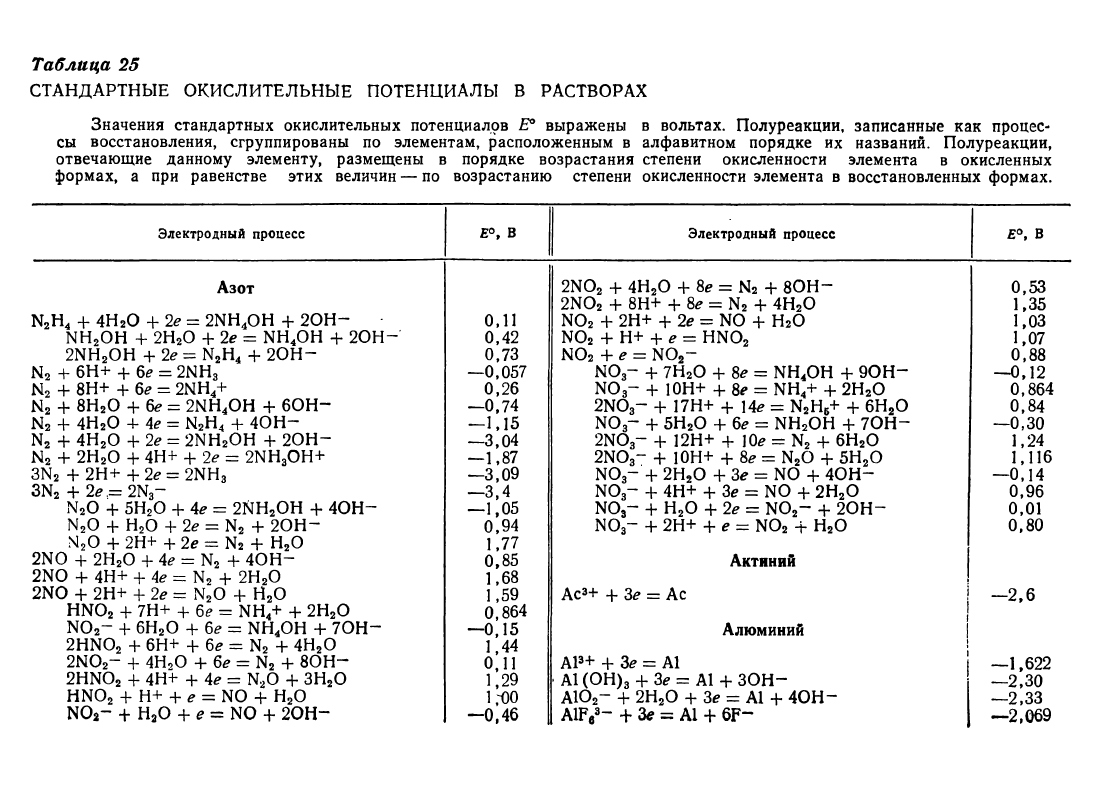
Та6лuца25
СТАНДАРТНЫЕ
ОКИСЛИТЕЛЬНЫЕ
ПОТЕНUИАЛЫ
В
РАСТВОРАХ
Значения
стандартных
окислительных
потенциалов
во
выражены
в
вольтах.
Полуреакции.
записанные
как
пропес
..
сы
восстановления,
сгруппированы
по
элементам,
расположенным
в
алфавитном
порядке
их
названий.
Полуреакции,
отвечающие
данному
элементу,
размещены
в
порядке
возрастания
степени
окнсленностн
элемента
в
окисленных
формах,
а
при
равенстве
этих
величин
-
по
возрастанию
степени
окисленности
элемента
в
восстановленных
формах.
Электродный
процесс
I
ЕО,
В
"
Электродный
процесс
I
ЕО,
В
Азот
2N0
2
+
4Н
2О
+
8е
=N
2
+
80Н-
0,53
2N0
2
+
8Н+
+
8е
=N
2
+
4Н
2О
1,35
N
2H
4
+
4Н
2
О
+
2е
==
2NH
40H
+
20Н-
0,11
N0
2
+
2Н+
+
2е
==
NO +
Н
2О
1,03
NH
20H
+
2Н
2О
+
2е
= NH
40H
+
20Н-'
0,42
N0
2
+
Н+
+
е
==
HN0
2
1,07
2NH
20H
+
2е
==
N
2H
4
+
20Н-
0,73
N0
2
+
е
==
N0
2
-
0,88
N
2
+
6Н+
+
6е
==
2NН
з
-0,057
NО
з-
+
7Н
2О
+
8е
==
NH
40H
+
90Н-
-0,12
N
2
+
8Н+
+
6е
==
2NH
4+
0,26
NО
з-
+
10Н+
+
8е
=NH
4+
+
2Н
2О
0,864
N
2
+
8Н
2О
+
бе
==
2NH
40H
+
60Н-
-0,74
2NО
з-
+
17Н+
+
14е
=N
2H
6+
+
6Н
2О
0,84
N
2
+
4Н
2О
+
4е
=N
2H
4
+
40Н-
-1,15
NО
з-
+
5Н
2О
+
6е
==
NH
20H
+
70Н-
-0,30
N
2
+
4Н
2О
+
2е
=2NH
20H
+
20Н-
-3,04
2NО
з-
+
12Н+
+
]Ое
==
N
2
+
6Н
2О
1,24
N
2
+
2Н
2О
+
4Н+
+
2е
=
2NН
зОН+
-1,87
2NО
з-:-
+
10Н+
+
8е
==
N
20
+
5Н
2О
1,116
3N
2
+
2Н+
+
2е
=
2NН
з
-3,09
NО
з-
+
2Н
2О
+
3е
==
NO +
40Н-
-0,14
3N
2
+
2е:=
2N
з-
-3,4
NО
з-
+
4Н+
+
3е
=NO +
2Н
2О
0,96
N
20
+
5Н
2О
+
4е
=2NH
20H
+
40Н-
-1,05
NО
з-
+
Н
2О
+
2е
=
N0
2-
+
20Н-
0,01
N
20
+
Н
2О
+
2е
=N
2
+
20Н-
0,94
NО
з-
+
2Н+
+
е
==
N0
2
+
Н
2О
0,80
N
20
+
2Н+
+
2е
==
N2 +
Н
2О
1,77
2NO
+
2Н
2О
+
4е
==
N
2
+
40Н-
0,85
Актиний
2NO +
4Н+
+
4е
==
N
2
+
2Н
2О
1,68
2NO
+
2Н+
+
2е
==
N
20
+
Н
2
О
1,59
Ас
3
+
+
3е
==
Ас
!
-2,6
HN0
2
+
7Н+
+
6е
==
NH
4+
+
2Н
2О
0,864
N0
2
-
+
6Н
2О
+
6е
= NH
40H
+
70Н-
-0,15
Алюминий
2HN0
2
+
6Н+
+
6е
==
N
2
+
4Н
2О
1,44
2N0
2
-
+
4Н
2О
+
6е
==
N
2
+
80Н-
0,11
АР+
+
3е
==
Аl
I
-1,622
2HN0
2
+
4Н+
+
4е
==
N
20
+
3Н
2О
1,29
· Al
(ОН)з
+
3е
==
Аl
+
30Н-
I
-2,30
HN0
2
+
Н+
+
е
=NO +
Н
2О
1;00
AI0
2
-
+
2Н
2О
+
3е
=Al +
40Н-
-2,33
N02-
+
Н
2О
+
е
= NO +
20Н-
-0.46
АIР
е
3
-
+
Зе;;
Al +
6Р-
-2.069

ЭJlектродный
процесс
I
ЕС,
В
I
ЭJlектродный
процесс
I
~.
в
I~
Америций
Висмут
Аm
З+
+
3е
=
Ат
-2,32
Bi
3
+ +
3е
=
Вl
0,2
Аm
(ОН)з
+
3е
=
Аm
+
30Н-
-2,71
BiO+ +
2Н+
+
3е
==
В!
+
Н
2
О
0,320
Аm
4+
+
е
=
Аm
3+
2,18
BiOCl +
2Н+
+
3е
==
В!
+
Н
2О
+
Сl-
0,160
Аm02+
+
4Н
~
+
2е
==
Аm
З+
+
2Н
2О
1,721
BiOOH
+
Н
2О
+
3е
==
В!
+
30Н-
-0,46
Аm02+
+
4Н+
+
е
=
Аm
4+
+
2Н
2О
1,261
8120з
+
3Н
2О
+
6е
==
2В!
+
60Н-
-0,46
Аm022+
+
4Н+
+
3е
==
Аm
3+
+
2Н
2О
1,694
Вi
2О
з
+
6Н+
+
6е
==
2В!
+
3Н
2О
0,371
АmО22+
+
е
=
Аm02+
1,639
BiCJ
4
-
+
3е
==
Bi +
4Сl-
0,16
NаВiО
з
+
4Н+
+
2е
==
BiO+ +
Na+
+
2Н
2О
>1,8
Астат
At
2
+
2е
=
2At-
0,2
Водород
2HAtO
+
2Н+
+
2е
==
At
2
+
2Н
2О
0,7
Н
2
+
2е
=
2Н-
-2,25
2AtO-
+
2Н
2О
+
2е
==
At
2
+
40Н-
0,0
2Н+
+
2е
==
Н2
0,0000
НАtО
з
+
4Н+
+
4е
==
HAtO +
2Н
2О
1,4
20+
+
2е
==
D
2
-0,0034
АtО
з-
+
2Н
2
О
+
4е
+
AtO-
+
40Н-
0,5
2Н
2О
+
2е
==
Н
2
+
20Н-
-0,828
2020
+
2е
= 02 +
200-
-0,87
Барий
Н
2О
2
+
2Н
+ +
2е
==
2Н20
1,776
n
Ва
2+
+
2е
==
Ба
-2,906
-1
Вольфрам
>
ВаО2
+
4Н+
+
2е
==
Ва
2+
+
2Н
2О
2,365
::с
~
W0
2
+
4Н+
+
4е
==
W +
2Н
2
О
-0,10
>
Бериллий
0,043
~
W
2О
б
+
2Н
+ +
2е
==
2W0
2
+
Н
2О
-1
Ве
2+
+
2е
=:
Ве
0,57
::с
-1,847
W
(СN)в
З
-
+
е
==
W (CN)B
4
-
е:
ВеО
+
Н
2О
+
2е
=
Ве
+
20Н-
-2,6]3
WО
з
+
6Н+
+
6е
==
W +
3Н
2О
-0,090
r!1
Ве022-
+
4Н+
+
2е
==
Ве
+
2Н
2О
-0,909
W0
4
2
-
+
4Н
2О
+
6е
==
W +
80Н-
-1,05
о
Ве20з2-
+
3Н
2О
+
4е
==
2Ве
+
60Н-
-2,63
WOi-
+
8Н+
+
6е
==
W +
4Н
2О
0,049
~
0,801
:s:
2W0
4
2-
+
6Н+
+
2е
==
W
2О
б
+
3Н
2О
о
Берклий
2WО
з
+
2Н+
+
2е
==
W
20
6
+
Н
2
О
0,03
~
:s::
Bk4+ +
е
==
Вk
З
+
1,6
-1
Гадолиний
r!1
:::а
Бор
tr
Gd
З
+
+
3е
==
Gd
-2,397
::с
НзВО
а
+
3Н+
+
3е
==
В
+
3Н
2
О
-0,870
Gd
(ОН)з
+
3е
==
Gd +
30Н-
-2,82
2:
~
